KR20140057718A - Redox-responsive polymer-photosensitizer conjugate containing disulfide linker and its composition for fluorescence imaging and photodynamic therapy comprising thereof - Google Patents
Redox-responsive polymer-photosensitizer conjugate containing disulfide linker and its composition for fluorescence imaging and photodynamic therapy comprising thereofDownload PDFInfo
- Publication number
- KR20140057718A KR20140057718AKR1020120123244AKR20120123244AKR20140057718AKR 20140057718 AKR20140057718 AKR 20140057718AKR 1020120123244 AKR1020120123244 AKR 1020120123244AKR 20120123244 AKR20120123244 AKR 20120123244AKR 20140057718 AKR20140057718 AKR 20140057718A
- Authority
- KR
- South Korea
- Prior art keywords
- polymer
- photosensitizer
- cancer
- fluorescence
- conjugate
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/409—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil having four such rings, e.g. porphine derivatives, bilirubin, biliverdine
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K41/00—Medicinal preparations obtained by treating materials with wave energy or particle radiation ; Therapies using these preparations
- A61K41/0057—Photodynamic therapy with a photosensitizer, i.e. agent able to produce reactive oxygen species upon exposure to light or radiation, e.g. UV or visible light; photocleavage of nucleic acids with an agent
- A61K41/0071—PDT with porphyrins having exactly 20 ring atoms, i.e. based on the non-expanded tetrapyrrolic ring system, e.g. bacteriochlorin, chlorin-e6, or phthalocyanines
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/001—Preparation for luminescence or biological staining
- A61K49/0013—Luminescence
- A61K49/0017—Fluorescence in vivo
- A61K49/0019—Fluorescence in vivo characterised by the fluorescent group, e.g. oligomeric, polymeric or dendritic molecules
- A61K49/0021—Fluorescence in vivo characterised by the fluorescent group, e.g. oligomeric, polymeric or dendritic molecules the fluorescent group being a small organic molecule
- A61K49/0036—Porphyrins
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Gastroenterology & Hepatology (AREA)
- Inorganic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
Translated fromKoreanDescription
Translated fromKorean본 발명은 환원제의 작용에 의하여 형광 및 반응성 산소 생성이 활성화되는 결합체에 관한 것으로, 더 자세하게는 암세포 선택적 형광 영상 또는 광역학 치료를 위한 이황화물 연결자 함유 고분자-광감각제 결합체에 관한 것이다.
The present invention relates to a conjugate in which fluorescence and reactive oxygen production are activated by the action of a reducing agent, and more particularly to a disulfide linker-containing polymer-photosensitizer conjugate for cancer cell selective fluorescence imaging or photodynamic therapy.
광역학 치료법(photo dynamic therapy: PDT)은 광감각제(photo-sensitizer)를 이용하여 수술 없이 암 등의 난치병을 치료하는 기술을 일컫는다. 이러한 광역학 치료법(PDT)은 BC 1400년경부터 시도되어 20세기 초부터 활발한 연구가 진행되었고, 현재에 이르러는 암의 진단과 치료, 동맥경화 및 관절염을 포함한 염증성 질환의 치료, 치과 질환 치료, 자가골수이식, 항생제, AIDS 치료, 피부이식 수술이나 피부질환 등의 치료에서 사용되고 있으며 그 응용범위는 점차 확대되고 있다.
Photodynamic therapy (PDT) refers to the treatment of intractable diseases such as cancer without surgery using a photo-sensitizer. These photodynamic therapies (PDTs) have been tried since around 1400 BC and have been actively researched since the early 20th century, and nowadays they have been used for the diagnosis and treatment of cancer, for the treatment of inflammatory diseases including arteriosclerosis and arthritis, Bone marrow transplantation, antibiotics, AIDS treatment, skin transplant surgery and skin diseases, and its application range is gradually expanding.
광감각제는 특정 파장의 빛에 조사되어 에너지적으로 여기(excitation)될 수 있으며, 이때 형광 신호를 발생하거나, 여기된 에너지를 주변의 기질 또는 산소에 전달하여 반응성 산소종(일항산소, 산소 라디칼, superoxide 및 peroxide 등)을 생성하면서 주변 종양 세포를 자멸(apoptosis) 또는 괴사(necrosis) 시킬 수 있다.
The photosensitizer can be energized by being irradiated with light of a specific wavelength, generating a fluorescence signal or transferring the excited energy to the surrounding substrate or oxygen to generate reactive oxygen species (unilateral oxygen, oxygen radical , superoxide and peroxide, etc.), while surrounding tumor cells can be apoptotic or necrosis.
현재 광역학 치료 요법에 사용되고 있는 광민감성 물질로는 포르피린(porphyrin) 유도체, 클로린(chlorin), 박테리오클로린(bacteriochlorin), 프탈로시아닌(phthalocyanine), 5-아미노레불린 산(5-aminolevulinic acid) 유도체 등이 알려져 있으며, 광민감성 사이클릭 테트라피롤 유도체는 암세포에 선택적으로 축적될 뿐만 아니라 화합물의 특성상 형광이나 인광을 나타내므로 종양의 조기진단 시약으로도 활용될 수 있는 특징이 있다.
Currently, photosensitizers used in photodynamic therapies include porphyrin derivatives, chlorin, bacteriochlorin, phthalocyanine, 5-aminolevulinic acid derivatives and the like. And the photosensitized cyclic tetrapyrrole derivatives selectively accumulate in cancer cells and exhibit fluorescence or phosphorescence due to the characteristics of the compounds, and thus can be used as an early diagnosis reagent for tumors.
또한, 암세포 뿐만 아니라 정상세포에도 심각한 독성효과를 나타내는 부작용을 갖는 항암제와는 달리, 광감각제는 빛에 노출되지 않으면 높은 농도에서도 세포 독성을 거의 나타내지 않으므로 빛에 노출되지 않은 정상 세포는 그대로 보존하면서 암세포만 선택적으로 제거할 수 있기 때문에 반복치료가 가능하며, 대부분 전신 마취의 위험성을 배제할 수 있으며, 간단한 국소 마취만으로도 수술할 수 있는 등 시술이 용이한 장점도 있다.
Unlike anticancer drugs, which have serious adverse effects not only on cancer cells but also on normal cells, the photosensitizer shows little cytotoxicity even at high concentrations if not exposed to light, so that normal cells not exposed to light are preserved Since only cancer cells can be selectively removed, it is possible to perform repeated treatment. Mostly, the risk of general anesthesia can be excluded, and there is also an advantage that easy operation such as surgery can be performed with a simple local anesthetic.
다만, 광감각제를 이용한 광역학 치료법이 기존의 항암치료나 방사선 치료에서 보이는 부작용을 현저히 줄이면서도 암 치료 효과는 극대화할 수 있는 장점이 있으나, 광역학 치료 후 발생하는 피부 광민감성(skin photosensitivity)의 문제가 지적되고 있다. 일례로, 미국 식약청의 허가를 받아서 암치료에 사용되는 광감각제인 Photofirin®의 경우, 정상조직에 비특이적으로 축적되어 광역학 치료 후에도 오랜기간 광감각제가 피부와 눈 등에 잔존하므로, 환자가 빛에 노출되는 경우 피부 또는 눈의 정상세포를 죽이는 피부 광민감성 부작용을 보인다. 이러한 피부 광민감성 부작용을 피하기 위하여 환자는 광역학 치료 시술 후 6주 이상 빛이 없는 환경에서 생활해야하는 불편함이 있다. 또한, 광감각제가 종양 조직 주변의 정상조직에도 쌓이는 경우 표적-대비-배경신호 비(target-to-background signal ratio)가 나빠지기 때문에 광감각제를 이용한 종양의 형광 영상 진단에 효율적이지 못하다.
However, photodynamic therapy using photodynamic agents has the advantage of maximizing the effect of cancer treatment while significantly reducing the side effects seen in conventional chemotherapy or radiation therapy, but it is also effective in the treatment of skin photosensitivity after photodynamic therapy, Is a problem. For example, in the case of Photofirin® , a phototherapeutic agent used in cancer treatment with the permission of the US Food and Drug Administration, nonspecific accumulation in normal tissues causes photodynamic agents to remain on the skin and eyes for a long time after photodynamic therapy, If it does, it exhibits skin-light-sensitive side effects that kill normal cells in the skin or eye. In order to avoid such skin photosensitivity side effects, the patient has to live in a light-free environment for 6 weeks or more after the photodynamic therapy. In addition, when the photosensitizer is deposited on normal tissue around the tumor tissue, the target-to-background signal ratio deteriorates, making it ineffective for fluorescence imaging of the tumor using the photosensitizer.
이에, 정상조직에 대한 비특이적 축적을 줄이기 위한 친수성 특성을 갖는 개질된 광감각제가 개발되고 있다. 그러나, 친수성이 증가된 광감각제는 정상세포에 대한 비특이적인 축적이 감소되고 체내에서 보다 빠르게 배출 되어 피부 광민감성 지속 기간이 상당히 단축되는 장점이 있는 반면, 치료에 충분한 양이 종양 조직에 전달되기 위해서는 용량을 높여서 투여해야하는 단점이 있으며, 암 세포 내 침투도 어렵기 때문에 광역학 치료 효능이 낮아진다는 단점이 있다. 따라서, 암 세포에 특이적으로 축적률을 높이고, 부작용이 없으며, 치료 효과가 우수한 새로운 광역학 치료제의 개발이 요구되고 있는 실정이다.
Accordingly, a modified photosensitizer having hydrophilic properties for reducing nonspecific accumulation in normal tissues has been developed. However, the photosensitizer with increased hydrophilicity has the advantage of reducing non-specific accumulation in normal cells and discharging more rapidly in the body, thereby significantly shortening the duration of skin photosensitivity, while sufficient amount of therapeutic agent is delivered to the tumor tissue However, there is a disadvantage in that the administration dose should be increased, and the penetration into cancer cells is also difficult, so that the photodynamic therapy effect is lowered. Therefore, there is a demand for development of a new photodynamic therapy agent which has a specific accumulation rate in cancer cells, has no side effects, and has excellent therapeutic effect.
이에, 본 발명자들은 암세포에 선택적으로 반응하여 형광 영상 진단이 가능하고 광역학 치료가 가능한 신규한 광역학 치료제를 개발하기 위해서 연구하던 중, 이황화물 연결자로 결합된 고분자-광감각제 결합체가 암 세포내로 들어갔을 때만 선택적으로 형광 신호 및 반응성 산소 생성이 활성화 된다는 점을 확인하고 본 발명을 완성하였다.
Accordingly, the present inventors have conducted studies to develop a novel photodynamic therapeutic agent which can selectively undergo fluorescence imaging and photodynamic therapy by selectively reacting with cancer cells, and have found that a polymer-photosensitizer conjugate bound to a disulfide linker is a cancer cell The present inventors confirmed that the fluorescence signal and the reactive oxygen generation are selectively activated only when they enter the sample.
본 발명은 형광 신호 발생 및 광역학 치료 효과가 표적 환부에서 보다 선택적으로 일어남으로써 질병 병소의 형광 영상 진단 효율을 높이고 광역학 치료 부작용을 줄일 수 있는 이황화 연결자로 결합된 고분자-광감각제 결합체 및 이를 함유하는 광역학 치료 또는 진단용 조성물에 관한 것이다.
The present invention relates to a polymer-photosensitizer conjugate combined with a disulfide linker capable of enhancing the fluorescence imaging efficiency of a diseased lesion and reducing side effects of photodynamic therapy by generating a fluorescence signal and a photodynamic therapy effect more selectively in the target lesion, To a photodynamic therapy or diagnostic composition containing the same.
상기 과제를 해결하기 위하여, 본 발명은 광감각제; 고분자; 및 상기 광감각제와 상기 고분자를 공유결합으로 연결하는 연결자를 포함하고, 상기 연결자는 이황화물 결합(disulfide bond)을 포함하는 이황화물 연결자로 결합된 고분자-광감각제 결합체를 제공한다.
In order to solve the above-mentioned problems, the present invention provides a photo- Polymer; And a connector for covalently coupling the photo-sensing agent and the polymer, wherein the connector comprises a disulfide bond and a polymer-photo-sensing agent conjugate bonded to the disulfide linker.
본 발명에서는 상기 지지체로 사용되는 고분자에 다수의 광감각제를 결합시킴으로써, 광감각제간의 거리가 10nm 이내로 가까워지고 그 결과, 광감각제들 간의 에너지 전달현상(resonance energy transfer)에 의한 에너지 소광(quenching) 현상이 일어나도록 유도한다. 이 경우에는, 광감각제가 빛에 의해서 조사되더라도 형광 신호를 발생하지 못하고 반응성 산소도 생성하지 못한다. 더욱이, 결합된 광감각제 간의 응집(aggregation)이 일어나게 되면 소광 현상이 매우 효과적으로 일어난다.
In the present invention, by attaching a plurality of photosensitizers to the polymer used as the support, the distance between the photosensitizers approaches 10 nm or less, and as a result, energy extinction by resonance energy transfer between the photosensitizers quenching phenomenon occurs. In this case, even if the photosensitizer is irradiated with light, it does not generate a fluorescence signal and does not generate reactive oxygen. Furthermore, when aggregation occurs between the combined photosensitizers, quenching occurs very effectively.
본 발명의 상기 이황화물 연결자로 결합된 고분자-광감제 결합체가 암세포내로 섭취되는 경우에는, 세포내 리소좀에 높은 농도로 존재하는 글루타티온(glutathione)에 의해서 이황화물 연결자가 끊어지게 되고, 광감각제가 고분자로부터 이탈되면서 광감각제 간의 거리가 멀어지기 때문에 형광신호 및 반응성 산소 생성이 다시 활성화된다. 이황화물 연결자를 분해할 수 있는 글루타티온은 혈액내에는 2 μM의 낮은 농도로 존재하지만, 세포내에서는 2~10 mM의 높은 농도로 존재한다 (D.P. Jones, J.L. Carlson, P.S. Samiec, P. Sternberg, Jr., V.C. Mody, Jr., R.L. Reed, L.A. Brown, Clin. Chim. Acta (1998) 275, 175-184; dR. Cheng, F. Feng, F. Meng, C. Deng, J. Feijen, Z. Zhong, J. Controlled Release (2011) 152, 2-12).
When the polymer-photosensitizer conjugate bound to the disulfide linker of the present invention is ingested into cancer cells, the disulfide linker is cleaved by glutathione present in a high concentration in the intracellular lysosome, and the photo- The fluorescence signal and reactive oxygen production are activated again because the distance between the photosensitizer is increased. Glutathione, which can disassociate disulfide linkers, is present at a low concentration of 2 μM in the blood but at a high concentration of 2 to 10 mM in the cells (DP Jones, JL Carlson, PS Samiec, P. Sternberg, Jr Cheng, F. Feng, F. Meng, C. Deng, and J. Feijen, Z. (eds.), VC Mody, Jr., RL Reed, LA Brown, Clin. Chim. Acta (1998) 275, 175-184; Zhong, J. Controlled Release (2011) 152, 2-12).
본 발명에서 광감각제의 결합을 위하여 지지체(backbone)로 사용되는 상기 고분자는 생체 적합성 고분자(biopolymer 또는 biomacromolecules) 또는 합성 고분자(synthetic polymer) 중에서 선택될 수 있다.
In the present invention, the polymer used as a backbone for binding a photosensitizer may be selected from a biopolymer or biomacromolecules or a synthetic polymer.
본 발명에서 상기 생체적합성 고분자는 생체 내에서 생체적합성을 갖는 모든 고분자가 사용될 수 있으며, 생체적합성 및 생분해성이 우수하고, 생체 내의 안정성이 우수하여 혈액 내에서의 생체 분포도가 높아 암 조직에 축적되는 특성을 지니는 것이 바람직하다. 상기 생체적합성 고분자의 바람직한 예로는 히알루론산(hyaluronic acid), 젤라틴(gelatin), 콜라겐(collagen), 키토산(chitosan), 글리콜 키토산(glycol chitosan), 헤파린(heparin), 헤파란 설페이트(heparan sulfate), 풀루란(pullulan), 콘드로이틴 설페이트(chondroitin sulfate), 엘라스틴(elastin), 덱스트란(dextran) 또는 알부민(albumin)인 것이 바람직하다.
In the present invention, the biocompatible polymer may be any polymer having biocompatibility in vivo. The biocompatible polymer is excellent in biocompatibility and biodegradability, has excellent stability in the living body, has high bio-distribution in the blood, Characteristics. Preferred examples of the biocompatible polymer include hyaluronic acid, gelatin, collagen, chitosan, glycol chitosan, heparin, heparan sulfate, It is preferably pullulan, chondroitin sulfate, elastin, dextran, or albumin.
또한 상기 합성 고분자는 폴리아크릴산(polyacrylic acid), 폴리라이신(poly-L-lysine), 폴리에틸렌글리콜-폴리 라이신(polyethylene glycol-grafted-poly-L-lysine), 폴리아스파틱산 (polyaspartic acid), 폴리에틸렌글리콜-폴리아스파틱산 (polyethylene glycol-grafted-polyaspartic acid), 폴리글루타믹산(polyglutamic acid), 폴리에틸렌글리콜-폴리글루타믹산 (polyethylene glycol-grafted-polyglutamic acid), 히드록시프로필메타크릴아미드 공중합체 (N-(2-hydroxypropyl)methacrylamide (HPMA) copolymer), 폴리에틸렌 이민(polyethylene imine), 폴리에틸렌글리콜-폴리에틸렌이민 (polyethylene glycol-grafted-polyethylene imine), 폴리비닐알코올(polyvinyl alcohol) 또는 덴드리머(dendrimers)인 것이 바람직하다.
The synthetic polymer may be selected from the group consisting of polyacrylic acid, poly-L-lysine, polyethylene glycol-grafted-poly-L-lysine, polyaspartic acid, Polyglycolic acid, polyethylene glycol-grafted-polyglutamic acid, hydroxypropylmethacrylamide copolymer (N, N'-diphenylmethacrylate, (2-hydroxypropyl) methacrylamide (HPMA) copolymer, polyethylene imine, polyethylene glycol-grafted-polyethylene imine, polyvinyl alcohol or dendrimers Do.
상기 고분자와 광감각제를 연결시키기 위한 이황화물 결합을 포함하는 이황화물 연결자는 글루타티온 등의 환원제에 의해서 이황화 결합이 분해된다. 이황화물 결합을 포함하는 이황화물 연결자의 양쪽 말단기 화학구조는 고분자 및 광감각제의 관능기(functional group)에 따라서 적절한 것을 사용할 수 있으며, 고분자와 광감각제가 모두 카르복실산(carboxylic acid)을 관능기로 갖고 있는 경우에는 하기 화학식 1로 표시되는 화합물과 같은 이황화물 연결자를 사용할 수 있다. 이 경우, 고분자의 카르복실산이 하기 화학식 1로 표시되는 화합물의 한쪽의 아민기와 아미드 결합 (amide bond)으로 공유 결합을 이루고, 광감각제의 카르복실산은 다른 한쪽의 아민기와 아미드 결합을 이루는 고분자-광감각제 결합체를 제공한다.The disulfide linkage containing a disulfide bond for linking the polymer with the photosensitizer is decomposed by a reducing agent such as glutathione. Both end-group chemical structures of the disulfide linkage including disulfide linkages can be appropriately used depending on the functional groups of the polymer and the photosensitizer, and both the polymer and the photo- , A disulfide linker such as a compound represented by the following general formula (1) may be used. In this case, the carboxylic acid of the polymer forms a covalent bond with one amine group of the compound represented by the following formula (1) and an amide bond, and the carboxylic acid of the photosensitizer forms an amide bond with the other amine- Thereby providing a photosensitizer combination.
[화학식 1][Chemical Formula 1]
상기 식에서, n1및 n2는 각각 독립적으로 1 내지 5의 정수이고, 바람직하게 n1 및 n2는 각각 2이다.
In the above formula, n1 And n2 are each independently an integer of 1 to 5, preferably n1 and n2 are each 2.
본 발명에서 사용되는 용어 '광감각제'는, 특정 파장의 빛에 조사되었을 때 여기(excitation)된 후, 형광 신호를 생성하거나, 주변의 기질 또는 산소와 반응하여 반응성 산소종(reactive oxygen species)을 생성하고, 생성된 반응성 산소종은 주변 종양 세포를 자멸 또는 괴사시키는 효과가 있다. 본 발명의 광감각제는 유리염기(free base) 또는 금속 착물(metal complex) 형태의 포르피린계 화합물 또는 비포르피린계 화합물일 수 있으며, 로다민 유도체, 알렉사 유도체, BODIPY 유도체 또는 시아닌 유도체일 수 있다. 바람직하게는, 상기 광감각제는 클로린 e6 (chlorin e6)이다.
As used herein, the term " photo-sensitizer " refers to a substance that excites when irradiated with light of a specific wavelength, generates a fluorescent signal, reacts with surrounding substrate or oxygen to form reactive oxygen species, And the generated reactive oxygen species has the effect of self-destroying or necrosising peripheral tumor cells. The photosensitizer of the present invention may be a porphyrin compound or a non-porphyrin compound in the form of a free base or a metal complex, and may be a rhodamine derivative, an Alexa derivative, a BODIPY derivative or a cyanine derivative. Preferably, the photosensitizer is chlorin e6.
또한, 상기 광감각제는 600 nm 내지 900 nm의 근적외선 파장 영역에서 형광신호를 내는 것이 바람직하다. 고분자에 결합 후, 광감각제 사이의 거리가 가까워지는 경우에는 상호간 에너지 전달현상에 의해서 형광신호 및/또는 반응성 산소 생성이 억제된다.
In addition, the photosensitizer preferably emits a fluorescence signal in a near-infrared wavelength range of 600 nm to 900 nm. When the distance between the photosensitizers is close to that after binding to the polymer, the fluorescence signal and / or reactive oxygen production is inhibited by mutual energy transfer phenomena.
본 발명에서 사용되는 광감각제는 하기에 기재된 광감각제 중의 하나일 수 있다. 하기 기재된 광감각제는 본 발명의 이해를 돕기 위한 것이며 이에 한정되는 것은 아니다.
The photosensitizer used in the present invention may be one of the photosensitizers described below. The photosensitizer described below is for the purpose of helping understanding of the present invention, but is not limited thereto.
현재 PDT (광역동) 요법에 사용되고 있는 광민감성 물질로는 유리 염기(free base) 또는 금속 착물(metal complex) 형태의 포르피린 기반(porphyrin-based) 화합물과 비포르피린(nonporphyrin)계 화합물로 크게 분류될 수 있다 (A.E. O'Connor, W.M. Gallagher, A.T. Byrne, Photochem. Photobiol. (2009) 85(5), 1053-1074; R.R. Allison, V.S. Bagnato, C.H. Sibata. Future Oncol. 2010 6(6), 929-940).The photosensitizers currently used in PDT therapy are broadly classified into porphyrin-based and nonporphyrin-based compounds in the form of free bases or metal complexes RB Allison, VS Bagnato, CH Sibata, Future Oncol. 2010, 6 (6), 929-7. [CrossRef], [ 940).
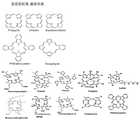
상기 광민감성 물질 화합물은 포르피린 유도체들(porphyrin derivatives); 포르피린을 구성하는 적어도 하나의 피롤(pyrrole)이 피롤린(pyrroline)으로 환원된 환원 포르피린계(reduced porphyrins); 클로린(chlorin); 박테리오클로린(bacteriochlorin); 또는 프탈로시아닌(phthalocyanine), 나프탈로시아닌 (naphthalocyanine)과 같은 포르피린 유사체들(porphyrin analogues)등이 있다. 도 12에 포르피린계 화합물의 중심 골격 구조를 나타내었으며, 필요에 따라서 여러 가지 합성 방법에 의해서 곁가지 구조에 카르복실산 등의 관능기를 도입할 수 있다.
The photosensitive compound may be selected from the group consisting of porphyrin derivatives; Reduced porphyrins in which at least one pyrrole constituting porphyrin is reduced to pyrroline; Chlorin; Bacteriochlorin; Or porphyrin analogues such as phthalocyanine, naphthalocyanine and the like. FIG. 12 shows the central skeleton structure of the porphyrin compound. If necessary, functional groups such as carboxylic acid can be introduced into the side chain structure by various synthesis methods.
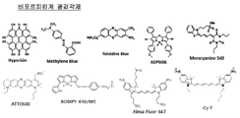
또한, 도 13에 비포르피린계 화합물을 나타내었으며, 비포르피린계 화합물은 하이페리신(hypericin), 로다민(rhodamine), 로즈벵갈(rose Bengal), 프소랄렌(psoralen), 페노씨아지늄(phenothiazinium) 계열 염료 또는 메로시아닌(merocyanine) 등 이다.
13 shows a non-porphyrin compound. The non-porphyrin compound includes hypericin, rhodamine, rose bengal, psoralen, phenothiazinium, ) Series dyes or merocyanine.
형광영상 목적으로 주로 사용되는 광감각제의 예로서는, Molecular Probe 사로부터 얻을 수 있는 보디피(BODIPY) 계열의 형광 염료들: 예를들어 BODIPY FL; BODIPY TMR STP 에스테르; BODIPY TR-X STP 에스테르; BODIPY 630/650-X STP 에스테르;및 BODIPY 650/665-X STP 에스테르 등이며, Molecular Probes 사로부터 얻을 수 있는 알렉사(Alexa) 계열의 형광염료들: 예를들어 Alexa Fluor 350 카르복시산; Alexa Fluor 430 카르복시산; Alexa Fluor 488 카르복시산; Alexa Fluor 532 카르복시산; Alexa Fluor 546 카르복시산; Alexa Fluor 555 카르복시산; Alexa Fluor 568 카르복시산; Alexa Fluor 594 카르복시산; Alexa Fluor 633 카르복시산; Alexa Fluor 647 카르복시산; Alexa Fluor 660 카르복시산;및 Alexa Fluor 680 카르복시산 등 이다.Examples of photosensitizers which are mainly used for fluorescence imaging include fluorescent dyes of the BODIPY series obtained from Molecular Probe Co., for example BODIPY FL; BODIPY TMR STP ester; BODIPY TR-X STP ester; BODIPY 630/650-X STP ester, and BODIPY 650/665-X STP ester; Alexa Fluorescent dyes available from Molecular Probes; for example Alexa Fluor 350 carboxylic acid; Alexa Fluor 430 carboxylic acid; Alexa Fluor 488 carboxylic acid; Alexa Fluor 532 carboxylic acid; Alexa Fluor 546 carboxylic acid; Alexa Fluor 555 carboxylic acid; Alexa Fluor 568 carboxylic acid; Alexa Fluor 594 carboxylic acid; Alexa Fluor 633 carboxylic acid; Alexa Fluor 647 carboxylic acid; Alexa Fluor 660 Carboxylic Acid, and Alexa Fluor 680 Carboxylic Acid.
또한, Amersham-Pharmacia Biotech로부터 얻을 수 있는 형광 염료의 예는 Cy3 NHS 에스테르; Cy 5 NHS 에스테르; Cy5.5 NHS 에스테르;및 Cy 7 NHS 에스테르 등 이며, VisEn Medical, Inc, (Woburn, MA)로부터 얻을 수 있는 형광 염료의 예는 VivoTag 680 및 VivoTag 750 등이다.Also examples of fluorescent dyes obtainable from Amersham-Pharmacia Biotech include Cy3 NHS esters;
또한, ATTO-TEC로부터 얻을 수 있는 형광 염료의 예는 ATTO 655, ATTO 665, ATTO 647N, ATTO 680, ATTO 700, ATTO 725 및 ATTO MB2 등이다.
Examples of fluorescent dyes obtainable from ATTO-TEC are ATTO 655, ATTO 665, ATTO 647N, ATTO 680, ATTO 700, ATTO 725 and ATTO MB2.
본 발명의 일 실시예에서 사용한 광감각제는 하기 화학식 2로 표시되는 클로린(chlorin) 기반 광감각제인 클로린 e6로서, 클로린 중심 골격구조를 화학적으로 처리하여 제조된다. 본 발명에서, 상기 클로린 e6의 카르복시기는 상기 화학식 1의 아민기와 결합한다.The photosensitizer used in one embodiment of the present invention is chlorin e6, a chlorin-based photosensitizer represented by the following formula (2), prepared by chemically treating the chlorine central skeleton structure. In the present invention, the carboxyl group of chlorin e6 is bonded to the amine group of the above formula (1).
[화학식 2](2)
본 발명에서, 광감각제는 이황화물 연결자를 통하여 고분자와 결합체를 형성하는데, 고분자-광감각제 결합체에 존재하는 광감각제의 결합비율은 결합체 전체 질량의 1 wt% 내지 60 wt% 가 바람직하다.
In the present invention, the photosensitizer forms a complex with the polymer through a disulfide linker, and the ratio of the photosensitizer present in the polymer-photosensitizer combination is preferably 1 wt% to 60 wt% of the total mass of the binder .
본 발명의 고분자-광감각제 결합체는 광감각제 자체에 비해 크기가 크기 때문에, 정맥 투여시에 비뇨계를 통하여 체외로 쉽게 배출되지는 않으면서도 종양 주변에 존재하는 느슨한 신생 혈관벽은 선택적으로 투과하여 종양 조직에 침투할 수 있으며, 종양의 림프관을 통한 배출기능의 부족으로 인해 종양에 축적되고 또한 오래 머무를 수 있다. 그 결과 종양 조직 내의 이러한 혈관특성에 기인한 EPR (enhanced retention and permeability) 효과에 의한 암의 수동 표적(passive targeting)이 가능해지고, 이로 인해서 암 조직에 선택적으로 축적된 결합체는 암세포 내로 엔도시스(endocytosis)에 의해 섭취되면서 암 세포내에서 형광 및 반응성 산소 생성 특성이 활성화 된다.
Since the polymer-photosensitizer conjugate of the present invention is larger in size than the photosensitizer itself, it is not easily discharged to the outside of the body through the urinary system at the time of intravenous administration, but the loose neovascular wall existing around the tumor selectively permeates It can penetrate into tumor tissue and accumulate in the tumor and remain in the tumor for a long time due to the lack of drainage function through the lymphatic duct of the tumor. As a result, it is possible to passively target cancer by the enhanced retention and permeability (EPR) effect due to the characteristics of blood vessels in the tumor tissue, and thus, the accumulation selectively accumulating in the cancer tissue can cause endocytosis ), The fluorescence and reactive oxygen production characteristics are activated in cancer cells.
또한, 본 발명의 이황화 결합된 고분자-광감작제 결합체는 수계에서 자기 결합에 의해서 100 nm 내지 1000 nm의 크기의 나노복합체를 형성할 수 있다. 즉, 친수성인 고분자와 소수성인 광감각제는 수계에서 나노크기의 자기조립체(self-assembly) 또는 자기집합체(self-aggregate)를 형성할 수 있다. 구형의 나노복합체를 형성하게 되면 이때에는 광감각제 간의 에너지 전달현상에 의해서 형광신호 및 반응성 산소 생성이 현저히 억제되게 된다. 이황화 결합된 고분자-광감작제 결합체가 혈액 내에서 순환하는 동안에는 나노복합체를 유지할 수 있어, 형광 및 반응성 산소가 발생되지 않으므로 광역학 치료시 발생하는 광민감성 부작용이 억제될 수 있다. 나노복합체 이황화 결합된 생체 적합성 고분자-광감작제 결합체는 암 조직에 대한 선택성 및 축적률이 높으며, 암 조직 주변의 느슨한 신생혈관의 높은 투과성으로 인하여 나타나는 EPR(enhanced permeability and retention) 효과에 의해서 암 조직에 선택적으로 축적이 된다. 이황화 결합된 생체 적합성 고분자-광감작제 결합체가 암세포 내에 있는 리소좀 내에 존재하는 글루타티온(glutathione)과 같은 환원제를 만나게 되는 때에는 광감작제와 생체 고분자를 연결하는 이황화결합이 분해되게 되고, 광감작제 간의 에너지전달 현상이 없어지면서 특정 파장의 레이저에 의해 형광 및 반응성 산소 생성이 활성화 된다.
In addition, the disulfide-bonded polymer-photosensitizer conjugate of the present invention can form a nanocomposite having a size of 100 nm to 1000 nm by magnetic coupling in a water system. In other words, hydrophilic polymers and hydrophobic photosensitizers can form nano-sized self-assemblies or self-aggregates in the aqueous system. When a spherical nanocomposite is formed, the fluorescence signal and reactive oxygen production are significantly suppressed by energy transfer between the photosensitizer. While the disulfide-bonded polymer-light sensitizer conjugate circulates in the blood, the nanocomposite can be maintained, and fluorescence and reactive oxygen are not generated, so that the photosensitivity side effect that occurs in photodynamic therapy can be suppressed. The nanocomposite disulfide bonded biocompatible polymer-photosensitizer conjugate has a high selectivity to and accumulation rate in cancer tissues, and is characterized by an enhanced permeability and retention (EPR) effect due to the high permeability of loose neovasculature around cancer tissue, . ≪ / RTI > When the disulfide-bonded biocompatible polymer-photosensitizer conjugate meets a reducing agent such as glutathione present in the lysosomes in the cancer cells, the disulfide bond connecting the photosensitizer and the biopolymer is decomposed, As the energy transfer phenomenon disappears, fluorescence and reactive oxygen generation are activated by a laser of a specific wavelength.
또한, 상기 고분자-광감각제 결합체에 표적형 리간드를 추가로 결합할 수 있으며, 상기 표적형 리간드는 친수성을 향상시킴과 동시에 암세포에 대한 적극적 표적(active targeting)을 가능하게 하는 특정 항체, 리보헥산(RNA) 또는 디옥시리보헥산(DNA) 압타머(aptamer), 펩타이드 리간드, 또는 엽산(folic acid)일 수 있다 (A.M. Bugaj. Photochem. Photobiol. Sci. (2011) 10, 1097-1109; A. J. Bullous, C.M. Alonso, R.W. Boyle. Photochem Photobiol Sci. (2011) 10(5), 721-50; Y. Wang, Z. Li, D. Hu, C.T. Lin, , J. Li, Y. Lin, J Am Chem Soc. (2010) 132(27), 9274-9276.).
In addition, a target ligand may be further bound to the polymer-photosensitizer conjugate, and the target ligand may be a specific antibody that enhances hydrophilicity and enables active targeting of cancer cells, ribohexane (RNA) or deoxyribohexane (DNA) aptamer, peptide ligand, or folic acid (AM Bugaj. Photochem. Photobiol. Sci (2011) 10, 1097-1109; AJ Bullous, CM Alonso, RW Boyle, Photochem Photobiol Sci. (2011) 10 (5), 721-50; Y. Wang, Z. Li, D. Hu, CT Lin, J. Li, Y. Lin, J Am Chem Soc. (2010) 132 (27), 9274-9276).
또한, 본 발명은 상기 고분자-광감각제 결합체를 포함하는, 암의 진단 또는 치료용 조성물을 제공한다.
The present invention also provides a composition for diagnosing or treating cancer, which comprises the above polymer-photosensitizer conjugate.
이때, 상기 결합체는 혈액순환시 또는 정상조직에서는 고분자에 결합된 광감각제들 사이에서 일어나는 에너지 전달현상에 의해서 형광 신호 및 세포 광독성을 나타내지 않는다. 상기 결합체가 암조직 또는 암세포에서 표적 및 축적되면 세포내 존재하는 글루타티온(glutathione)과 같은 환원제에 의해 이황화결합이 절단되어 고분자와 광감각제가 분리되며, 이때는 광감각제간의 에너지 전달현상이 없어지기 때문에, 빛에 노출된 광감각제는 강한 형광 신호를 나타내고 또한 반응성 산소종을 생성하면서 세포 독성을 나타낸다. 즉, 암세포 밖에서는 고분자에 결합된 광감각제의 형광 및 반응성 산소 생성이 억제되고, 결합체가 암세포 내로 들어갔을 때에만 형광 및 반응성 산소의 생성이 활성화되어 암 선택적 형광 영상 및 광역학 치료가 가능해진다. 따라서 종양조직에서 선택적으로 활성화되는 반응성 산소 생성 특성으로 인하여 광역학 치료시 발생하는 피부 광민감성 부작용은 예방하면서도 종양의 광역학 치료 효과는 최대한으로 증대시킬 수 있다.
At this time, the conjugate does not exhibit fluorescence signal and cell phototoxicity due to the energy transfer phenomenon occurring between the photosensitizers bound to the polymer during blood circulation or normal tissues. When the conjugate is targeted and accumulated in cancer tissues or cancer cells, the disulfide bond is cleaved by a reducing agent such as glutathione present in the cell to separate the polymer and the photosensitizer. In this case, energy transfer phenomenon between the photosensitizer is eliminated , The photosensitizer exposed to light exhibits strong fluorescence signals and also exhibits cytotoxicity while producing reactive oxygen species. That is, fluorescence and reactive oxygen production of the photosensitizer bound to the polymer are inhibited outside the cancer cell, and fluorescence and reactive oxygen generation are activated only when the conjugate enters the cancer cell, thereby enabling cancer selective fluorescence imaging and photodynamic therapy . Therefore, due to the selective activation of reactive oxygen species in tumor tissues, it is possible to maximize the effect of photodynamic therapy of tumors while preventing skin photosensitivity side effects that occur in photodynamic therapy.
상기 암의 진단 및 치료용 조성물은 약제학적으로 유효량의 고분자-광감각제 결합체와, 약제학적으로 허용 가능한 담체를 포함한다. 상기 담체는 희석제일 수 있다. 상기 조성물은 보존제, 습윤제, 유화제, 및 분산제 등의 보조제를 추가로 포함할 수 있다.
The composition for the diagnosis and treatment of cancer includes a pharmaceutically effective amount of a polymer-photosensitizer conjugate and a pharmaceutically acceptable carrier. The carrier may be a diluent. The composition may further comprise adjuvants such as preservatives, wetting agents, emulsifying agents, and dispersing agents.
이러한 약제학적 조성물은 의도된 투여 경로와 조화되도록 제형화될 수 있다. 투여 경로의 예는, 비경구, 예를 들어 정맥내, 피부내, 피하, 비내, 경피(국소), 점막관통, 및 직장 투여를 포함하나, 이들에 한정되는 것은 아니다.
Such pharmaceutical compositions may be formulated to be compatible with the intended route of administration. Examples of routes of administration include, but are not limited to, parenteral, for example, intravenous, intradermal, subcutaneous, intranasal, transdermal (topical), mucosal penetration, and rectal administration.
비경구 투여를 위해 사용될 수 있는 적절한 담체는 당업자에게 널리 공지되어 있다. 예를 들어, 염화나트륨 주사액, 링거 주사액, 덱스트로오스 주사액, 덱스트로오스 및 염화나트륨 주사액, 및 락테이트 함유 링거 주사액를 포함하나 이들에 한정되지 않는 수성 운반체(vehicle); 에틸 알코올, 폴리에틸렌 글리콜, 및 폴리프로필렌 글리콜을 포함하나 이들에 한정되지 않는 수-혼화성 운반체; 및 옥수수 유, 면실 유, 땅콩 유, 참깨 유, 에틸 올레이트, 이소프로필 미리스테이트, 및 벤질 벤조에이트를 포함하나 이들에 한정되지 않는 비-수성 운반체일 수 있다.
Suitable carriers that can be used for parenteral administration are well known to those skilled in the art. An aqueous vehicle including, but not limited to, sodium chloride injection, Ringer's injection, dextrose injection, dextrose and sodium chloride injection, and lactate-containing Ringer's injection; Water-miscible carriers including but not limited to ethyl alcohol, polyethylene glycol, and polypropylene glycol; And non-aqueous carriers including, but not limited to, corn oil, cottonseed oil, peanut oil, sesame oil, ethyl oleate, isopropyl myristate, and benzyl benzoate.
이러한 약제학적 조성물은 종양 치료 또는 종양 진단을 위해 사용될 수 있다. 종양 치료 또는 종양 진단을 위해 사용되는 경우에, 유효량은 케이스 별로 의사에 의해 결정될 수 있다. 이 때, 환자의 나이, 성별, 체중, 또는 치료 또는 진단되어야 할 병태의 중증도가 고려될 수 있다. 일예로서, 고분자-광감각제 결합체는 광감각제의 당량 및 환자 체중을 기준으로 0.001 ㎍/㎏ 내지 10 ㎎/㎏으로 투여될 수 있다. 특정 예에서 상기 결합체는 광감각제를 기준으로 0.1 ㎎/㎏ 내지 2 ㎎/㎏으로 투여될 수 있다.
Such pharmaceutical compositions may be used for tumor therapy or tumor diagnosis. When used for tumor therapy or tumor diagnosis, the effective amount can be determined by a physician on a case-by-case basis. At this time, the severity of the patient's age, sex, weight, or condition to be treated or diagnosed can be considered. As an example, the polymer-photosensitizer conjugate can be administered at 0.001 [mu] g / kg to 10 mg / kg, based on the equivalent of the photosensitizer and the patient's body weight. In certain instances, the conjugate may be administered at a dose of 0.1 mg / kg to 2 mg / kg, based on the photosensitizer.
본 발명에서, 상기 암은 소화기, 비뇨기, 생식기, 호흡기, 순환기, 뇌 및 신경계의 암으로 이루어진 군에서 선택될 수 있다.
In the present invention, the cancer may be selected from the group consisting of digestive, urinary, reproductive, respiratory, circulatory, brain and nervous system cancers.
보다 구체적으로, 상기 암은 폐암, 비소세포성 폐암, 결장암, 골암, 췌장암, 피부암, 두부 또는 경부 암, 자궁암, 난소암, 직장암, 위암, 항문부근암, 결장암, 유방암, 나팔관암종, 자궁내막암종, 자궁경부암종, 질암종, 음문암종, 호지킨병(Hodgkin's disease), 식도암, 소장암, 내분비선암, 갑상선암, 부갑상선암, 부신암, 연조직 육종, 요도암, 음경암, 전립선암, 만성 또는 급성 백혈병, 림프구 림프종, 방광암, 신장 또는 수뇨관암, 신장세포암종, 신장골반 암종, 중추신경계(central nervous system, CNS) 종양, 1차 중추신경계 림프종, 척수 종양, 뇌간 신경교종 및 뇌하수체 선종으로 이루어진 군으로부터 선택될 수 있으나, 이에 한정되는 것은 아니다.
More particularly, the cancer is selected from the group consisting of lung cancer, non-small cell lung cancer, colon cancer, bone cancer, pancreatic cancer, skin cancer, head or neck cancer, uterine cancer, ovarian cancer, rectal cancer, gastric cancer, colon cancer, breast cancer, fallopian tube carcinoma, endometrial carcinoma , Cancer of the uterine cervix, vaginal cancer, vulvar carcinoma, Hodgkin's disease, esophageal cancer, small bowel cancer, endocrine cancer, thyroid cancer, parathyroid cancer, adrenal cancer, soft tissue sarcoma, urethral cancer, penile cancer, prostate cancer, chronic or acute From the group consisting of leukemia, lymphocytic lymphoma, bladder cancer, renal or ureteral cancer, renal cell carcinoma, renal pelvic carcinoma, central nervous system (CNS) tumor, primary central nervous system lymphoma, spinal cord tumor, brainstem glioma and pituitary adenoma But is not limited thereto.
또한, 본 발명의 고분자-광감각제 결합체를 포함하는 암 진단 및 치료용 조성물은 정맥주사, 복강내주사, 근육내주사, 두개내주사, 종양내주사, 상피내주사, 피부관통전달, 식도투여, 복부투여, 동맥주사, 관절내주사 및 구강내투여로 이루어진 군으로부터 선택된 경로로 투여될 수 있다.
In addition, the composition for diagnosing and treating cancer comprising the polymer-photosensitizer conjugate of the present invention may be administered by intravenous injection, intraperitoneal injection, intramuscular injection, intracranial injection, intratumoral injection, intraperitoneal injection, Intraperitoneal administration, intraarterial injection, intraarticular injection and intraoral administration.
본 발명의 이황화 연결자로 결합된 고분자-광감각제 결합체는, 표적으로 하는 암 세포 내에서만 선택적으로 형광 및 반응성 산소 생성이 활성화되어 광역학 치료의 부작용을 감소시키고, 암 선택적 형광 영상 및 광역학 치료가 가능한 장점을 가진다.
The polymer-photosensitizer conjugate conjugated with a disulfide linker of the present invention selectively activates fluorescence and reactive oxygen species selectively only in a target cancer cell, thereby reducing adverse effects of photodynamic therapy, and selectively activating cancer selective fluorescence imaging and photodynamic therapy .
도 1은, 고분자-광감각제 결합체의 구성을 보여주는 모식도이다. 결합체는 고분자, 광감각제, 이황화물 결합(disulfide bond, -SS-)을 함유하는 연결자, 그리고 표적화 리간드(targeting ligand)로 구성된다.
도 2A는 고분자-광감각제 결합체가 세포내에 들어갔을 때에만 형광 신호 및 반응성 산소 생성이 활성화 되는 특성 개념을 모식적으로 나타낸 것이다.
도 2B는 고분자-광감각제 결합체가 빛에 의해 노출이 되더라도 인접한 광감각제간의 에너지 전달(RET)현상으로 인해서 형광 및 반응성 산소가 생성 되지 않음을 보여주는 모식도이다.
도 2C는 고분자-광감각제 결합체가 표적으로 하는 세포내에 존재하는 환원제 의해서 이황화물 결합이 분해되어 광감각제간의 거리가 멀어질 때, 강한 형광 신호가 발생하고 반응성 산소 생성도 활성화 되는 모식도이다.
도 3은 본 발명의 일 실시예에 따른 히알루론산-Ce6(HA-Ce6) 결합체의 합성과정을 나타낸 것이다.
도 4는 본 발명의 일 실시예에 따른 히알루론산-Ce6(HA-Ce6) 결합체의 1H-NMR 분석 결과를 나타낸 것이다.
도 5는, 히알루론산-Ce6(HA-Ce6) 결합체를 이용하여 만들어진 나노입자 (HA-Ce6 NP)의 주사전자현미경(SEM) 사진(A) 및 수용액상 크기분포를 나타낸 그래프(B)이다.
도 6은, Ce6 및 HA-Ce6 NP가 분산된 수용액의 UV/Vis 흡광 스펙트럼(A), 및 380 nm 빛 조사 시 형광 발생(B)을 비교한 것이다.
도 7은, 일항산소 검출 시약인 SOSG를 사용하여, Ce6 및 HA-Ce6 NP가 분산된 수용액에 빛 조사(light irradiation)시 시간에 따른 일항산소 생성정도를 비교한 것이다.
도 8은, DDT 농도 및 처리 시간에 따른 HA-Ce6 NP의 형광강도의 변화(A), 및 여러 DDT 농도로 HA-Ce6 NP를 5시간 동안 처리해준 후에 측정한 일항산소 생성의 상대적 양을 비교한 그래프(B)이다.
도 9A는, 암세포에 Ce6 (흑색막대) 및 HA-Ce6 NP(백색막대)를 여러 Ce6 농도로 24시간동안 처리해 준 후, 세포 생존율을 측정한 그래프이다.
도 9B는, 암세포에 Ce6 및 HA-Ce6 NP를 여러 Ce6 농도로 24시간동안 처리해 준 후, 670 nm 레이저를 이용하여 빛을 조사하고 세포 생존율을 측정한 결과이다.
도 10은, 암세포에 Ce6 및 HA-Ce6 NP를 2 μM Ce6 당량으로 18시간동안 처리해준 후 FACS 데이터를 분석한 그래프이다.
도 11은, Ce6 (A) 및 HA-Ce6 NP(B)를 같은 조건으로 처리한 후, Lysotracker로 형광염색을 추가로한 U-87MG 세포의 공초점 형광 현미경 이미지이다. 그림에서 보여지는 공초점 현미경 형광이미지들 중, 왼쪽은 U-87MG 세포에 처리한 Lysotracker에 의한 형광(초록색 부분) 이미지이고, 중간은 Ce6에서 발생한 형광(붉은색 부분) 이미지이며, 오른쪽은 Lysotracker와 Ce6의 두 형광이미지를 융합시킨 사진이다. 노란색 부분은 Lysotracker의 형광과 Ce6의 형광이 일치하는 부분이다.
도 12는, 광감각제로서 사용되는 포르피린계 화합물의 중심 골격 구조를 나타낸 것이다.
도 13은, 광감각제로서 사용되는 비포르피린계 화합물을 나타낸 것이다.BRIEF DESCRIPTION OF THE DRAWINGS FIG. 1 is a schematic diagram showing the structure of a polymer-photo-sensitizer combination; FIG. The conjugate consists of a polymer, a photosensitizer, a linker containing a disulfide bond (-SS-), and a targeting ligand.
2A schematically shows a characteristic concept of activating fluorescence signal and reactive oxygen generation only when a polymer-photosensitizer conjugate enters a cell.
FIG. 2B is a schematic diagram showing that fluorescence and reactive oxygen are not generated due to energy transfer (RET) between adjacent photosensitizers even though the polymer-photosensitizer conjugate is exposed to light.
FIG. 2C is a schematic diagram in which strong fluorescence signals are generated and reactive oxygen generation is activated when disulfide bonds are decomposed by a reducing agent present in a cell targeted by a polymer-photosensitizer conjugate and the distance between the photosensitizers is distant.
FIG. 3 illustrates a process of synthesizing a hyaluronic acid-Ce6 (HA-Ce6) conjugate according to an embodiment of the present invention.
FIG. 4 shows the 1 H-NMR analysis results of the hyaluronic acid-Ce (HA-Ce 6) conjugate according to an embodiment of the present invention.
5 is a scanning electron microscope (SEM) photograph (A) of a nanoparticle (HA-Ce6 NP) made using a hyaluronic acid-Ce6 (HA-Ce6) conjugate and a graph (B) showing an aqueous solution size distribution.
6 compares the UV / Vis absorption spectrum (A) of an aqueous solution containing Ce6 and HA-Ce6 NP dispersed therein and the fluorescence emission (B) upon irradiation at 380 nm.
FIG. 7 is a graph comparing the degree of anoxic oxygen production with time when light irradiation is performed on an aqueous solution containing Ce6 and HA-Ce6 NP dispersed using SOSG as a detection reagent for oxygen.
Figure 8 shows the change in fluorescence intensity (A) of HA-Ce6 NP with DDT concentration and treatment time, and the relative amount of unilamellar oxygen production measured after treatment of HA-Ce6 NP with various DDT concentrations for 5 hours One graph (B).
FIG. 9A is a graph showing the cell survival rate after treating Ce6 (black rod) and HA-Ce6 NP (white rod) with various Ce6 concentrations for 24 hours in cancer cells. FIG.
FIG. 9B shows the result of irradiation of Ce6 and HA-Ce6 NP with various Ce6 concentrations for 24 hours to cancer cells, irradiation with light using a 670 nm laser, and cell viability.
FIG. 10 is a graph showing FACS data analysis after treatment of Ce6 and HA-Ce6 NP with cancer cells for 2 hours at 2 μM Ce6 equivalent.
11 is a confocal fluorescence microscope image of U-87MG cells treated with Ce6 (A) and HA-Ce6 NP (B) under the same conditions, followed by fluorescence staining with Lysotracker. Among the confocal microscope fluorescence images shown in the figure, the left image is fluorescence (green part) image by Lysotracker treated on U-87MG cells, the middle image is fluorescence (red part) image generated on Ce6 and the right image is Lysotracker This is a photograph of two fluorescence images of Ce6. The yellow part corresponds to the fluorescence of Lysotracker and the fluorescence of Ce6.
12 shows the central skeleton structure of a porphyrin compound used as a photosensitizer.
Fig. 13 shows a non-porphyrin compound used as a photosensitizer.
이하, 본 발명을 보다 구체적으로 설명하기 위하여 본 발명에 따른 바람직한 실시예를 첨부된 도면을 참조하여 보다 상세하게 설명한다. 그러나, 본 발명은 여기서 설명되어지는 실시예에 한정되지 않고 다른 형태로 구체화될 수도 있다.
Hereinafter, preferred embodiments of the present invention will be described in detail with reference to the accompanying drawings. However, the present invention is not limited to the embodiments described herein but may be embodied in other forms.
실시예Example 1: 고분자- 1: polymer-광감각제Photo sensation agent 결합체의 합성 및 나노입자의 제조 Synthesis of conjugates and preparation of nanoparticles
히알루론산(HA, MW 66,300 Da)은 Lifecore Biomedical(MN, USA)로부터 구입하였으며, 1-에틸-3(3-디메틸아미노프로필)카보디이미드(EDC), N-히드록시설포석신이미드(sulfo-NHS) 및 시스타민 다이하이드로클로라이드(cystamine dihydrochloride)는 Sigma-Aldrich(MO, USA)로부터 구입하여 사용하였다. Chlorin e6(Ce6) 및 투석막(MW cut-off: 50,000 Da)는 Frontier Scientific(UT, USA) 및 Spectrum Laboratories(CA, USA)로부터 각각 구입하였다.Hyaluronic acid (HA, MW 66,300 Da) was purchased from Lifecore Biomedical (MN, USA) and was mixed with 1-ethyl-3 (3-dimethylaminopropyl) carbodiimide (EDC), N-hydroxy pseudoside -NHS) and cystamine dihydrochloride were purchased from Sigma-Aldrich (MO, USA). Chlorin e6 (Ce6) and dialysis membrane (MW cut-off: 50,000 Da) were purchased from Frontier Scientific (UT, USA) and Spectrum Laboratories (CA, USA).
아민 기능기화된 생체 고분자 히알루론산과 광감각제인 Chlorin e6를 결합시키기 위하여, 먼저 이황화결합(disulfide bond) 함유 연결자를 이용한 아미노화 히알루론산을 제조하였다. 200 ㎎ 히알루론산을 인산완충액(pH 7.4, 10 mM, 10 ㎖)에 용해시킨 후, 카르복실기 활성화제인 1-에틸-3(3-디메틸아미노프로필)카보디이미드(EDC, 240 mM, 0.5 ㎖) 및 N-히드록시설포석신이미드(sulfo-NHS, 250 mM, 0.5 ㎖)를 순차적으로 첨가하였다. 30분 동안 반응시킨 후, 시스타민(27 mg)이 용해된 인산완충액(1 ㎖)을 첨가하였다. 상온에서 밤새(overnight) 반응시킨 후, 반응물은 증류수로 투석하고 동결건조하여 이황화결합 연결자 함유 아미노화 히알루론산을 얻었다. 수득한 아미노화 히알루론산과 Chlorin e6(Ce6)의 결합체를 제조하기 위하여, 먼저 디메틸설폭사이드(DMSO) 용매 10 ㎖에 녹인 카르복실기 활성화제인 1-에틸-3-(3-디메틸아미노프로필)카보디이미드(EDC, 34 mM) 및 N-히드록시설포석신이미드(sulfo-NHS, 35 mM)를 Chlorin e6(Ce6, 20 ㎎)에 순차적으로 첨가하고 반응시켜 활성화된 NHS-Chlorin e6 용액을 제조하였다. 디메틸폼아마이드(DMF):물을 부피비로 1:1 혼합한 혼합용매 5 ㎖에 상기 아미노화 히알루론산(50 mg)을 녹이고, 상기 활성화된 NHS-Chlorin e6 용액을 혼합한 후 상온에서 18시간 동안 반응시켜 생체 고분자-광감각제 결합체인 히알루론산-Ce6(HA-Ce6) 결합체 용액을 합성하였다. 상기 히알루론산-Ce6(HA-Ce6) 결합체 용액은 하루 동안 인산완충액 및 증류수로 각각 투석하여 정제하고, 동결건조하여 도 3에 보여지는 히알루론산-Ce6(HA-Ce6) 결합체를 얻었다. 상기 결합체의 증류수 투석을 통하여 나노입자가 얻어졌다.
Aminated hyaluronic acid was prepared by using a disulfide bond - containing linker in order to bind aminofunctional biopolymer hyaluronic acid with Chlorin e6 which is a photosensitizer. 200 mg of hyaluronic acid was dissolved in phosphate buffer (pH 7.4, 10 mM, 10 ml), and then 1-ethyl-3- (3-dimethylaminopropyl) carbodiimide (EDC, 240 mM, 0.5 ml) N-hydroxysuccinimide (sulfo-NHS, 250 mM, 0.5 mL) was added sequentially. After reaction for 30 minutes, phosphoric acid buffer (1 ml) in which cystamine (27 mg) was dissolved was added. After overnight reaction at room temperature, the reaction product was dialyzed with distilled water and lyophilized to obtain aminated hyaluronic acid containing disulfide bond. Ethyl-3- (3-dimethylaminopropyl) carbodiimide, which is a carboxyl group activating agent, dissolved in 10 ml of dimethylsulfoxide (DMSO) solvent, was added to prepare the conjugate of the obtained aminated hyaluronic acid and Chlorin e6 (EDC, 34 mM) and N-hydroxysuccinimide (sulfo-NHS, 35 mM) were sequentially added to Chlorin e6 (Ce6, 20 mg) and reacted to prepare an activated NHS-Chlorin e6 solution. Dimethylformamide (DMF): The aminated hyaluronic acid (50 mg) was dissolved in 5 ml of a 1: 1 mixture of water and water, the activated NHS-Chlorin e6 solution was mixed, and the mixture was stirred at room temperature for 18 hours To prepare a hyaluronic acid-Ce6 (HA-Ce6) conjugate solution as a biopolymer-photosensitizer conjugate. The hyaluronic acid-Ce6 (HA-Ce6) conjugate solution was dialyzed with phosphate buffer and distilled water for one day, purified and lyophilized to obtain a hyaluronic acid-Ce6 (HA-Ce6) conjugate shown in FIG. Nano particles were obtained through dialysis of distilled water of the conjugate.
실시예Example 2: 고분자- 2: polymer-광감각제Photo sensation agent 결합체의 결합비율 분석 Analysis of binding ratio of conjugates
상기 실시예 1에서 제조된 생체 고분자-광감각제 결합체인 히알루론산-Ce6(HA-Ce6) 결합체가 형성되었는지 확인하기 위하여, 핵자기 공명 분석 (1H-NMR)을 실시 하였으며, 그 결과를 도 4에 나타내었다. 얻어진 핵자기 공명 결과의 분석에 의하면, 히알루론산-Ce6(HA-Ce6) 결합체가 성공적으로 형성되었으며, 히알루론산 내의 2개의 글루코스 링(2 glucose rings)마다 0.27개의 Ce6가 결합된 것으로 계산 되었다.
Nuclear magnetic resonance (1H-NMR) analysis was carried out to confirm whether the hyaluronic acid-Ce6 (HA-Ce6) conjugate, which is a biopolymer-photosensitizer conjugate prepared in Example 1, was formed. Respectively. Analysis of the resulting nuclear magnetic resonance results showed that hyaluronic acid-Ce6 (HA-Ce6) conjugate was successfully formed and 0.27 Ce6 bound to each of the two glucose rings in hyaluronic acid was calculated.
실험예Experimental Example 1: 고분자- 1: polymer-광감각제Photo sensation agent 나노입자( Nanoparticles (HAHA--Ce6Ce6NPNP)의 형태 및 크기 분석Analysis of shape and size
상기 실시예 1에서 합성된 히알루론산-Ce6(HA-Ce6)를 이용하여 제조된 나노입자 HA-Ce6 NP의 형태를 주사전자현미경(FE-SEM)을 이용하여 관찰하였다. 또한, 수용액에 분산된 히알루론산-Ce6 나노입자인 HA-Ce6 NP의 제타전위 및 크기(hydrodynamic size)는 제타전위/입도 분석기(Marvern Instruments Worcestershire, UK)를 이용하여 측정하였다. 상기 주사전자현미경 분석 결과 및 크기 분석 결과를 도 5에 나타내었다.The morphology of the nanoparticles HA-Ce6 NP prepared using the hyaluronic acid-Ce6 (HA-Ce6) synthesized in Example 1 was observed using a scanning electron microscope (FE-SEM). In addition, zeta potential and size (hydrodynamic size) of hyaluronic acid-Ce6 nanoparticles HA-Ce6 NP dispersed in an aqueous solution were measured using a zeta potential / particle size analyzer (Marvern Instruments Worcestershire, UK). The SEM and analysis results are shown in FIG.
도 5A는 히알루론산-Ce6 나노입자(HA-Ce6 NP)의 주사전자현미경(SEM) 이미지를 나타낸 것이며, 도 5B는 히알루론산-Ce6 나노입자(HA-Ce6 NP)의 수용액상 크기(hydrodynamic size)를 나타낸 것이다. 나노입자의 크기(hydrodynamic size)는 245.85±51.46 nm로 나타났으며, 제타 전위는 -40.23±5.99 mV로 얻어졌다. 이것을 통하여 히알루론산-Ce6 결합체는 수용액 상에서 자가배열(self-assembly)에 의해서 나노입자를 형성함을 확인하였고, 나노입자 안쪽에는 Ce6가 위치하고 바깥쪽에는 음이온성 친수성 고분자인 히알루론산이 분포함을 알 수 있었다.
FIG. 5A shows a scanning electron microscope (SEM) image of hyaluronic acid-Ce6 nanoparticles (HA-Ce6 NP), and FIG. 5B shows the hydrodynamic size of hyaluronic acid-Ce6 nanoparticles (HA- . The hydrodynamic size of the nanoparticles was 245.85 ± 51.46 nm, and the zeta potential was -40.23 ± 5.99 mV. Through this, it was confirmed that the hyaluronic acid-Ce6 conjugate forms a nanoparticle by self-assembly in an aqueous solution, and Ce6 is located inside the nanoparticle and hyaluronic acid, which is an anionic hydrophilic polymer, I could.
실험예Experimental Example 2: 고분자- 2: polymer-광감각제Photo sensation agent 나노입자 ( Nanoparticles (HAHA--Ce6Ce6NPNP)의 형광 및) Of fluorescence and일항산소Singlet oxygen 생성 억제 현상 분석 Analysis of generation inhibition phenomena
광감각제인 Ce6와 고분자-광감각제 나노입자 (HA-Ce6 NP)를 각각 인산완충액에 분산시키고, UV/Vis 흡광 스펙트럼을 분석하였다. 도 6A의 결과에 의하면, HA-Ce6 NP의 UV/Vis 흡광 스펙트럼의 소렛밴드(soret band)는 Ce6에 비하여 매우 넓어져(broadening) 있다. 이러한 broadening현상은 광감각제인 Ce6끼리의 응집(aggregation)이 있을 때 볼 수 있는 전형적인 현상으로서, 이를 통하여 HA-Ce6 NP내의 Ce6들은 소수성 상호작용에 의해서 서로 응집된 형태로 존재함을 증명한다.The photosensitizer Ce6 and the polymer-light sensing agent nanoparticles (HA-Ce6 NP) were dispersed in phosphate buffer, respectively, and the UV / Vis absorption spectra were analyzed. 6A, the soret band of the UV / Vis absorption spectrum of HA-Ce6 NP is much broader than that of Ce6. This broadening phenomenon is a typical phenomenon observed when there is an aggregation of Ce6, which is a photosensitizer. This demonstrates that Ce6 in HA-Ce6 NP exists in a cohesive form due to hydrophobic interaction.
광감각제인 Ce6간의 거리가 10 nm 이내로 가까워지게 되면 Ce6간의 에너지 전달현상에 의해서 소광(quenching)이 일어날 수 있는데, Ce6끼리 응집이 되는 경우에는 소광현상이 매우 효과적으로 일어나게 되고, 광감각제인 Ce6는 특정 파장의 빛에 노출이 되더라도 형광신호와 반응성 산소종(특히, 일항산소)을 생성해 내지 못하게 된다.When the distance between Ce6 and Ce6 is close to 10 nm, quenching may occur due to the energy transfer between Ce6. Ce6 is very effective for quenching, and Ce6, which is a photosensitizer, Even if exposed to light of a wavelength, it is impossible to generate a fluorescent signal and reactive oxygen species (especially, oxygen).
도 6A의 UV/Vis 흡광 스펙트럼 결과로부터 예상했던 것처럼, Ce6는 붉은 색의 강한 형광을 생성해 내지만, HA-Ce NP 내의 Ce6는 형광 발생 능력이 현저히 억제되어 있음을 도 6B를 통하여 확인할 수 있다.As can be seen from the results of the UV / Vis absorption spectra shown in FIG. 6A, Ce6 produces strong red fluorescence, but Ce6 in the HA-Ce NP is significantly inhibited in fluorescence generation ability .
다음으로, 광감각제의 일항산소 생성(singlet oxygen generation, SOG) 능력 억제 특성을 평가하기 위하여, 일항산소 검출 시약인 Singlet Oxygen Sensor Green(SOSG, Molecular Probes, NY, USA)을 사용하였다. 일항산소 검출 시약을 Ce6 및 HA-Ce6 NP가 함유된 인산완충액(PBS: 6.7 mM, pH 7.4, NaCl 154 mM)에 혼합하고, 최종적으로 광감각제인 Ce6의 농도가 2μM Ce6 당량이 되도록 하였다. 일항산소 생성을 위하여, 각 샘플 용액을 670 nm 레이져(조사 선량 속도: 68 mW/cm2)로 조사하면서 일항산소 생성을 분석하였다. 도 7에 나타낸 바와 같이 HA-Ce6 NP의 일항산소 생성 능력이 Ce6에 비하여 현저히 억제되어 있음을 알 수 있다.
Next, Singlet Oxygen Sensor Green (SOSG, Molecular Probes, NY, USA) was used to evaluate the singlet oxygen generation (SOG) abilities of the photosensitizer. The combined oxygen detection reagent was mixed with phosphoric acid buffer (Ce: 6.7 mM, pH 7.4, NaCl: 154 mM) containing Ce6 and HA-Ce6 NP, and finally the concentration of Ce6 as a photosensitizer was 2 μM Ce6 equivalents. For the production of uniaxial oxygen, the production of unconfined oxygen was analyzed by irradiating each sample solution with a 670 nm laser (irradiation dose rate: 68 mW / cm 2). As shown in Fig. 7, it can be seen that the ability of HA-Ce6 NP to produce oxygen singly is significantly suppressed as compared with Ce6.
실험예Experimental Example 3: 히알루론산- 3: hyaluronic acid-Ce6Ce6 나노입자 ( Nanoparticles (HAHA--Ce6Ce6NPNP)에서 형광 및) And fluorescence일항산소Singlet oxygen 생성 회복 분석 Production recovery analysis
상기 실시예 1에서 제조된 HA-Ce6 NP의 형광 및 일항산소 생성능력이 환원제의 작용에 의하여 회복되는지를 확인하기 위하여, 환원제 반응성 회복 실험을 실시하였다. HA-Ce6 NP를 인산완충액(PBS)에 2μM Ce6 당량 농도로 분산시키고, 여러 dithiothreitol(DTT) 농도로 처리한 후, Ce6의 형광 강도가 증가되는지를 측정하였다. DTT 처리 후, 용액을 400 nm에서 여기(excitation)시키고 발광값을 측정하였다. 도 8A에 의하면, HA-Ce6 NP는 DTT의 농도 및 처리 시간에 따라서 형광이 증가되었다. 특히, 환원제인 DTT를 5 mM의 농도로 처리 후 5분 이내에 HA-Ce6 NP의 형광이 5배 증가 하였으며, 5시간 처리해 주었을 때 8배의 형광증가가 관찰되었다. 반면, HA-Ce6 NP를 5μM의 DTT로 처리해 주었을 때는, 5시간의 처리 시간동안 형광 증가가 전혀 관찰되지 않았다.In order to confirm that the fluorescence and anion-generating ability of the HA-Ce6 NP prepared in Example 1 was restored by the action of the reducing agent, a reductive reactivity restoration experiment was performed. HA-Ce6 NP was dispersed in phosphate buffer (PBS) at a concentration of 2 μM Ce6 equivalents and treated with various dithiothreitol (DTT) concentrations to determine if the fluorescence intensity of Ce6 was increased. After the DTT treatment, the solution was excited at 400 nm and the emission value was measured. According to Fig. 8A, HA-Ce6 NP showed an increase in fluorescence depending on the concentration of DTT and the treatment time. In particular, fluorescence of HA-Ce6 NP was increased 5-fold within 5 minutes after treatment with 5 mM of DTT as a reducing agent, and 8-fold increase in fluorescence was observed when treated for 5 hours. On the other hand, when HA-Ce6 NP was treated with 5 μM of DTT, no increase in fluorescence was observed during the treatment time of 5 hours.
환원제 처리 농도에 따른 일항산소 회복 능력을 분석하기 위하여 HA-Ce6 NP가 분산된 수용액을 여러 농도의 DTT로 5시간동안 처리한 후, 670 nm의 레이저 빔(조사선량 속도 68 mW/cm2)으로 조사하면서, 일항산소 검출시약의 형광증가를 측정하였다. 도 8B에 보여지는 결과에 의하면, HA-Ce6 NP의 일항산소 생성 능력은 처리해준 DTT의 농도에 비례하여 회복 되었는데, 특히 5 mM DTT를 5시간 처리한 경우에는 일항산소 생성 능력이 6.2 배 증가하였다. 반면, HA-Ce6 NP를 5μM의 DTT로 처리해 주었을 때는, 일항산소 생성 능력의 회복이 전혀 관찰되지 않았다. 이 결과로, HA-Ce6 NP는 환원제의 작용에 의해서 선택적으로 형광 및 일항산소 생성이 증가함을 확인할 수 있었다.
In order to analyze the ability of recovering oxygen according to the reducing agent concentration, HA-Ce6 NP-dispersed aqueous solution was treated with various concentrations of DTT for 5 hours and then irradiated with a laser beam at 670 nm (irradiation dose rate 68 mW / cm2 ) The fluorescence increase of the unidentified oxygen detection reagent was measured. 8B, the ability of HA-Ce6 NP to produce oxygen was recovered in proportion to the concentration of treated DTT, especially when 5 mM DTT was treated for 5 hours, the ability to produce oxygen was increased 6.2 times . On the other hand, when HA-Ce6 NP was treated with 5 μM of DTT, no recovery of oxygen production ability was observed at all. As a result, it was confirmed that HA-Ce6 NP selectively increases fluorescence and anoxic oxygen production by the action of a reducing agent.
실험예Experimental Example 4: 4:생체외In vitro광독성Phototoxicity 세포 실험 ( Cell experimentsInInvitrovitrophototoxicity광전성testtest))
상기 실시예 1에서 제조한 HA-Ce6 NP를 이용한 암의 광역학 치료 효과를 확인하기 위하여, 생체외 세포 생존능 분석을 시행하였다. 실험을 위하여 ATCC사로부터 구입한 U-87MG 인간 교아종세포(human glioblastoma cell line)를 사용하였으며, 10% 우태아 혈청(FBS) 및 1% 페니실린-스트렙토마이신이 보충된 DMEM을 세포의 배양액으로 이용하였고, 37℃, humidified 5% CO2인큐베이터에서 세포를 배양하였다. 실험을 위하여 사용된 U-87MG 세포는, 히알루론산을 분해하는 효소인 hyaluronidase을 발현하지 않는 것으로 알려져 있으며, 따라서 U-87MG 세포의 경우는 hyaluronidase에 의한 나노입자의 분해 효과를 배재할 수 있다.In order to confirm the photodynamic treatment effect of cancer using HA-Ce6 NP prepared in Example 1, the viability of an in vitro cell was analyzed. For the experiment, U-87MG human glioblastoma cell line purchased from ATCC was used, and DMEM supplemented with 10% fetal bovine serum (FBS) and 1% penicillin-streptomycin was used as a culture medium of cells At 37 ° C, humidified 5% CO2 Cells were cultured in an incubator. The U-87MG cells used for the experiments are known to not express hyaluronidase, an enzyme that degrades hyaluronic acid. Therefore, in the case of U-87MG cells, the degradation effect of hyaluronidase by nanoparticles can be eliminated.
먼저, HA-Ce6 NP의 세포 독성을 평가하기 위하여, U-87MG 세포에 Ce6 및 HA-Ce6 NP를 여러 농도로 처리하고 세포 생존율을 측정하였다. U-87MG 세포를 96-well 플레이트에 1×104cells/well 밀도로 접종하고 세포부착을 위해 24시간 동안 배양하였다. 그 후, 10% 소태아혈청(FBS)를 함유하는 DMEM 세포 배양액을 사용하여 Ce6 및 HA-Ce6 NP를 녹이고, 최종농도 1, 5, 10, 20μM Ce6 당량이 되도록 샘플을 희석하였다. 세포에 있는 기존의 세포배양액을 광감각제를 함유한 배지로 교체하고 24시간 동안 처리해주었다. 이 후, 광감각제가 함유된 세포배양액을 제거하고, 세포를 3번 세척한 후 새로운 세포배양액을 각각의 well에 첨가해 주었다. 세포 계수 키트(cell counting kit, Dojindo Labotatories)를 사용하여 세포 생존율을 측정하였다. 대조군 암세포는 광감각제가 들어있지 않은 세포배양액으로 24시간 처리하고, 세포 생존율을 측정하였다. 대조군의 세포 생준율을 100%로 하여, 각 샘플 처리군의 세포 생존율을 구하였다. 도 9A에 의하면, 빛을 조사하지 않는 경우에는, Ce6 및 HA-Ce6 NP 모두 세포 독성을 나타내지 않았다.First, in order to evaluate the cytotoxicity of HA-Ce6 NP, U-87MG cells were treated with various concentrations of Ce6 and HA-Ce6 NP, and cell viability was measured. U-87MG cells were inoculated into 96-well plates at a density of 1 × 104 cells / well and cultured for 24 hours for cell attachment. Thereafter, the sample was diluted with DMEM cell culture medium containing 10% fetal bovine serum (FBS) to dissolve Ce6 and HA-Ce6 NP and to give a final concentration of 1, 5, 10, 20 μM Ce6 equivalents. The existing cell culture medium in the cells was replaced with a culture medium containing a photosensitizer and treated for 24 hours. After this, the cell culture medium containing the photosensitizer was removed, the cells were washed three times, and a new cell culture medium was added to each well. Cell viability was measured using a cell counting kit (Dojindo Labotatories). Control cancer cells were treated with cell culture medium containing no photosensitizer for 24 hours and cell viability was measured. The cell viability of each sample-treated group was determined assuming that the cell viability of the control group was 100%. According to Fig. 9A, Ce6 and HA-Ce6 NP did not show cytotoxicity when light was not irradiated.
다음으로, 광역학 치료 효능을 평가하였다. U-87MG 세포를 96-well 플레이트에 1×104cells/well 밀도로 접종하고 세포부착을 위해 24시간 동안 배양하였다. 그 후, 10% 소태아혈청(FBS)를 함유하는 DMEM 세포 배양액을 사용하여 Ce6 및 HA-Ce6 NP를 녹이고, 최종농도 0.1, 0.5, 1, 2μM Ce6 당량이 되도록 샘플을 희석하였다. 세포에 있는 기존의 세포배양액을 광감각제를 함유한 배지로 교체하고 24시간 동안 처리해주었다. 이 후, 광감각제가 함유된 세포배양액을 제거하고, 세포를 3번 세척한 후 새로운 세포배양액을 각각의 well에 첨가해 주었다. 광역학 치료(PDT)를 위하여, 세포에 670 nm 레이저(조사선량 속도 50 mW/cm2 및 조사선량 5 J/cm2)를 사용하여 빛을 조사하였다. 빛 조사 후, 세포를 24시간 동안 추가 배양하고 세포 계수 키트를 사용하여 세포 생존율을 측정하였다. 도 9B에 의하면, HA-Ce6 NP는 일항산소 생성 능력이 현저히 억제되어 있음에도 불구하고, Ce6과 비슷한 광역학 치료 효과를 나타 내었다. 이것은 세포내로 섭취된 HA-Ce6 NP의 일항산소 생성 능력이 세포내에 존재하는 환원제인 글루타티온에 의해서 회복되었기 때문인 것으로 보였다.
Next, the photodynamic therapy efficacy was evaluated. U-87MG cells were inoculated into 96-well plates at a density of 1 × 104 cells / well and cultured for 24 hours for cell attachment. Thereafter, the sample was diluted with DMEM cell culture medium containing 10% fetal bovine serum (FBS) to dissolve Ce6 and HA-Ce6 NP, and to have a final concentration of 0.1, 0.5, 1, 2 μM Ce6 equivalents. The existing cell culture medium in the cells was replaced with a culture medium containing a photosensitizer and treated for 24 hours. After this, the cell culture medium containing the photosensitizer was removed, the cells were washed three times, and a new cell culture medium was added to each well. For photodynamic therapy (PDT), cells were irradiated with 670 nm laser (
실험예Experimental Example 5: 체외 세포 흡수 및 형광 활성 시험 5: In vitro cell uptake and fluorescence activity test
Ce6 및 HA-Ce6 NP를 세포배양액을 사용하여 용해 및 희석시킨 후 2 μM Ce6 당량으로 농도를 맞추었다. 먼저 광감각제의 세포내 흡수 및 형광 활성화를 정량분석하기 위하여 flow cytometric analysis (FACS) 분석을 실시하였다. U-87MG세포를 6-웰 플레이트에 1×105cells/well의 숫자로 넣고, 용기 바닥에 세포가 부착할 수 있도록 24시간 동안 배양하였다. 이후, Ce6 및 HA-Ce6 NP가 용해된 세포배양액으로 교체하고, 18시간동안 처리해주었다. 세포밖에 존재하는 광감각제를 제거하기 위하여 세포를 세포배양액으로 세번 세척하고 신선한 배지를 첨가하였다. 세포를 FACS 튜브에 옮기고, 633 nm 레이저를 이용하여 여기 시키면서 형광을 측정하였다. 도 10의 FACS 분석 결과에 의하면, HA-Ce NP를 처리한 세포는 Ce6를 처리한 세포와 유사한 형광 강도를 보였다. 이는 HA-Ce6 NP의 형광 발생 능력이 세포내에서 다시 활성화 되었음을 말해준다.Ce6 and HA-Ce6 NP were dissolved and diluted with the cell culture medium, and the concentration was adjusted to 2 μM Ce6 equivalents. First, flow cytometric analysis (FACS) analysis was performed to quantitate intracellular absorption and fluorescence activation of the photosensitizer. U-87MG cells were added to a 6-well plate at a number of 1 × 105 cells / well and cultured for 24 hours to allow cells to adhere to the bottom of the container. Subsequently, the cells were replaced with a cell culture solution in which Ce6 and HA-Ce6 NP were dissolved, and treated for 18 hours. Cells were washed three times with cell culture medium and fresh medium was added to remove the photosensitizer present outside the cells. The cells were transferred to a FACS tube and fluorescence was measured by excitation using a 633 nm laser. According to the FACS analysis of FIG. 10, HA-Ce NP treated cells showed fluorescence intensity similar to that of Ce6 treated cells. This suggests that the ability of HA-Ce6 NP to induce fluorescence was re-activated in the cells.
글루타티온이 높은 농도로 존재하는 리소좀(lysosome)에서 형광이 활성화 되는지를 확인하기 위하여, LysoTracker를 이용하여 세포의 리소좀을 라벨링하고 Ce6 형광이 발생되는 곳과 위치가 겹치는지를 평가하였다. U-87MG세포를 LabTek II Chambered Coverglass (Nalge Nunc International Corp.)에 1×105 cells/well의 숫자로 넣고, 용기 바닥에 세포 부착할 수 있도록 24시간 동안 배양하였다. 이후, Ce6 및 HA-Ce6 NP가 2μM Ce6 당량으로 용해된 세포배양액으로 교체하고, 18시간동안 처리해주었다. 세포밖에 존재하는 광감각제를 제거하기 위하여 세포를 세포배양액으로 세번 세척하고, 리소좀을 형광 염색하는 시약인 Lyso-tracker blue-DND22 (Molecular Probe사)가 100 nM 농도로 함유된 배지로 30분 동안 추가 처리해 주였다. 공초점 현미경 (confocal laser scanning microscope ;CLSM, ZEISS LSM 510 META)을 이용하여 Ce6 및 HA-Ce6 NP의 형광(여기: 405 nm, 발광: 650 nm long-pass filter)과 Lysotracker의 형광 영상을 각각 얻은 후 세포 내에서 두 형광 영상이 겹치는 곳을 확인하였다. 도 11A에 의하면, HA-Ce6 NP와 Lysotracker의 형광영상이 상당부분 겹치는 것을 볼 수 있으며, 이것은 HA-Ce6 NP의 형광 활성화가 글루타티온이 높은 농도로 존재하는 리소좀에서 일어났음을 보여준다. 도 11b에 의하면, Ce6의 형광과 lysotracker의 형광이 겹치는 부분은 적은 것으로 나타났다.
To determine if fluorescence is activated in lysosomes with high glutathione concentrations, LysoTracker was used to label the lysosomes of the cells and assess whether they overlap with where the Ce6 fluorescence occurs. U-87MG cells were plated in LabTek II Chambered Coverglass (Nalge Nunc International Corp.) at a number of 1 × 105 cells / well and incubated for 24 hours so that cells could be attached to the bottom of the container. Subsequently, the cell culture broth in which Ce6 and HA-Ce6 NP were dissolved in 2 占 Ce Ce6 equivalents was replaced and treated for 18 hours. Cells were washed three times with the cell culture medium to remove the photosensitizer present outside the cells, and Lyso-tracker blue-DND22 (Molecular Probe), a reagent for fluorescent dyeing lysosomes, was inoculated in a medium containing 100 nM for 30 minutes Further processing was required. Fluorescence images of Ce6 and HA-Ce6 NP (excitation: 405 nm, emission: 650 nm long-pass filter) and Lysotracker were obtained using a confocal laser scanning microscope (CLSM, ZEISS LSM 510 META) We observed the overlap of two fluorescent images in the posterior cells. Figure 11A shows a substantial overlap of fluorescence images of HA-Ce6 NP with Lysotracker, indicating that the fluorescence activation of HA-Ce6 NP occurred in lysosomes with high glutathione concentrations. Referring to FIG. 11B, there is little overlap between the fluorescence of Ce6 and the fluorescence of lysotracker.
Claims (11)
Translated fromKoreanA photosensitizer; Polymer; And a connector for covalently coupling the photo-sensing agent and the polymer, wherein the connector is coupled to a disulfide linker comprising a disulfide bond.
The polymer-optical sensing agent conjugate according to claim 1, wherein the polymer is a biocompatible polymer or a synthetic polymer.
The biodegradable polymer according to claim 2, wherein the biocompatible polymer is hyaluronic acid, gelatin, collagen, chitosan, glycol chitosan, heparin, heparan sulfate, pullulan, chondroitin sulfate, elastin, dextran or albumin. A combination.
3. The method of claim 2, wherein the synthetic polymer is selected from the group consisting of polyacrylic acid, poly-L-lysine, polyethylene glycol-polylysine, polyaspartic acid, polyethylene glycol-polyaspartic acid, polyglutamic acid, polyethylene glycol- polyglutamic acid, Hydroxypropylmethacrylamide copolymer, hydroxypropylmethacrylamide copolymer, hydroxypropylmethacrylamide copolymer, polyethyleneimine, polyethylene glycol-polyethyleneimine, polyvinyl alcohol or dendrimer.
[화학식 1]
상기 식에서, n1 및 n2는 각각 독립적으로 1 내지 5의 정수이다.
[2] The compound according to claim 1, wherein the linker is represented by the following Formula 1, wherein one carboxyl group of the polymer is bonded to one amine group of the compound represented by the following Formula 1, Polymer-light sensation agent conjugated with a photosensitizer:
[Chemical Formula 1]
In the above formula, n1 and n2 are each independently an integer of 1 to 5.
2. The polymer-optical photosensitizer conjugate according to claim 1, wherein the photo-sensitizer is a porphyrin compound or a non-porphyrin compound in the form of a free base or a metal complex.
시기와 하기 화학식 1의 아민기가 결합하는 것을 특징으로 하는 고분자-광감각제 결합체:
[화학식 1]
상기 식에서, n1 및 n2는 각각 독립적으로 1 내지 5의 정수이다.
7. The method of claim 6, wherein the photosensitizer is chlorine e6,
Polymer and the amine group of the following formula (1) are bonded to each other:
[Chemical Formula 1]
In the above formula, n1 and n2 are each independently an integer of 1 to 5.
The polymer-photosensitizer conjugate according to claim 1, wherein the photo-sensitizer is a rhodamine derivative, an Alexa derivative, a bipiperidine derivative or a cyanine derivative and emits a fluorescence signal in a near infrared wavelength range of 600 to 900 nm.
2. The polymer-light sensing agent conjugate according to claim 1, wherein a target-type ligand is further bonded to the polymer-light sensing agent conjugate.
10. The polymer-photosensitizer conjugate of claim 9, wherein the target ligand is an antibody, ribhexane (RNA) or deoxyribohexane (DNA) plasmid, a peptide ligand, or folic acid.
10. A composition for fluorescence imaging or photodynamic therapy comprising a polymer-light sensing agent conjugate coupled to a disulfide linker of any one of claims 1 to 10 and a pharmaceutically acceptable carrier.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020120123244AKR101452819B1 (en) | 2012-11-01 | 2012-11-01 | Redox-responsive polymer-photosensitizer conjugate containing disulfide linker and its composition for fluorescence imaging and photodynamic therapy comprising thereof |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020120123244AKR101452819B1 (en) | 2012-11-01 | 2012-11-01 | Redox-responsive polymer-photosensitizer conjugate containing disulfide linker and its composition for fluorescence imaging and photodynamic therapy comprising thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20140057718Atrue KR20140057718A (en) | 2014-05-14 |
| KR101452819B1 KR101452819B1 (en) | 2014-10-23 |
Family
ID=50888268
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020120123244AExpired - Fee RelatedKR101452819B1 (en) | 2012-11-01 | 2012-11-01 | Redox-responsive polymer-photosensitizer conjugate containing disulfide linker and its composition for fluorescence imaging and photodynamic therapy comprising thereof |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR101452819B1 (en) |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107095859A (en)* | 2017-04-24 | 2017-08-29 | 四川大学 | A kind of medicament-carried nano capsule sensitive with tumour cell bioreductive microenvironment and preparation method thereof |
| CN107982547A (en)* | 2017-07-27 | 2018-05-04 | 大连民族大学 | Redox responds the application of chitosan-liposome |
| KR20190103999A (en)* | 2018-02-28 | 2019-09-05 | 부산대학교 산학협력단 | Nanodrug Composites, preparation method therof, and use for the same |
| CN112386695A (en)* | 2020-11-30 | 2021-02-23 | 西安交通大学 | Chitosan-based nano prodrug carrying indocyanine green and platinum drugs and preparation method thereof |
| CN112876837A (en)* | 2020-04-08 | 2021-06-01 | 四川大学 | Photoreduction degradation composition and preparation method and application thereof |
| KR20210099899A (en)* | 2020-02-05 | 2021-08-13 | 가톨릭대학교 산학협력단 | Fabrication of Photo-responsive Nanodiamond Particles for Photodynamic Cancer Treatment |
| WO2021235661A1 (en)* | 2020-05-21 | 2021-11-25 | 가톨릭대학교 산학협력단 | Enteroendocrine cell target polymer conjugated with photosensitizer, and medical use thereof for ameliorating metabolic disease |
| CN114668854A (en)* | 2022-03-14 | 2022-06-28 | 山东滨州智源生物科技有限公司 | Photoactivated porphyrin prodrug ternary assembly, preparation method and application thereof |
| CN115462372A (en)* | 2022-09-07 | 2022-12-13 | 武汉理工大学 | A GSH-responsive photodynamic antibacterial nanosystem and its preparation method and application |
| WO2024144339A1 (en)* | 2022-12-29 | 2024-07-04 | 가톨릭대학교 산학협력단 | Pharmaceutical composition for enhancing anticancer effect of immune checkpoint inhibitor |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101847264B1 (en) | 2016-03-29 | 2018-04-10 | 국립암센터 | Antigen-responsive antibody-fluorochrome conjugates and method detecting target-cells using fluorescence imaging by thereof |
| KR20250066811A (en) | 2023-11-07 | 2025-05-14 | 서울대학교산학협력단 | Charge-convertible nanoparticle, and medical use thereof |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8057821B2 (en) | 2004-11-03 | 2011-11-15 | Egen, Inc. | Biodegradable cross-linked cationic multi-block copolymers for gene delivery and methods of making thereof |
| WO2006064453A2 (en) | 2004-12-17 | 2006-06-22 | Koninklijke Philips Electronics N.V. | Targeting agents for molecular imaging |
| KR100911250B1 (en) | 2009-04-29 | 2009-08-07 | 다이아텍코리아 주식회사 | Method for preparing a novel chlorine e6-folate binding compound |
| KR101116570B1 (en) | 2009-10-08 | 2012-02-14 | 국립암센터 | Photosensitive agent-metal nanoparticle complex and composition for photodynamic therapy or diagnosis containing the same |
- 2012
- 2012-11-01KRKR1020120123244Apatent/KR101452819B1/ennot_activeExpired - Fee Related
Cited By (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107095859A (en)* | 2017-04-24 | 2017-08-29 | 四川大学 | A kind of medicament-carried nano capsule sensitive with tumour cell bioreductive microenvironment and preparation method thereof |
| CN107095859B (en)* | 2017-04-24 | 2020-03-10 | 四川大学 | Drug-loaded nanocapsule with tumor cell bioreductive microenvironment sensitivity and preparation method thereof |
| CN107982547A (en)* | 2017-07-27 | 2018-05-04 | 大连民族大学 | Redox responds the application of chitosan-liposome |
| CN107982547B (en)* | 2017-07-27 | 2020-10-16 | 大连民族大学 | Application of redox-responsive chitosan-liposomes |
| KR20190103999A (en)* | 2018-02-28 | 2019-09-05 | 부산대학교 산학협력단 | Nanodrug Composites, preparation method therof, and use for the same |
| KR20210099899A (en)* | 2020-02-05 | 2021-08-13 | 가톨릭대학교 산학협력단 | Fabrication of Photo-responsive Nanodiamond Particles for Photodynamic Cancer Treatment |
| CN112876837A (en)* | 2020-04-08 | 2021-06-01 | 四川大学 | Photoreduction degradation composition and preparation method and application thereof |
| CN112876837B (en)* | 2020-04-08 | 2021-11-23 | 四川大学 | Photoreduction degradation composition and preparation method and application thereof |
| WO2021235661A1 (en)* | 2020-05-21 | 2021-11-25 | 가톨릭대학교 산학협력단 | Enteroendocrine cell target polymer conjugated with photosensitizer, and medical use thereof for ameliorating metabolic disease |
| CN112386695A (en)* | 2020-11-30 | 2021-02-23 | 西安交通大学 | Chitosan-based nano prodrug carrying indocyanine green and platinum drugs and preparation method thereof |
| CN114668854A (en)* | 2022-03-14 | 2022-06-28 | 山东滨州智源生物科技有限公司 | Photoactivated porphyrin prodrug ternary assembly, preparation method and application thereof |
| CN115462372A (en)* | 2022-09-07 | 2022-12-13 | 武汉理工大学 | A GSH-responsive photodynamic antibacterial nanosystem and its preparation method and application |
| WO2024144339A1 (en)* | 2022-12-29 | 2024-07-04 | 가톨릭대학교 산학협력단 | Pharmaceutical composition for enhancing anticancer effect of immune checkpoint inhibitor |
Also Published As
| Publication number | Publication date |
|---|---|
| KR101452819B1 (en) | 2014-10-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101452819B1 (en) | Redox-responsive polymer-photosensitizer conjugate containing disulfide linker and its composition for fluorescence imaging and photodynamic therapy comprising thereof | |
| Luo et al. | GSH-sensitive polymeric prodrug: synthesis and loading with photosensitizers as nanoscale chemo-photodynamic anti-cancer nanomedicine | |
| Lee et al. | Tumor-homing photosensitizer-conjugated glycol chitosan nanoparticles for synchronous photodynamic imaging and therapy based on cellular on/off system | |
| Yang et al. | Tumor microenvironment (TME)-activatable circular aptamer-PEG as an effective hierarchical-targeting molecular medicine for photodynamic therapy | |
| Zhang et al. | Light-triggered theranostic liposomes for tumor diagnosis and combined photodynamic and hypoxia-activated prodrug therapy | |
| Liu et al. | Photosensitizer-conjugated redox-responsive dextran theranostic nanoparticles for near-infrared cancer imaging and photodynamic therapy | |
| Liang et al. | Theranostic porphyrin dyad nanoparticles for magnetic resonance imaging guided photodynamic therapy | |
| Yang et al. | Hierarchical tumor acidity-responsive self-assembled magnetic nanotheranostics for bimodal bioimaging and photodynamic therapy | |
| JP7372672B2 (en) | Complex of active pharmaceutical ingredients | |
| Lee et al. | Tumor specificity and therapeutic efficacy of photosensitizer-encapsulated glycol chitosan-based nanoparticles in tumor-bearing mice | |
| Shi et al. | A fullerene-based multi-functional nanoplatform for cancer theranostic applications | |
| Shi et al. | PEGylated fullerene/iron oxide nanocomposites for photodynamic therapy, targeted drug delivery and MR imaging | |
| KR101035269B1 (en) | Novel photodynamic therapy using polymer derivative-photosensitizer complex | |
| Siwawannapong et al. | Ultra-small pyropheophorbide-a nanodots for near-infrared fluorescence/photoacoustic imaging-guided photodynamic therapy | |
| Huang et al. | Chlorotoxin-modified macromolecular contrast agent for MRI tumor diagnosis | |
| KR102081666B1 (en) | Phamaceutical composition for treating cancer | |
| Li et al. | A photosensitizer-conjugated magnetic iron oxide/gold hybrid nanoparticle as an activatable platform for photodynamic cancer therapy | |
| KR101336501B1 (en) | Nano ion-complex for photodynamic theraphy comprising hydrophile cationic polymer photosensitizer derivatives and anionic polysaccharide quencher derivatives | |
| KR20140014443A (en) | Graphene oxide-photosensitizers complex containing disulfide linker and composition for diagonosis and therapy of canncer using the same | |
| US20120014874A1 (en) | Photosensitizer-metal nanoparticle charge complex and composition containing the complex for photodynamic therapy or diagnosis | |
| Tang et al. | Near-infrared light-activated red-emitting upconverting nanoplatform for T1-weighted magnetic resonance imaging and photodynamic therapy | |
| Li et al. | Near-infrared light and redox dual-activatable nanosystems for synergistically cascaded cancer phototherapy with reduced skin photosensitization | |
| Li et al. | Light-enhanced hypoxia-responsive nanoparticles for deep tumor penetration and combined chemo-photodynamic therapy | |
| KR101419254B1 (en) | Enzyme-responsive graphene oxide/biopolymer-photosensitizer nanocomplex and composition for fluorescence image and photodynamic/photothermal treatment comprising thereof | |
| Zhao et al. | Multifunctional magnetic nanoparticles for simultaneous cancer near-infrared imaging and targeting photodynamic therapy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application | St.27 status event code:A-0-1-A10-A12-nap-PA0109 | |
| PA0201 | Request for examination | St.27 status event code:A-1-2-D10-D11-exm-PA0201 | |
| D13-X000 | Search requested | St.27 status event code:A-1-2-D10-D13-srh-X000 | |
| D14-X000 | Search report completed | St.27 status event code:A-1-2-D10-D14-srh-X000 | |
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection | St.27 status event code:A-1-2-D10-D21-exm-PE0902 | |
| AMND | Amendment | ||
| P11-X000 | Amendment of application requested | St.27 status event code:A-2-2-P10-P11-nap-X000 | |
| P13-X000 | Application amended | St.27 status event code:A-2-2-P10-P13-nap-X000 | |
| PG1501 | Laying open of application | St.27 status event code:A-1-1-Q10-Q12-nap-PG1501 | |
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent | St.27 status event code:N-2-6-B10-B15-exm-PE0601 | |
| AMND | Amendment | ||
| E13-X000 | Pre-grant limitation requested | St.27 status event code:A-2-3-E10-E13-lim-X000 | |
| P11-X000 | Amendment of application requested | St.27 status event code:A-2-2-P10-P11-nap-X000 | |
| P13-X000 | Application amended | St.27 status event code:A-2-2-P10-P13-nap-X000 | |
| PX0901 | Re-examination | St.27 status event code:A-2-3-E10-E12-rex-PX0901 | |
| PX0701 | Decision of registration after re-examination | St.27 status event code:A-3-4-F10-F13-rex-PX0701 | |
| X701 | Decision to grant (after re-examination) | ||
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment | St.27 status event code:A-2-4-F10-F11-exm-PR0701 | |
| PR1002 | Payment of registration fee | St.27 status event code:A-2-2-U10-U11-oth-PR1002 Fee payment year number:1 | |
| PG1601 | Publication of registration | St.27 status event code:A-4-4-Q10-Q13-nap-PG1601 | |
| P22-X000 | Classification modified | St.27 status event code:A-4-4-P10-P22-nap-X000 | |
| P22-X000 | Classification modified | St.27 status event code:A-4-4-P10-P22-nap-X000 | |
| FPAY | Annual fee payment | Payment date:20170906 Year of fee payment:4 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:4 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:5 | |
| P22-X000 | Classification modified | St.27 status event code:A-4-4-P10-P22-nap-X000 | |
| PC1903 | Unpaid annual fee | St.27 status event code:A-4-4-U10-U13-oth-PC1903 Not in force date:20191015 Payment event data comment text:Termination Category : DEFAULT_OF_REGISTRATION_FEE | |
| PC1903 | Unpaid annual fee | St.27 status event code:N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text:Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date:20191015 |