KR101640545B1 - Production method of catalyst-graphitic carbon nitride-reduced graphene oxide composite, the composite produced thereby, and an electrode using the same - Google Patents
Production method of catalyst-graphitic carbon nitride-reduced graphene oxide composite, the composite produced thereby, and an electrode using the sameDownload PDFInfo
- Publication number
- KR101640545B1 KR101640545B1KR1020150043552AKR20150043552AKR101640545B1KR 101640545 B1KR101640545 B1KR 101640545B1KR 1020150043552 AKR1020150043552 AKR 1020150043552AKR 20150043552 AKR20150043552 AKR 20150043552AKR 101640545 B1KR101640545 B1KR 101640545B1
- Authority
- KR
- South Korea
- Prior art keywords
- carbon nitride
- catalyst
- rgo
- graphene oxide
- composite
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
- C01B31/043—
- C01B31/0438—
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01G—CAPACITORS; CAPACITORS, RECTIFIERS, DETECTORS, SWITCHING DEVICES, LIGHT-SENSITIVE OR TEMPERATURE-SENSITIVE DEVICES OF THE ELECTROLYTIC TYPE
- H01G11/00—Hybrid capacitors, i.e. capacitors having different positive and negative electrodes; Electric double-layer [EDL] capacitors; Processes for the manufacture thereof or of parts thereof
- H01G11/22—Electrodes
- H01G11/30—Electrodes characterised by their material
- H01G11/32—Carbon-based
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/13—Electrodes for accumulators with non-aqueous electrolyte, e.g. for lithium-accumulators; Processes of manufacture thereof
- H01M4/133—Electrodes based on carbonaceous material, e.g. graphite-intercalation compounds or CFx
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/8647—Inert electrodes with catalytic activity, e.g. for fuel cells consisting of more than one material, e.g. consisting of composites
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Materials Engineering (AREA)
- Power Engineering (AREA)
- Composite Materials (AREA)
- Microelectronics & Electronic Packaging (AREA)
- Catalysts (AREA)
Abstract
Translated fromKoreanDescription
Translated fromKorean본 발명은 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법과, 이에 의하여 제조된 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체, 이를 이용하여 제조된 전극, 연료전지 및 커패시터에 관한 것이다.
The present invention relates to a method for producing a catalyst-graphitic carbon nitride-reduced graphene oxide composite, a catalyst-graphitic carbon nitride-reduced graphene oxide composite produced thereby, an electrode manufactured using the same, a fuel cell and a capacitor .
탄소원자가 벌집모양의 육각형의 격자를 가진 탄소의 2차원적인 동소체인 그래핀은 양자홀 효과, 상온에서 높은 캐리어 이동도 (~10,000 cm2/Vs), 큰 비표면적(2630 cm2/g), 우수한 광투과도(~97.7%), 높은 기계적 물성(~1 TPa) 그리고 우수한 열전도도(3000-5000 W/mK) 등의 매우 우수한 특성을 지니고 있다. 이러한 그래핀을 제조하는 방법에는 흑연결정으로부터 그래핀 한 층을 분리하는 방법과 고온에서 탄소를 잘 흡착하는 전이금속을 촉매층으로 이용하여 그래핀을 합성하는 화학기상증착법 및 고온에서 결정에 흡착되어 있거나 포함되어 있던 탄소가 표면의 결을 따라 성장하는 에피성장법이 연구되고 있다. 특히, 흑연을 산화시켜 용액 상에서 분리한 후 환원시키는 화학적 박리법은 대량생산의 가능성과 화학적 개질이 용이하여 다른 소재와의 하이브리드가 가능하다는 장점 때문에 많은 연구가 진행되고 있고, 흑연을 산화시키고 이온성 물질을 층간에 삽입시켜 층간거리를 넓혀 그래핀 옥사이드를 제조하고, 이를 이차전지나 슈퍼커패시터의 전극활물질로 적용하는 연구가 진행되고 있다.Graphene, which is a two-dimensional isoform of carbon with a hexagonal grid of carbon atoms, has a quantum Hall effect, high carrier mobility (~ 10,000 cm2 / Vs) at room temperature, large specific surface area (2630 cm2 / g) It has excellent properties such as excellent light transmittance (~ 97.7%), high mechanical properties (~ 1 TPa) and excellent thermal conductivity (3000-5000 W / mK). Methods for producing such graphenes include a method of separating a graphene layer from a graphite crystal and a chemical vapor deposition method of synthesizing graphene using a transition metal that absorbs carbon well at a high temperature as a catalyst layer, An epitaxial growth method has been studied in which the contained carbon grows along the surface texture. Particularly, the chemical peeling method which oxidizes graphite and separates it in a solution state and then reduces the graphite has a lot of researches because of the possibility of mass production and easy chemical modification and hybridization with other materials. Research is being conducted to prepare graphene oxide by expanding the interlayer distance by inserting a material between layers and applying it as an electrode active material of a secondary battery or a super capacitor.
또한 그래핀은 상술한 바와 같이 독특한 전기적, 열적, 광학적, 기계적 성질을 가지면서 큰 비표면적을 가짐에 따라 특히 에너지 저장소재 및 촉매 담체로서 관심을 받고 있다. 그러나 그래핀의 촉매 담체로의 적용시, 그래핀 나노시트 사이에 작용하는 강력한 π전자 상호작용(π-π stacking interaction)으로 인한 심각한 뭉침 현상과 그래핀 나노시트의 재적층 현상, 그리고 그래핀과 나노촉매 사이의 약한 상호작용으로 인하여 지지체를 이용한 촉매의 낮은 안정성과 촉매 자체의 높은 표면 에너지가 문제되고 있다.
In addition, graphene has attracted attention as an energy storage material and a catalyst carrier especially because it has a large specific surface area with unique electrical, thermal, optical and mechanical properties as described above. However, when applied to a catalyst carrier of graphene, severe aggregation due to strong π-electron interaction (π-π stacking interaction) between graphene nanosheets and redeposition of graphene nanosheets, Due to the weak interaction between the nanocatalysts, low stability of the catalyst using the support and high surface energy of the catalyst itself are problematic.
한편, 흑연의 유사체로서, 그래파이트 형 탄소 질화물은 N-치환 흑연으로 간주될 수 있는 2차원 적층 구조를 가지고 있다. 그래파이트 형 탄소 질화물은 탄소구조체에 질소의 기능화와 더불어 높은 경도(high hardness), 낮은 마찰 계수(low friction coefficient), 촉매 활성(catalytic activity) 등의 물리적 특성으로 많은 관심을 받고 있다. 특히, 질소에 의해 나노크기의 금속입자가 잘 흡착되며, 순수한 탄소보다 물질의 전자전달이 높아 벤젠의 활성, 삼량화 반응(trimerization reactions), 이산화 탄소 활성, 광촉매 등 촉매 활성을 높인다는 보고가 있다.On the other hand, as an analogue of graphite, graphitic carbon nitride has a two-dimensional laminated structure which can be regarded as N-substituted graphite. The graphitic carbon nitride has attracted much attention due to the functionalization of nitrogen in the carbon structure and physical properties such as high hardness, low friction coefficient and catalytic activity. In particular, it has been reported that nano-sized metal particles are well adsorbed by nitrogen, and electron transfer of substances is higher than that of pure carbon, thereby increasing catalytic activity such as benzene activity, trimerization reactions, carbon dioxide activity, and photocatalyst .
그러나 종래의 알려진 그래파이트 형 탄소질화물 제조공정은 CN이 풍부한 질소 전구체의 탄화반응 또는 세밀한 열분해에 의한 축합(condensation)에 의해 합성 할 수 있다. 하지만 이렇게 만들어진 그라파이트 형 탄소질화물은 고가의 장비를 사용하여야 할 뿐 만 아니라 합성수율도 낮아 제조비용 높은 단점이 있다. 또한, 그라파이트 형 탄소질화물을 단독으로 사용하였을 경우, 산업상 이용될 만큼에 전기전도도를 나타내지 못하는 한계가 있다.
However, conventional processes for producing graphite-type carbon nitride can be synthesized by carbonization of a CN-rich nitrogen precursor or condensation by fine thermal decomposition. However, the graphite-type carbon nitride thus formed has a disadvantage in that not only expensive equipment is used but also the synthesis yield is low and the manufacturing cost is high. Further, when the graphitic carbon nitride is used singly, there is a limit in that it can not exhibit electrical conductivity so as to be used industrially.
이에, 본 발명자들은 그래핀을 에너지 저장 소재 및 촉매 담체로 적용할 수 있도록 연구한 끝에, 화학적으로 박리된 그래핀 옥사이드를 이용하여 그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체를 제조함으로써 화학적 개질과 물리적 결합이 이루어지도록 하여, 그래핀 나노시트 사이에 작용하는 강력한 π전자 상호작용과 상대적으로 약한 그래핀과 촉매 사이의 상호작용의 문제를 해결하여 촉매 담체로서 적용하여, 촉매가 담지된 그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체를 제조하고 본 발명을 완성하였다.Therefore, the present inventors have studied graphene as an energy storage material and a catalyst support, and have found that by chemically modifying graphene oxide by preparing graphene-type carbon nitride-reduced graphene oxide complex using chemically peeled graphene oxide The present invention solves the problem of strong π electron interaction acting between graphene nanosheets and interaction between relatively weak graphene and catalyst so as to be applied as a catalyst carrier, The nitride-reduced graphene oxide complex was prepared and the present invention was completed.
따라서 본 발명은, 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법을 제공하는 것을 기술적 해결과제로 한다.Accordingly, it is a technical object of the present invention to provide a process for producing a catalyst-graphitic carbon nitride-reduced graphene oxide composite.
또한 본 발명은, 상기 방법으로 제조되는 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체를 제공하는 것을 다른 해결과제로 한다.Another object of the present invention is to provide a catalyst-graphitic carbon nitride-reduced graphene oxide composite produced by the above method.
또한 본 발명은 상기 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체를 포함하는 전극을 제공하는 것을 또다른 해결과제로 한다.Another object of the present invention is to provide an electrode comprising the catalyst-graphitic carbon nitride-reduced graphene oxide complex.
또한 본 발명은 상기 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체를 포함하는 전극을 이용하여 제조되는 연료전지, 커패시터를 제공하는 것을 또다른 해결과제로 한다.
Another object of the present invention is to provide a fuel cell and a capacitor which are manufactured using the electrode including the catalyst-graphitic carbon nitride-reduced graphene oxide composite.
상기 기술적 과제를 해결하기 위한 본 발명의 일 측면에 따르면,According to an aspect of the present invention,
1) 동결 건조된 그래파이트옥사이드를 증류수에 분산시켜, 그래핀옥사이드 현탁액을 제조하는 단계;1) dispersing the lyophilized graphite oxide in distilled water to prepare a graphene oxide suspension;
2) 상기 현탁액에 탄소질화물 전구체를 첨가한 후 수열합성으로 그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체(g-C3N4@RGO)를 제조하는 단계; 및2) preparing a graphite-type carbon nitride-reduced graphene oxide complex (gC3 N4 @RGO) by hydrothermal synthesis after adding a carbon nitride precursor to the suspension; And
3) 상기 복합체를 폴리올 용매에 분산시킨 후, 전이금속염을 첨가하여 혼합하고 교반함으로써, 전이금속 촉매를 담지하는 단계;를 포함하는 것을 특징으로 하는, 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법이 제공된다.3) a step of dispersing the composite in a polyol solvent, followed by adding a transition metal salt, mixing, and stirring to transfer the transition metal catalyst, and then, carrying the catalyst-graphitic carbon nitride-reduced graphene oxide A method of making a composite is provided.
본 발명에 있어서, 상기 1)단계에서 제조된 현탁액은, 하이드록시기, 카르복실기 및 에폭시기 중에서 선택된 1종 이상의 작용기를 포함하는 그래파이트옥사이드를 포함하고; 상기 2)단계의 탄소질화물 전구체는 염화시아누르(C3Cl3N3),멜라민(C3H6N6), 멜렘 (C3H6N10) 및 멜람(C6H9N11)중에서 선택된 1종 이상인 것을 특징으로 한다.
In the present invention, the suspension prepared in the step 1) comprises graphite oxide containing at least one functional group selected from a hydroxyl group, a carboxyl group and an epoxy group; The carbon nitride precursor in the step 2) is selected from the group consisting of cyanuric chloride (C3 Cl3 N3 ), melamine (C3 H6 N6 ), melem (C3 H6 N10 ), and melam (C6 H9 N11 ) And the like.
더욱 바람직하게는, 상기 2)단계의 탄소질화물 전구체는 멜라민이고; 상기 멜라민과 그래파이트옥사이드의 중량비는 1: 5~20일 수 있다.More preferably, the carbon nitride precursor in step 2) is melamine; The weight ratio of melamine to graphite oxide may be 1: 5 to 20.
또한 본 발명에 있어서, 상기 2)단계는, 수열합성으로 g-C3N4@RGO 복합체를 제조한 후, 열처리하여 상기 g-C3N4@RGO 복합체를 안정화하는 것이 바람직하다. 더욱 바람직하게는, 상기 수열합성은 90~110℃의 온도로 48~120시간 동안 수행하고; 상기 열처리는 100~300℃의 온도로 5~30분간 수행하는 것을 특징으로 한다.In the present invention, it is preferable that the gC3 N4 @RGO composite is prepared by hydrothermal synthesis and then heat-treated to stabilize the gC3 N4 @RGO composite. More preferably, the hydrothermal synthesis is carried out at a temperature of 90 to 110 DEG C for 48 to 120 hours; The heat treatment is performed at a temperature of 100 to 300 DEG C for 5 to 30 minutes.
바람직하게는 본 발명에 있어서, 상기 3)단계는,Preferably, in the present invention, the step 3)
a) 상기 2)단계에서 제조된 g-C3N4@RGO 복합체를 표면개질하는 단계;a) modifying the surface of the gC3 N4 @RGO composite prepared in the step 2);
b) 상기 표면 개질된 복합체를 폴리올 용매에 분산시키고, 전이금속염을 더 첨가하여 혼합하는 단계; 및b) dispersing the surface-modified composite in a polyol solvent, and further adding and mixing a transition metal salt; And
c) 상기 b)단계 혼합액의 pH를 9~11로 조절한 후, 교반 및 분산함으로써 상기 표면개질된 복합체에 전이금속 촉매를 담지하는 단계;를 포함하는 것을 특징으로 한다.and c) carrying the transition metal catalyst on the surface-modified composite by adjusting the pH of the mixed solution of step b) to 9 to 11, followed by stirring and dispersing.
더욱 바람직하게는 상기 표면개질은 H2SO4, HNO3 및 P2O5 중에서 선택되는 적어도 하나 이상의 산화제를 이용하여 수행되는 것을 특징으로 한다.More preferably, the surface modification is performed using at least one oxidizing agent selected from H2 SO4 , HNO3 and P2 O5 .
또한 본 발명에 있어서, 상기 2)단계의 폴리올 용매는 에틸렌글리콜(Ethylene Glycol), 디에틸렌글리콜(Diethylene Glycol), 트리에틸렌글리콜(Triethylene Glycol) 및 테트라에틸렌글리콜(Tetraethylene Glycol)로 이루어진 군에서 선택된 1종 이상일 수 있다.In the present invention, the polyol solvent in step 2) may be selected from the group consisting of ethylene glycol, diethylene glycol, triethylene glycol, and tetraethylene glycol. It can be more than a species.
또한 본 발명에 있어서, 상기 전이금속염은, 백금(Pt), 팔라듐(Pd), 구리(Au), 은(Ag), 니켈(Ni), 코발트(Co), 철(Fe), 주석(Sn), 로듐(Rh), 오스뮴(Os), 이리듐(Ir), 텅스텐(W), 루테듐(Ru), 및 티타늄(Ti) 및 바나듐(V) 중에서 선택된 1종 이상의 금속을 포함하는 것을 특징으로 한다.
In the present invention, the transition metal salt may be at least one selected from the group consisting of Pt, Pd, Au, Ag, Ni, Co, Fe, Sn, , At least one metal selected from the group consisting of rhodium (Rh), osmium (Os), iridium (Ir), tungsten (W), ruthenium (Ru), titanium (Ti) and vanadium .
또한 상기 다른 기술적 과제를 해결하기 위한 본 발명의 다른 측면에 따르면, 상기 방법으로 제조되는, 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체가 제공된다.
According to another aspect of the present invention, there is provided a catalyst-graphitic carbon nitride-reduced graphene oxide composite produced by the above method.
또한 상기 또다른 기술적 과제를 해결하기 위한 본 발명의 또다른 측면에 따르면, 상기 촉매-그래파이트형 탄소질화물-환원된 그래핀옥사이드 복합체를 이용하여 제조되는 전극, 상기 전극을 이용하여 제조되는 연료전지, 커패시터가 이 제공된다.
According to another aspect of the present invention, there is provided an electrode manufactured using the catalyst-graphitic carbon nitride-reduced graphene oxide composite, a fuel cell manufactured using the electrode, A capacitor is provided.
또한 상기 또다른 기술적 과제를 해결하기 위한 본 발명의 또다른 측면에 따르면, 상기 촉매-그래파이트형 탄소질화물-환원된 그래핀옥사이드 복합체를 이용하여 제조되는 전극을 이용하여 제조되는 연료전지, 커패시터가 제공된다.
According to another aspect of the present invention, there is provided a fuel cell comprising: a fuel cell comprising a catalyst-graphitic carbon nitride-reduced graphene oxide complex; do.
또한 상기 또다른 기술적 과제를 해결하기 위한 본 발명의 또다른 측면에 따르면, 상기 촉매-그래파이트형 탄소질화물-환원된 그래핀옥사이드 복합체를 이용하여 제조되는 전극을 이용하여 제조되는 커패시터가 제공된다.
According to another aspect of the present invention, there is provided a capacitor manufactured using an electrode manufactured using the catalyst-graphitic carbon nitride-reduced graphene oxide composite.
본 발명의 방법에 따르면 고가의 환원제를 사용하지 않고도 산소 작용기가 제거된 환원된 그래핀 옥사이드를 제조할 수 있고, 그래핀 옥사이드가 재적층되는(restacking) 것을 방지 할 수 있어 그래핀 옥사이드를 촉매 담체로서 적용할 수 있는 효과가 있다. 또한, 종래 알려진 그래파이트형 탄소 질화물 제조과정 중 탄화반응 또는 고온의 열적 처리 없이 그래핀 옥사이드 상에 그래파이트형 탄소 질화물이 고르게 분포되어 높은 수율의 그래파이트형 탄소질화물-환원된 그래핀 옥사이드(g-C3N4@RGO) 복합체를 제조할 수 있는 효과가 있다.According to the method of the present invention, it is possible to produce reduced graphene oxide from which an oxygen functional group is removed without using an expensive reducing agent, and it is possible to prevent restacking of graphene oxide, As shown in Fig. Further, graphite-type carbon nitride is uniformly distributed on graphene oxide without carbonization or thermal treatment at a high temperature in a conventional process for producing graphite-type carbon nitride, and a high yield of graphite-type carbon nitride-reduced graphene oxide (gC3 N4 @ RGO) complexes can be produced.
또한 본 발명에 따른 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법에 따르면, 물질 이동성 및 표면적이 극대화되어 매우 우수한 물리적 특성 및 전기적 특성을 가지면서, 촉매 금속 입자가 더욱 작은 형태로 고분산될 수 있어, 에너지 저장소재로서 응용됨은 물론, 금속 촉매가 지지된 촉매체로서 다양한 분야에 응용되는 것도 가능하다.
Also, according to the method for producing a catalyst-graphitic carbon nitride-reduced graphene oxide composite according to the present invention, the material mobility and the surface area are maximized, and the catalyst metal particles are formed into a smaller form It can be applied to various fields as a catalyst body supported with a metal catalyst as well as an energy storage material.
도 1은 본 발명에 따른 촉매-그래파이트형 탄소질화물-환원된 그래핀옥사이드(M/g-C3N4@RGO) 복합체의 제조공정의 흐름도 및 복합체를 모식화하여 나타낸 것이다.
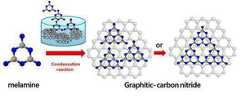
도 2는 본 발명의 일 실시예에 따라 멜라민을 이용하여 g-C3N4@RGO를 제조하는 반응을 모식화하여 나타낸 것이다.
도 3은 본 발명의 일 실시예에 따른 g-C3N4@RGO 복합체 및 RGO의 SEM 분석결과를 나타낸 것이다.
도 4는 본 발명의 일 실시예에 따른 g-C3N4@RGO 복합체 및 RGO의 EDAX분석결과를 나타낸 것이다.
도 5는 본 발명의 일 실시예에 따른 g-C3N4@RGO 복합체 및 RGO의 FT-IR 분석결과를 나타낸 것이다.
도 6은 본 발명의 일 실시예에 따른 Pt/g-C3N4@RGO 복합체 및 Pt/RGO의 TEM 분석결과와 입도분포를 나타낸 것이다.
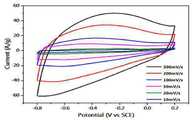
도 7 및 도 8은 본 발명의 일 실시예에 따른 g-C3N4@RGO 복합체 및 RGO의 정전용량 측정 결과를 나타낸 것이다.
도 9는 본 발명의 일 실시예에 따른 g-C3N4@RGO 복합체 및 RGO의 비정전 용량 분석 결과를 나타낸 것이다.
도 10은 본 발명의 일 실시예에 따른 Pt/g-C3N4@RGO 복합체, Pt/RGO, Pt/G 및 Pt/C의 ECSA 측정 결과를 나타낸 것이다.BRIEF DESCRIPTION OF THE DRAWINGS FIG. 1 is a schematic representation of a flow diagram and complex of a process for preparing a catalyst-graphitic carbon nitride-reduced graphene oxide (M / gC3 N4 @ RGO) complex according to the present invention.
Figure 2 is a schematic representation of the reaction to produce gC3 N4 @RGO using melamine in accordance with one embodiment of the present invention.
FIG. 3 shows SEM analysis results of the gC3 N4 @RGO complex and RGO according to an embodiment of the present invention.
FIG. 4 shows the EDAX analysis results of the gC3 N4 @RGO complex and RGO according to an embodiment of the present invention.
FIG. 5 shows FT-IR analysis results of gC3 N4 @RGO complex and RGO according to an embodiment of the present invention.
FIG. 6 shows TEM analysis results and particle size distribution of Pt / gC3 N4 @RGO composite and Pt / RGO according to an embodiment of the present invention.
FIGS. 7 and 8 show the results of capacitance measurement of gC3 N4 @RGO composite and RGO according to an embodiment of the present invention.
FIG. 9 shows the results of the noncontact capacity analysis of gC3 N4 @RGO complex and RGO according to an embodiment of the present invention.
FIG. 10 shows the results of ECSA measurement of Pt / gC3 N4 @RGO composite, Pt / RGO, Pt / G and Pt / C according to an embodiment of the present invention.
이하, 본 발명을 상세하게 설명한다.Hereinafter, the present invention will be described in detail.
본 발명에 따른 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법은,The method for producing a catalyst-graphitic carbon nitride-reduced graphene oxide composite according to the present invention comprises:
1) 동결 건조된 그래파이트 옥사이드를 증류수에 분산시켜, 그래핀옥사이드 현탁액을 제조하는 단계;1) dispersing the lyophilized graphite oxide in distilled water to prepare a graphene oxide suspension;
2) 상기 현탁액에 탄소질화물 전구체를 첨가한 후 수열합성으로 그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체(g-C3N4@RGO)를 제조하는 단계; 및2) preparing a graphite-type carbon nitride-reduced graphene oxide complex (gC3 N4 @RGO) by hydrothermal synthesis after adding a carbon nitride precursor to the suspension; And
3) 상기 복합체를 폴리올 용매에 분산시킨 후, 전이금속염을 첨가하여 혼합하고 교반함으로써, 전이금속 촉매를 담지하는 단계;를 포함한다.3) dispersing the composite in a polyol solvent, and then adding a transition metal salt, mixing, and stirring to carry the transition metal catalyst.
본 발명에 따른 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법에 있어서 상기 1)단계는 그래핀 옥사이드 현탁액을 제조하는 단계이다.In the method for producing the catalyst-graphitic carbon nitride-reduced graphene oxide complex according to the present invention, the step 1) is a step of preparing a graphene oxide suspension.
구체적으로, 동결 건조된 그래파이트 옥사이드를 증류수 하에서 초음파로 분산하여 증류수 내에 균일하게 분산된 그래핀 옥사이드 현탁액을 제조하게 된다. 이 때, 초음파 분산 정도는 그래파이트 옥사이드의 층과 층 사이에 용매가 삽입되는 것을 돕고, 그래핀 옥사이드의 박리를 유도하여 그래핀 옥사이드를 그래파이트 형 탄소질화물의 주형(Template)으로 작용하게 한다.Specifically, the freeze-dried graphite oxide is dispersed by ultrasonication under distilled water to prepare a graphene oxide suspension uniformly dispersed in distilled water. At this time, the degree of ultrasonic dispersion assists the solvent to be inserted between the layer of the graphite oxide and induces the separation of the graphene oxide, so that the graphene oxide acts as a template of the graphitic carbon nitride.
또한 상기 그래파이트 옥사이드는 Hummers 방법을 비롯한 공지된 다양한 방법으로 제조된 그래파이트 옥사이드를 사용할 수 있고, 상기 그래파이트 옥사이드의 제조시 산화방법 또는 처리시간 등을 조절함으로써 그래파이트 옥사이드의 층간 거리 및 산화정도, 결함정도, 크기 등을 제어할 수 있다. 이 때, 상기 그래파이트옥사이드는 H2SO4, K2S2O8, KNO3, 및 KMnO4 중에서 적어도 하나의 산화제를 이용하여 표면에 하이드록시기, 카르복실기, 에폭시기 등과 같은 작용기가 부착된 그래파이트 옥사이드를 이용할 수 있다. 상기 작용기가 부착되어 표면개질된 그래파이트 옥사이드는 탄소질화물과 물리적으로 결합될 수 있도록 하여 그래파이트 형 탄소질화물의 생성을 도울 수 있게 된다.The graphite oxide may be prepared by a variety of known methods including Hummers method. In the production of the graphite oxide, by controlling the oxidation method or the treatment time, the interlayer distance and oxidation degree of graphite oxide, the degree of defect, Size, and so on. At this time, the graphite oxide may be formed using at least one oxidizing agent selected from the group consisting of H2 SO4 , K2 S2 O8 , KNO3 , and KMnO4 , and a graphite oxide having a functional group such as a hydroxyl group, a carboxyl group, Can be used. The graphite oxide to which the functional group is attached and the surface-modified graphite oxide can physically bond with the carbon nitride, thereby helping to produce graphitic carbon nitride.
또한 상기 그래파이트 옥사이드는 특히 동결 건조된 그래파이트 옥사이드를 이용함으로써 그래핀 시트간 층간 간격이 좁아져 다시 재적층되는 현상을 방지하게 된다.
In addition, the use of the freeze-dried graphite oxide prevents the phenomenon that the interlayer spacing between graphene sheets is narrowed and re-deposited again.
또한 본 발명에 따른 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법에 있어서 상기 2)단계는 그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체(g-C3N4@RGO)를 제조하는 단계이다.Also, in the method for producing the catalyst-graphitic carbon nitride-reduced graphene oxide composite according to the present invention, the step 2) is a step of preparing a graphite-type carbon nitride-reduced graphene oxide complex (gC3 N4 @RGO) .
구체적으로, 상기 1)단계에서 제조된 그래핀 옥사이드 현탁액에 탄소질화물 전구체를 첨가한 후, 수열합성에 의하여 C3N4네트워크 구조를 갖는 그래파이트형 탄소질화물-환원된 그래핀 옥사이드(g-C3N4@RGO) 복합체가 제조된다.Specifically, a carbon nitride precursor was added to the graphene oxide suspension prepared in the step 1), and then a graphite-type carbon nitride-reduced graphene oxide having a C3 N4 network structure (gC3 N4 @ RGO) complexes are prepared.
또한 탄소질화물 전구체로는 염화시아누르 (C3Cl3N3), 멜라민 (C3H6N6), 멜렘 (C3H6N10) 및 멜람 (C6H9N11)중에서 선택된 1종 이상을 사용할 수 있다.The carbon nitride precursors include cyanuric chloride (C3 Cl3 N3 ), melamine (C3 H6 N6 ), melem (C3 H6 N10 ), and melam (C6 H9 N11 ) May be used.
구체적으로 멜라민의 경우 반응을 모식화하여 도 2에 나타낸 바와 같이, 상기 멜라민은 상기 1)단계에서 그래핀 옥사이드의 작용기의 도움으로 반응 및 축합에 의해 복제가 일어나며 C3N4 네트워크 구조를 갖는 그래파이트형 탄소 질화물이 형성된다.Specifically, in the case of melamine, the reaction is modeled and as shown in FIG. 2, the melamine is replicated by reaction and condensation with the aid of the functional group of graphene oxide in the step 1), and graphite having a C3 N4 network structure Type carbon nitride is formed.
또한 상기 멜라민은 그래파이트 옥사이드와의 중량비가 1:5~20 범위가 되도록 첨가할 수 있다. 멜라민이 상기 중량범위 미만으로 첨가되는 경우, 그래핀 옥사이드의 환원이 효과적으로 일어나기 어려울 뿐 만 아니라, 향상된 그래파이트 형 탄소질화물을 생성에 제한이 되며, 상기 중량범위를 초과하는 경우 반응의 부산물을 형성하여 성능을 저하시킬 수 있다.The melamine may be added in a weight ratio of 1: 5 to 20 with respect to graphite oxide. When melamine is added in an amount less than the above-mentioned weight range, reduction of graphene oxide is difficult to occur effectively, and in addition, formation of an improved graphite-type carbon nitride is limited, and if it exceeds the weight range, by- Can be reduced.
또한 상기 2)단계의 수열합성은 90℃ 내지 110℃ 온도에서 48시간 내지 120시간을 수행하는 것이 바람직하다. 온도가 90℃ 미만일 경우, 그래파이트 형 탄소질화물로 전환 효율이 감소하고 상기 온도범위를 초과하는 경우 그래핀옥사이드의 산소작용기가 열로 인해 분해되어 합성효율을 감소시킬 수 있어 바람직하지 않다. 또한 상기 온도범위에서의 수열합성 시간이 48시간 미만일 경우, 탄소질화물 기본단위인 멜론(melem)구조의 비율이 높아 고도의 규칙적인 배열된 구조를 가지기 어려우며 120시간을 초과하게 되면 반응시간이 길어져 효율이 저하되는 문제가 있다.The hydrothermal synthesis of step 2) is preferably performed at a temperature of 90 ° C to 110 ° C for 48 hours to 120 hours. When the temperature is less than 90 ° C, the conversion efficiency decreases to graphite-type carbon nitride, and when the temperature exceeds the above range, the oxygen functional groups of graphene oxide are decomposed due to heat to reduce synthesis efficiency. When the hydrothermal synthesis time in the temperature range is less than 48 hours, the proportion of the melon structure, which is a basic unit of carbon nitride, is high and it is difficult to have a highly ordered structure. When the hydrothermal synthesis time exceeds 120 hours, Is lowered.
또한 상기 2)단계의 수열합성과정에서, 별도의 환원제 없이도 산소 작용기가 제거된 환원된 그래핀 옥사이드가 제조되면서, 그래파이트형 탄소질화물이 고르게 분포된 높은 수율의 g-C3N4@RGO 복합체가 형성되고, 그래핀 옥사이드가 재적층되는 것도 방지하게 된다.Also, in the hydrothermal synthesis process in the step 2), reduced graphene oxide having oxygen functional groups removed without using any reducing agent, a gC3 N4 @RGO complex having a uniformly distributed graphite type carbon nitride is formed , Preventing graphene oxide from being deposited again.
이 때, 상기 수열합성으로 g-C3N4@RGO 복합체를 제조한 후, 여과, 세척 및 건조한 다음, 열처리(anealing)하여 g-C3N4@RGO 복합체를 안정화시키는 단계를 더 수행할 수 있다. 이 때, 상기 열처리는 불활성 가스 분위기 하에서 100~300℃의 온도로 5~30분간 수행할 수 있다.
At this time, the gC3 N4 @RGO complex may be prepared by the hydrothermal synthesis, followed by filtration, washing, drying, and then annealing to stabilize the gC3 N4 @RGO complex. At this time, the heat treatment may be performed at a temperature of 100 to 300 ° C for 5 to 30 minutes under an inert gas atmosphere.
또한 본 발명에 따른 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법에 있어서 상기 3)단계는 전이금속 촉매를 담지하는 단계이다.Also, in the method for preparing a catalyst-graphitic carbon nitride-reduced graphene oxide composite according to the present invention, the step 3) is a step of supporting a transition metal catalyst.
구체적으로, 상기 g-C3N4@RGO 복합체를 폴리올 용매에 분산시킨 후, 전이금속(M)염을 첨가하여 혼합하고 교반함으로써 분산시켜 전이금속 촉매가 g-C3N4@RGO 복합체에 담지된 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체(M/g-C3N4@RGO)가 제조된다.Specifically, the gC3 N4 @RGO complex is dispersed in a polyol solvent, and then a transition metal (M) salt is added thereto, followed by mixing and stirring to disperse the catalyst. The transition metal catalyst is supported on the gC3 N4 @RGO complex. A graphite-type carbon nitride-reduced graphene oxide complex (M / g C3 N4 @ RGO) is prepared.
본 발명에 있어서, 상기 g-C3N4@RGO 복합체는 소수성이므로 촉매가 담지될 수 있도록 활성화하는 과정을 더 거치는 것이 바람직하다. 따라서, 상기 3)단계는,In the present invention, since the gC3 N4 @RGO complex is hydrophobic, it is preferable to further activate the catalyst so that the catalyst can be supported. Therefore, in the step 3)
a) 상기 2)단계에서 제조된 g-C3N4@RGO 복합체를 표면개질하는 단계;a) modifying the surface of the gC3 N4 @RGO composite prepared in the step 2);
b) 상기 표면 개질된 복합체를 폴리올 용매에 분산시키고, 전이금속염을 더 첨가하여 혼합하는 단계; 및b) dispersing the surface-modified composite in a polyol solvent, and further adding and mixing a transition metal salt; And
c) 상기 b)단계 혼합액의 pH를 9~11로 조절한 후, 교반 및 분산함으로써 상기 표면개질된 복합체에 전이금속 촉매를 담지하는 단계;를 포함한다.c) carrying the transition metal catalyst on the surface-modified composite by controlling the pH of the mixed solution of step b) to 9 to 11, followed by stirring and dispersing.
이 때, 상기 a)단계의 표면 개질은 화학적 처리방법 또는 물리적 결합방법을 통한 표면 개질이 가능하다.At this time, the surface modification in step a) can be performed by a chemical treatment method or a physical bonding method.
화학적 처리의 경우, H2SO4, HNO3 및 P2O5 중에서 선택되는 적어도 하나 이상의 산화제를 이용하여 산처리하여 표면 개질이 가능하고, 이에 한정되지 않고 당 업계에 공지된 방법을 이용하여 표면 개질하는 것이 가능하다.In the case of chemical treatment, surface modification can be performed by acid treatment using at least one oxidizing agent selected from H2 SO4 , HNO3, and P2 O5 , and the surface modification is not limited thereto, It is possible to modify it.
예를 들면, 고온의 산성 용액에서 1 내지 8시간 동안 교반하여 g-C3N4@RGO에 하이드록시기를 도입할 수 있다. 이 때, 상기 교반 시간이 1시간 미만일 경우, g-C3N4@RGO 복합체의 표면이 충분히 개질되지 않으며, 8시간 이상일 경우 탄소체로 이루어진 g-C3N4@RGO의 구조가 파괴되어 우수한 특성이 손실될 우려가 있다.For example, a hydroxy group can be introduced into gC3 N4 @RGO by stirring in a hot acidic solution for 1 to 8 hours. If the agitation time is less than 1 hour, the surface of the gC3 N4 @RGO composite is not sufficiently modified, and if the agitation time is more than 8 hours, the structure of gC3 N4 @RGO composed of a carbon material is destroyed and excellent properties are lost There is a concern.
또한 물리적 결합의 경우, 고분자 등을 결합하여 표면 개질하는 것이 가능하며, 바람직하게는 N-alkyl이나 N,N-dialkyl amide 그룹을 가지는 전도성 고분자를 사용할 수 있다. 이러한 전도성 고분자로는 폴리아닐린계 고분자, 폴리피롤계 고분자, 폴리티오펜계 고분자 및 폴리파라페닐렌계 고분자로 이루어진 군으로부터 선택된 1종 이상일 수 있으나, 이에 한정되지 않는다.Further, in the case of physical bonding, it is possible to modify the surface by bonding polymers or the like, and preferably a conductive polymer having N-alkyl or N, N-dialkyl amide groups can be used. The conductive polymer may be at least one selected from the group consisting of a polyaniline-based polymer, a polypyrrole-based polymer, a polythiophene-based polymer, and a polyparaphenylene-based polymer.
물리적 결합의 예를 들면, 상기 전도성 고분자를 용매에 녹인 후, g-C3N4@RGO 복합체를 첨가한 후 교반하여 물리적으로 전도성 고분자를 결합시켜 표면 개질이 이루어지게 된다. 이 때, 상기 용매로는 에탄올, 알코올, 물, 테트라하이드로퓨란, 메틸에틸케톤 등을 사용할 수 있으며, 바람직하게는 상기 용매는 g-C3N4@RGO 복합체와의 중량비가 1:1~50 범위로 사용하도록 한다. 상기 범위 미만인 경우 복합체의 분산 자체가 어려울 수 있고, 상기 범위 초과시 농도가 너무 낮아 전도성 고분자가 복합체에 결합되지 않는 문제가 발생할 수 있다. 또한 상기 용매에 전도성 고분자를 용해시킨 후, 복합체를 첨가한 후 15분 이상 교반하여 물리적으로 전도성 고분자가 완전히 결합할 수 있도록 하는 것이 바람직하다.
For example, the conductive polymer may be dissolved in a solvent, and then the gC3 N4 @RGO complex may be added and stirred to physically couple the conductive polymer to the surface of the conductive polymer. The solvent may be ethanol, alcohol, water, tetrahydrofuran, methyl ethyl ketone, etc. Preferably, the solvent is used in a weight ratio of 1: 1 to 50 with respect to the gC3 N4 @RGO complex Use. If it is less than the above range, dispersion of the complex itself may be difficult, and when the above range is exceeded, the concentration may be too low to cause a problem that the conductive polymer is not bonded to the complex. In addition, it is preferable to dissolve the conductive polymer in the solvent, add the complex, and stir the mixture for 15 minutes or more to physically bind the conductive polymer completely.
또한 상기 b)단계는, 상기 표면 개질된 g-C3N4@RGO 복합체를 폴리올 용매에 분산시키게 되는데 이 때, 상기 폴리올 용매는 에틸렌글리콜(Ethylene Glycol), 디에틸렌글리콜(Diethylene Glycol), 트리에틸렌글리콜(Triethylene Glycol) 및 테트라에틸렌글리콜(Tetraethylene Glycol)로 이루어진 군에서 선택된 1종 이상일 수 있다. 바람직하게는, 상기 g-C3N4@RGO 복합체는 폴리올 용매 100 중량%에 대하여 내지 0.001 내지 0.5 중량%로 사용하도록 한다. 이는 상기 함량이 0.001 중량% 미만인 경우, 반응 후, M/g-C3N4@RGO 복합체 내에서 g-C3N4@RGO 복합체 첨가에 의한 전기전도도 향상을 기대하기 어렵고, 0.5 중량%를 초과하는 경우, g-C3N4@RGO 복합체 분말의 분산이 어렵기 때문이다.In the step b), the surface-modified gC3 N4 @RGO complex is dispersed in a polyol solvent. The polyol solvent may be selected from the group consisting of ethylene glycol, diethylene glycol, triethylene glycol (Triethylene Glycol) and tetraethylene glycol (Tetraethylene Glycol). Preferably, the gC3 N4 @RGO complex is used in an amount of from 0.001 to 0.5% by weight based on 100% by weight of the polyol solvent. When the content is less than 0.001 wt%, it is difficult to expect the improvement of the electrical conductivity by adding the gC3 N4 @RGO complex in the M / g C3 N4 @RGO complex after the reaction, and when it exceeds 0.5 wt% gC3 N4 @RGO composite powder is difficult to disperse.
이어서 상기 g-C3N4@RGO 복합체 분말을 폴리올 용매에 분산시킨 용액에, 전이금속(M)염을 첨가하여 혼합하고, 상기 c)단계에서 상기 혼합액의 pH를 조절하여 촉매의 크기 분포를 조절한 후, 교반 및 분산하여 전이금속 촉매가 g-C3N4@RGO 복합체에 담지되도록 한다.Next, a transition metal (M) salt is added to and mixed with a solution in which the gC3 N4 @RGO composite powder is dispersed in a polyol solvent. In step c), the pH of the mixed solution is adjusted to control the size distribution of the catalyst Then, it is stirred and dispersed so that the transition metal catalyst is supported on the gC3 N4 @RGO complex.
이 때, 상기 혼합액의 pH는 9 내지 11로 조절함으로써 환원반응이 원활하게 진행되도록 할 수 있고, pH 조절 용매로는 강알칼리성을 가지는 수산화칼륨(KOH) 또는 수산화나트륨(NaOH) 등을 사용하는 것이 좋다. 상기 pH 범위의 조절에 의하여 담지되는 전이금속 촉매의 크기 분포를 보다 균일하게 조절할 수 있고, 이 경우, 상기 pH 조절 용매는 전이금속 염을 첨가하여 완전히 용해되어 혼합된 후에 첨가하는 것이 바람직하다.At this time, the pH of the mixed solution can be adjusted to 9 to 11 to facilitate the reduction reaction, and potassium hydroxide (KOH) or sodium hydroxide (NaOH) having a strong alkaline property can be used as the pH adjusting solvent good. By adjusting the pH range, it is possible to more uniformly control the size distribution of the supported transition metal catalyst. In this case, it is preferable that the pH adjusting solvent is added after adding the transition metal salt to completely dissolve and mix.
또한 상기 c) 단계에서 교반 및 분산에 의하여 전이금속 촉매는 g-C3N4@RGO 복합체에 담지되는데, 이 때 상기 분산은 초음파 분산을 이용할 수 있다.Also, in the step c), the transition metal catalyst is supported on the gC3 N4 @RGO composite by stirring and dispersion, wherein the dispersion can be performed by ultrasonic dispersion.
또한 상기 전이금속 염(metal salt)은 백금(Pt), 팔라듐(Pd), 구리(Au), 은(Ag), 니켈(Ni), 코발트(Co), 철(Fe), 주석(Sn), 로듐(Rh), 오스뮴(Os), 이리듐(Ir), 텅스텐(W), 루테듐(Ru), 및 티타늄(Ti) 및 바나듐(V) 중에서 선택된 1종 이상의 금속을 포함할 수 있고, 원자단, 또는 원자단의 혼합물 형태도 가능하며, 상기한 금속염에 한정되는 것이 아니라, 촉매가 사용되는 환경에 따라 적절한 활성을 가질 수 있는 금속염 중에서 선택할 수 있다.
The transition metal salt may be at least one selected from the group consisting of Pt, Pd, Au, Ag, Ni, Co, Fe, Sn, And may include at least one metal selected from rhodium (Rh), osmium (Os), iridium (Ir), tungsten (W), ruthenium (Ru), titanium (Ti), and vanadium (V) Or an atomic group, and it is not limited to the above-mentioned metal salt, but may be selected from metal salts which can have appropriate activity depending on the environment in which the catalyst is used.
이와 같이 본 발명의 방법에 따르면 그래핀 제조에 관한 화학적 박리법을 이용하여 환원된 그래핀 옥사이드를 제조하되, 탄소질화물과 복합체를 형성하도록 함으로써, 화학적 개질 및 물리적 결합에 의하여 상기 복합체가 촉매 담체로서 기능하고, 탄소질화물에 의한 촉매 활성이 향상됨은 물론 그래핀에 의하여 전기적 특성 등을 향상시킬 수 있다. 따라서 본 발명의 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체는 에너지 저장 소재로서 우수한 특성을 나타낼 수 있게 된다.As described above, according to the method of the present invention, the reduced graphene oxide is produced using a chemical stripping method related to the production of graphene, and by forming a complex with carbon nitride, by chemical modification and physical bonding, And the catalytic activity by the carbon nitride is improved, and the electrical characteristics and the like can be improved by graphene. Accordingly, the catalyst-graphitic carbon nitride-reduced graphene oxide composite of the present invention can exhibit excellent properties as an energy storage material.
따라서 상기 방법으로 제조되는 본 발명의 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체는 전극소재로서 활용가능하다.Therefore, the catalyst-graphitic carbon nitride-reduced graphene oxide composite of the present invention manufactured by the above method can be utilized as an electrode material.
이러한 본 발명의 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체를 커패시터 전극으로 이용하는 경우, 우수한 전기전도성 및 내구성을 가진 전극을 제공할 수 있게 된다. 이 경우 상기 커패시터 전극의 비축전 용량은 10~350 F/g, 바람직하게는 200~350 F/g이다. 즉, 본 발명에 따른 복합체를 이용한 커패시터 전극은 슈퍼 커패시터 전극으로서, 종래 화학적 박리법에 의하여 NaBH4로 환원제로 이용하여 제조되는 환원된 그래핀보다 우수한 전기전도성 및 내구성을 가진 전극을 제공할 수 있게 된다.When the catalyst-graphitic carbon nitride-reduced graphene oxide composite of the present invention is used as a capacitor electrode, it is possible to provide an electrode having excellent electrical conductivity and durability. In this case, the non-storage capacity of the capacitor electrode is 10 to 350 F / g, preferably 200 to 350 F / g. That is, the capacitor electrode using the composite according to the present invention can be used as a supercapacitor electrode and can provide an electrode having superior electrical conductivity and durability than reduced graphene produced by using NaBH4 as a reducing agent by a conventional chemical stripping method do.
또한 본 발명의 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체는 연료전지용 전극촉매로서 유용하게 활용될 수 있다.
Also, the catalyst-graphitic carbon nitride-reduced graphene oxide complex of the present invention can be usefully utilized as an electrode catalyst for fuel cells.
이하, 실시예를 들어 본 발명을 상세히 설명하기로 하나, 본 발명이 이에 한정되는 것은 아니다.
Hereinafter, the present invention will be described in detail with reference to examples, but the present invention is not limited thereto.
<<실시예Example 1> 백금-그래파이트형 1> Platinum-graphite type탄소질화물Carbon nitride-환원된- Reduced그래핀Grapina옥사이드Oxide(Pt/g-C(Pt / g-C33NN44@RGO) 복합체의 제조@RGO) composite
1-1 그래파이트1-1 graphite옥사이드의Oxide 제조 Produce
먼저, 500ml 삼각플라스크를 준비하고, 0~5℃ 상태에서 그래파이트(graphite, SP-1, Bay carbon사)와 NaNO3 (1g), H2SO4 (46ml)을 넣고 교반하여 잘 섞어주었다. 상기 용액에 KMnO4을 천천히 투입하고, 핫 플레이트(hot plate)를 이용하여 천천히 온도를 올려 주어 물 중탕(30℃~40℃)을 실시하였다. 그 후, 뜨거운 증류수(DI water)와 H2O2(5.2ml) 혼합용액을 추가로 투입하였다. 그 후, 감압 여과(vaccum filtration)후, 증류수(DI water)로 세척 하였다. 상기 세척된 용액을 충분히 초음파 분산(ultra sonication) 처리 후, 동결건조(lyophilization)하여, 그래파이트 옥사이드를 얻었다.
First, a 500 ml Erlenmeyer flask was prepared, and graphite (SP-1, Bay carbon), NaNO3 (1 g) and H2 SO4 (46 ml) were added at 0 to 5 ° C and stirred. KMnO4 was slowly added to the solution, and the temperature was slowly raised by using a hot plate to conduct a water bath (30 ° C to 40 ° C). Thereafter, a mixed solution of hot distilled water (DI water) and H2 O2 (5.2 ml) was further added. Then, after vacuum filtration, it was washed with distilled water (DI water). The washed solution was sufficiently subjected to ultra sonication treatment and then lyophilized to obtain graphite oxide.
1-2 그래파이트형1-2 graphite type탄소질화물Carbon nitride-환원된- Reduced그래핀Grapina옥사이드Oxide(g-C(g-C33NN44@RGO) 복합체의 제조@RGO) composite
상기 실시예 1-1에서 동결 건조된 그래파이트 옥사이드 0.2g를 용매 하에서 멜라민(2-amino-4,6-dichlorotriazine) 1.6g을 첨가하여 1시간 동안 초음파 처리 후. 환류장치를 이용하여 100℃에서 96시간 동안 수열 합성하여 g-C3N4@RGO 복합체를 제조하였다. 다음으로, 상기 제조된 g-C3N4@RGO 복합체를 석영 튜브 로(quartz tube furnance)을 이용하여, 200℃에서 30분 동안 열처리(annealing)하여 제조된 복합체를 안정화 시켰다.
0.2 g of the lyophilized graphite oxide in Example 1-1 was added with 1.6 g of melamine (2-amino-4,6-dichlorotriazine) in a solvent, and the mixture was ultrasonicated for 1 hour. GC3 N4 @RGO complex was prepared by hydrothermal synthesis at 100 ° C for 96 hours using a reflux condenser. Next, the thus-prepared gC3 N4 @RGO composite was annealed at 200 ° C for 30 minutes using a quartz tube furnace to stabilize the composite.
1-3 백금-그래파이트형1-3 Platinum - Graphite Type탄소질화물Carbon nitride-환원된- Reduced그래핀Grapina옥사이드Oxide(Pt/g-C(Pt / g-C33NN44@RGO) 복합체의 제조@RGO) composite
상기 실시예 1-2에서 제조된 g-C3N4@RGO 복합체(0.1g) 을 황산(H2SO4)과 질산(HNO3) 혼합용액에 넣고 교반(stirring) 하였다. 이를 감압 여과(vaccum filtration) 장치를 이용하여 상기 여과한 후, 증류수로 여러 번 세척하고, g-C3N4@RGO 복합체와 백금 전구체인 H2PtCl66H2O를 증류수 하에서 초음파 분산 하였다. 이 후, 상기 g-C3N4@RGO 복합체에 에틸렌 글라이콜(Ethylene glycol)용액을 넣고 NaOH를 넣어 pH를 11으로 조절하고, 약 135℃에서 4시간 30분 동안 환류(reflux)장치를 이용해서 교반하였다. 이 후, 약 60℃정도까지 식혀서 감압여과(vaccum filtration) 후 세척하고, 세척이 완료된 시료를 동결건조(lyophilization)하여 시료를 얻었다. 최종적으로 얻은 촉매를 Pt/g-C3N4@RGO로 명명하였다.
The gC3 N4 @RGO complex (0.1 g) prepared in Example 1-2 was added to a mixed solution of sulfuric acid (H2 SO4 ) and nitric acid (HNO3 ) and stirred. The filtrate was washed with distilled water several times, and gC3 N4 @RGO complex and H2 PtCl6 6H2 O, a platinum precursor, were ultrasonically dispersed in distilled water. Ethylene glycol solution was then added to the gC3 N4 @RGO complex, the pH was adjusted to 11 by adding NaOH, and the solution was refluxed for 4 hours and 30 minutes at about 135 ° C. Lt; / RTI > Thereafter, the sample was cooled to about 60 ° C, washed with vacuum filtration, and lyophilized to obtain a sample. The finally obtained catalyst was named Pt / gC3 N4 @RGO.
<<비교예Comparative Example 1> 환원된 1> Reduced그래핀Grapina옥사이드(RGO)의Oxide (RGO) 제조 Produce
먼저, 상기 실시예 1-1에 기재된 방법과 동일한 방법으로, 그래파이트 옥사이드를 제조하였다. 상기 그래파이트 옥사이드(0.1g)를 환원제인 수소화붕소나트륨(NaBH4) 1.87g과 증류수(DI-water) 30ml을 드로핑 깔때기(dropping fannel)을 사용하여 넣고 천천히 투입하고 90℃에서 2시간 동안 교반하여 환원된 그래핀 옥사이드(RGO)을 제조하였다.
First, graphite oxide was prepared by the same method as described in Example 1-1 above. 1.87 g of sodium borohydride (NaBH4 ) and 30 ml of distilled water (DI-water) were added to the graphite oxide (0.1 g) using a dropping funnel and stirred at 90 ° C for 2 hours Reduced graphene oxide (RGO) was prepared.
<<비교예Comparative Example 2> 백금이 2> Platinum담지된Supported 환원된 Reduced그래핀Grapina옥사이드의Oxide 제조(Pt/ Manufacturing (Pt /RGORGO))
상기 g-C3N4@RGO 복합체 대신, 상기 비교예 1에서 제조된 방법으로 환원된 그래핀 옥사이드를 이용하는 것을 제외하고는 상기 실시예 1-3에 기재된 방법과 동일한 방법으로 백금이 담지된 환원된 그래핀 옥사이드(Pt/RGO)를 제조하였다.
The procedure of Example 1-3 was repeated except that the gC3 N4 @RGO composite was replaced with the graphene oxide prepared by the method of Comparative Example 1, Pin oxide (Pt / RGO).
<<비교예Comparative Example 3> 백금이 3> Platinum담지된Supported그라파이트의Graphite 제조 (Pt/ Manufacturing (Pt /GrGr))
Bay carbon에서 구입한 그래파이트(graphite, SP-1)를 아무 처리 하지 않고 준비하였다. 다음으로, 상기 g-C3N4@RGO 복합체 대신, 상기 준비한 그래파이트를 이용하는 것을 제외하고는 상기 실시예 1-3에 기재된 방법과 동일한 방법으로 백금이 담지된 그래파이트(Pt/Gr)를 제조하였다.
Graphite (SP-1) purchased from Bay carbon was prepared without any treatment. Next, platinum-supported graphite (Pt / Gr) was prepared in the same manner as in Example 1-3, except that the prepared graphite was used in place of the gC3 N4 @RGO composite.
<<분석예Analysis example> 평가 및 분석> Evaluation and Analysis
상기 실시예 및 비교예에 의하여 제조된 물질에 대한 구조적, 전기화학적 성능을 평가 및 분석하였다.
Structural and electrochemical performances of the materials prepared by the above Examples and Comparative Examples were evaluated and analyzed.
1-11-1SEMSEM 분석 analysis
상기 실시예 1-2에서 제조된 g-C3N4@RGO 복합체와, 상기 비교예 1에서 제조된 RGO의 표면을 관찰하기 위하여, 주사 현미경(Scanning Electron Microscope, SEM)으로 측정하고 그 결과를 도 3에 나타내었다. 분석에 이용된 장비는 Hitachi사의 S-3500N 모델을 이용하였다.The surface of the gC3 N4 @RGO composite prepared in Example 1-2 and the surface of RGO prepared in Comparative Example 1 was measured by a scanning electron microscope (SEM). The results are shown in FIG. 3 Respectively. The equipment used for the analysis was Hitachi's S-3500N model.
도 3을 참조하면, 시트형 구조의 RGO와는 달리, g-C3N4@RGO 복합체는 그래핀 시트에 그래파이트형 탄소질화물이 붙어 있는 구조 형태인 것을 확인할 수 있다.
Referring to FIG. 3, it can be seen that the gC3 N4 @RGO composite unlike the RGO of the sheet-like structure has a structure in which graphite-type carbon nitride is attached to the graphene sheet.
1-21-2EDAXEDAX 분석 analysis
상기 실시예 1-2에서 제조된 g-C3N4@RGO 복합체 시편의 원소의 성분을 분석하기 위하여 에너지 분산형 X선 분석장치(Energy Dispersive X-ray microanalysis, EDAX)으로 측정하고 그 결과를 도 4에 나타내었다. 분석에 이용된 장비는 EDAX를 장착한 Hitachi사의 S-4700 모델을 이용하였다.The components of the gC3 N4 @RGO composite specimen prepared in Example 1-2 were analyzed by Energy Dispersive X-ray microanalysis (EDAX). The results are shown in FIG. 4 Respectively. The equipment used for the analysis was Hitachi's S-4700 model equipped with EDAX.
도 4를 참조하면, 상기 실시예 1-2에서 제조된 g-C3N4@RGO 복합체의 표면에 질소의 존재를 통해 그래파이트형 탄소질화물이 고르게 분포하고 있음을 확인할 수 있다.
Referring to FIG. 4, graphite-type carbon nitride is uniformly distributed on the surface of the gC3 N4 @RGO composite prepared in Example 1-2 through the presence of nitrogen.
1-3 FT-IR 분석1-3 FT-IR analysis
상기 실시예 1-2에서 제조된 g-C3N4@RGO 복합체 시편 및 비교예 1에서 제조된 RGO 시편의 구조를 분석하기 위하여 푸리에변환 적외선흡수 분광법(Fourier Transform Infrared Spectroscopy, FT-IR)으로 측정하고 그 결과를 도 5에 나타내었다. 분석에 이용된 장비는 perkinElmer사의 NEW FT-IR Spectrum Two 모델을 이용하였다.The structure of the gC3 N4 @RGO composite specimen prepared in Example 1-2 and the structure of the RGO specimen prepared in Comparative Example 1 were measured by Fourier Transform Infrared Spectroscopy (FT-IR) The results are shown in Fig. The instrument used for the analysis was a NEW FT-IR Spectrum Two model from perkinElmer.
도 5를 참조하면, 상기 실시예 1-2에서 제조된 g-C3N4@RGO 복합체의 표면상에는 그래파이트 옥사이드의 하이드록시기(hydroxyl, broad peak 2600~3468cm-1,-OH)기의 피크(Peak)가 사라지고, C=N (1571,1630 cm-1), C-N (1255,1323,1428 cm-1), CN-heterocycle (809 cm-1), NH2(broad peak 3150~3500 cm-1)그룹이 생성된 것을 확인할 수 있다.Referring to FIG. 5, on the surface of the gC3 N4 @RGO composite prepared in Example 1-2, peaks of hydroxyl group (hydroxyl, broad peak 2600 to 3468 cm-1 , -OH) group of graphite oxide )disappears, C = N (1571,1630 cm -1 ), CN (1255,1323,1428 cm -1), CN-heterocycle (809 cm -1), NH 2 (broad peak 3150 ~ 3500 cm-1 ) group was generated.
또한, 상기 비교예 1에서 제조된 RGO의 표면상에는 하이드록시기(hydroxyl, broad 2600~3468cm-1, -OH), 알킬기(alkyl, 2860, 2922 cm-1, -CH2), C=C (1548 or 1623 cm-1) 및 카르복실기(Carboxyl, 1720cm-1(C=O), 1370cm-1(C-O) , 1225cm-1(-OH), COOH)그룹이 존재함을 확인할 수 있다.On the surface of the RGO prepared in Comparative Example 1, a hydroxyl group (hydroxyl, broad 2600 to 3468 cm-1 , -OH), an alkyl group (alkyl, 2860, 2922 cm-1 , -CH2 ) 1548 or 1623 cm-1) and a carboxyl group(carboxyl, 1720cm -1 (C = O), 1370cm -1 (CO), 1225cm -1 (-OH), COOH) can be confirmed that the group is present.
또한, 멜라민은 아민기(amine, broad peak 3150~3500 cm-1,-NH2 or =NH), C=N(1571, 1630 cm-1), C-N(1255, 1323, 1428 cm-1) 및 CN 헤테로사이클( 809 cm-1) 확인할 수 있다.
In addition, the melamine has an amine group (broad peak 3150-3500 cm-1 , -NH2 or = NH), C = N (1571, 1630 cm-1 ), CN (1255, 1323, 1428 cm-1 ) CN Heterocycle (809 cm-1 ) can be confirmed.
1-41-4TEMTEM 분석 analysis
상기 실시예 1-3에서 제조된 Pt/g-C3N4@RGO 복합체 시편 및 비교예 2에서 제조된 Pt/RGO 시편의 구조와, 담지된 Pt 입자의 분포 및 크기를 분석하기 위하여, 투과전자현미경(Transmission electron mictroscopy, TEM)으로 측정하고 그 결과를 도 6에 나타내었다. 분석에 이용된 장비는 Jeol사의 JEM-2100F모델을 이용하였다.In order to analyze the structure of the Pt / gC3 N4 @RGO composite specimen prepared in Example 1-3 and the Pt / RGO specimen prepared in Comparative Example 2 and the distribution and size of the supported Pt particles, a transmission electron microscope (Transmission electron microscopy, TEM). The results are shown in Fig. The equipment used for the analysis was Jeol's JEM-2100F model.
도 6을 참고하면, 상기 실시예 1-3에서 제조된 Pt/g-C3N4@RGO 복합체가, 비교예 2에서 제조된 Pt/RGO에 비하여 보다 작은 Pt 입자가 더 균일하게 분포되어 있음을 확인할 수 있다. 또한, 평균 입도를 각각 구하면 실시예 1-3에서 제조된 Pt/g-C3N4@RGO의 경우 1.5 내지 2.5 nm의 분포를 가지고, 비교예 2에서 제조된 Pt/RGO의 경우 2.5 내지 4.0 nm의 분포를 가지는 것으로 관찰되었다. 이로써 본 발명의 실시예에 의할 경우 보다 더 작은 입자 크기를 가질 수 있어, 본 발명의 제조방법이 입자크기를 제어할 수 있음을 확인할 수 있다.
6, it can be seen that the Pt / gC3 N4 @RGO composite prepared in Example 1-3 had smaller Pt particles distributed more uniformly than Pt / RGO prepared in Comparative Example 2 . The average particle size was found to be 1.5 to 2.5 nm in the case of Pt / gC3 N4 @RGO prepared in Example 1-3, and 2.5 to 4.0 nm in the case of Pt / RGO prepared in Comparative Example 2 Distribution. Thus, it can be seen that the method of the present invention can control the particle size because it can have a smaller particle size than the case of the embodiment of the present invention.
1-5 정전용량(Capacitance) 측정1-5 Measuring Capacitance
상기 실시예 1-2에서 제조된 g-C3N4@RGO 복합체 시편 및 비교예 1에서 제조된 RGO 시편을, Cyclic Voltammetry(CV)를 이용하여 정전용량(Capacitance)을 측정하고 그 결과를 도 7 및 도 8에 나타내었다. 분석을 위해 Potentiostat사의 IVIUMSTAT를 이용하였고 3전극(Three-electrode)방법으로 측정하였다.The capacitance of the gC3 N4 @RGO composite specimen prepared in Example 1-2 and the RGO specimen prepared in Comparative Example 1 were measured using a cyclic voltammetry (CV) 8. For analysis, IVIUMSTAT from Potentiostat was used and measured by a three-electrode method.
구체적으로, 작업전극(working electrode)은 상기 실시예 1-2 및 비교예 1에서 제조된 시편과 도전재(Super-P), 바인더 폴리비닐리덴다이플로라이드(PVDF, Aldrich社)를 각각 무게 비 (85:10:5)로 준비하여 N-methyl pyrrolidinone(NMP)에 녹였다. NMP로 슬러리의 점도를 조절 한 후, 니켈폼(Nickel foam)에 스파츄라(plastic spatula)를 이용하여 균일하게 코팅하였다. 코팅된 니켈폼을 100℃ 오븐에서 12시간 동안 건조시킨 후 압축기(Roll presser)를 이용하여 압축하였다. 상대전극(Counter electrode)은 백금 전극(Pt wire)를 사용하였으며, 기준전극(reference electrode)은 포화 칼로멜 전극(Saturated calomel electrode, SCE)을 이용하여 전압범위 -0.8~0.2V의 영역에서 10, 20, 50, 100, 200, 300 mV/s의 주사속도(scan rate)로 측정 하였다. 이 때 전해질(electrolyte)은 6 M의 수산화 칼륨(KOH)를 사용하였다.Specifically, a working electrode was prepared by mixing the specimen, the conductive material (Super-P) and the binder polyvinylidene difluoride (PVDF, Aldrich) prepared in Example 1-2 and Comparative Example 1, (85: 10: 5) and dissolved in N-methyl pyrrolidinone (NMP). The viscosity of the slurry was adjusted with NMP and uniformly coated on a nickel foam with a plastic spatula. The coated nickel foam was dried in an oven at 100 ° C. for 12 hours and then compressed using a roll press. The counter electrode was a platinum wire and the reference electrode was 10 and 20 volts in a voltage range of -0.8 to 0.2 V using a saturated calomel electrode (SCE) , And scan rates of 50, 100, 200, and 300 mV / s. At this time, 6 M of potassium hydroxide (KOH) was used as the electrolyte.
도 7 및 도 8을 참고하면, 주사속도(Scan rate)에 변화에 따른 CV 특성을 평가한 결과 전기이중층 커패시터(EDLCs) 특성인 사각형(rectangular)의 곡선을 가지는 용량성 거동(capacitative behavior)을 보이는 것으로 나타났다. 또한, Specific Current[A/g]는 주사속도에 비례하여 증가하였다.하지만, g-C3N4@RGO인 경우가 RGO보다 주사속도가 증가해도 전기이중층 커패시터(EDLCs) 특성인 사각형(rectangular)의 곡선을 가지는 용량성 거동을 나타낼 뿐만 아니라, 축전용량도 높음을 알 수 있다.Referring to FIGS. 7 and 8, a CV characteristic according to a change in scan rate is evaluated. As a result, a capacitive behavior having a rectangular curved line characteristic of electric double layer capacitors (EDLCs) Respectively. Also, Specific Current [A / g] increased in proportion to the scanning speed. However, in the case of gC3 N4 @RGO, not only the capacitive behavior with rectangular curves characteristic of electric double layer capacitors (EDLCs), but also the capacitance is high even if the scanning speed is higher than RGO .
상기 CV 시험 결과 값을 통해 비축전 용량(specific capacitance [F/g]) 값을 확인 할 수 있는데, 하기 식에 따라 측정된다. (I는 전류밀도(current density, A cm-2), ν는 포텐셜주사속도(potential scan rate,V s-1), ΔV는 전압범위, m은 활물질의 양(g cm-2))The value of the specific capacitance [F / g] can be confirmed through the CV test result, which is measured according to the following equation. V is the voltage range, m is the amount of the active material (g cm-2 ), and V is the current density (A cm-2 ), where V is the potential scan rate (V s-1 )
또한 도 9에서, 비정전 용량(Specific Capacitance[F/g])은 전류밀도에 비례하고 주사속도에 반비례 하는 것으로 나타났고, 상기 실시예 1-2에서 제조된 g-C3N4@RGO 복합체의 경우, 비교예 1에 따른 RGO는 각각 비축전 용량에 비하여 현저하게 비축전 용량이 향상됨을 확인할 수 있다.
9, the specific capacitance [F / g]) was found to be proportional to the current density and inversely proportional to the scanning speed. In the case of the gC3 N4 @RGO composite prepared in Example 1-2, It can be confirmed that the RGO according to Comparative Example 1 has remarkably improved non-storage capacity as compared with the non-storage capacity.
1-6 전기화학적 특성 및1-6 Electrochemical properties and비표면적Specific surface area 측정 Measure
상기 실시예 1-3에서 제조된 Pt/g-C3N4@RGO 복합체 시편 및 비교예 2, 3에서 제조된 Pt/RGO, Pt/G 시편 및 시판하는 Pt/C 시편을 Cyclic Voltammetry(CV)를 이용하여 전기화학적 표면적(electrochemical surface area, ECSA)을 측정하였다. 전기화학적 표면적(ECSA)은 백금 결정 위에 단일층으로 흡착된 수소의 흡착 전하(0.21 mC/cm2)를 토대로, 담지 전해질(1.0M H2SO4)에서 평형 사이클릭 볼타모그램(cyclic voltammograms)의 수소 흡착 영역의 총 전하량으로부터 계산할 수 있다. 분석을 위해 Potentiostat사의 IVIUMSTAT를 이용하였고 3전극(Three-electrode)방법을 사용하였다. 또한 상기 전기화학적 표면적(electrochemical surface area, ECSA)은 백금에 기초한 촉매의 고유 전기화학적 활성을 측정하는데 중요한 인자로, 상기 제조된 촉매를 이용하여 촉매 잉크를 제조한 후, 이를 유리질 카본(glassy carbon, 0.07cm)에 도포하여 작업전극을 제조하였고, 백금 와이어(pt wire)을 상대전극, Ag/AgCl를 기준전극, 1M의 황산(H2SO4)수용액을 전해질 사용하여 50mV s-1의 주사속도(scan rate)로 CV(cyclic voltammetry)측정을 수행하였다. 상기 결과는 도 10에 나타내었다. 네거티브 방향 포텐셜 스캔에서 +0.1 내지 -0.25 V에서 강한 피크가 나타는데 이는 결합된 흡착수소를 나타낸다. 각 시료에 대한 전기화학적 표면적(ECSA)은 백금에 대하여 각각 Pt/g-C3N4@RGO (81.5 m2g-1), Pt/RGO (51.1 m2g-1), Pt/C (42.3 m2g-1), 및 Pt/Gr(35.2 m2g-1)으로 측정되어 Pt/g-C3N4@RGO에서 가장 높은 전기화학적 표면적을 나타내었다.
The Pt / gC3 N4 @RGO composite specimen prepared in Example 1-3 and the Pt / RGO, Pt / G specimen and commercially available Pt / C specimen prepared in Comparative Examples 2 and 3 were subjected to cyclic voltammetry (CV) The electrochemical surface area (ECSA) was measured by using an electrochemical cell. The electrochemical surface area (ECSA) was calculated from the equilibrium cyclic voltammograms of the supported electrolyte (1.0 MH2 SO4 ), based on the adsorption charge (0.21 mC / cm2 ) Can be calculated from the total amount of charge in the hydrogen adsorption region. For analysis, IVIUMSTAT from Potentiostat was used and a three-electrode method was used. In addition, the electrochemical surface area (ECSA) is an important factor for measuring the intrinsic electrochemical activity of a catalyst based on platinum. The catalytic ink is prepared using the catalyst, 0.07 cm) to prepare a working electrode. Using a platinum wire as a counter electrode, Ag / AgCl as a reference electrode, and 1 M aqueous solution of sulfuric acid (H2 SO4 ) as an electrolyte, a scanning speed of 50 mV s-1 (cyclic voltammetry) measurement was performed at a scan rate. The results are shown in FIG. A strong peak appears at +0.1 to -0.25 V in the negative directional potential scan, indicating bound adsorbed hydrogen. The electrochemical surface area (ECSA) for each sample was Pt / gC3 N4 @RGO (81.5 m2 g-1 ), Pt / RGO (51.1 m2 g-1 ), Pt / C2 g-1 ) and Pt / Gr (35.2 m2 g-1 ), indicating the highest electrochemical surface area in Pt / gC3 N4 @RGO.
이상에서 살펴본 바와 같이, 본 발명에 따른 Pt/g-C3N4@RGO 복합체는 그래핀 옥사이드를 주형으로 이용하면서 탄소질화물이 C3N4 네트워크를 형성하면서 결합되도록 하여 복합체를 형성하고 여기에 전이금속 촉매를 담지함으로써 촉매의 활성을 향상시킴은 물론, 기계적, 전기적 물성을 향상시킬 수 있어 우수한 에너지 저장소재로서 적용될 수 있게 된다.
As described above, the Pt / gC3 N4 @RGO composite according to the present invention forms a complex by allowing carbon nitride to form a C3N4 network while using graphene oxide as a template to support a transition metal catalyst Thereby improving the activity of the catalyst and, at the same time, improving the mechanical and electrical properties of the catalyst.
Claims (13)
Translated fromKorean2) 상기 현탁액에 탄소질화물 전구체를 첨가한 후 수열합성으로 그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체(g-C3N4@RGO)를 제조하는 단계; 및
3) 상기 복합체를 폴리올 용매에 분산시킨 후, 전이금속염을 첨가하여 혼합하고 교반함으로써, 전이금속 촉매를 담지하는 단계;를 포함하며,
상기 1)단계에서 제조된 현탁액은, 하이드록시기, 카르복실기 및 에폭시기 중에서 선택된 1종 이상의 작용기를 포함하는 그래파이트옥사이드를 포함하고; 상기 2)단계의 탄소질화물 전구체는 염화시아누르(C3Cl3N3), 멜라민(C3H6N6), 멜렘 (C3H6N10) 및 멜람(C6H9N11) 중에서 선택된 1종 이상이고;
상기 3)단계는,
a) 상기 2)단계에서 제조된 g-C3N4@RGO 복합체를 표면개질하는 단계와, b) 상기 표면 개질된 복합체를 폴리올 용매에 분산시키고, 전이금속염을 더 첨가하여 혼합하는 단계, 및 c) 상기 b)단계 혼합액의 pH를 9~11로 조절한 후, 교반 및 분산함으로써 상기 표면개질된 복합체에 전이금속 촉매를 담지하는 단계를 포함하는 것을 특징으로 하는, 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법.
1) dispersing the lyophilized graphite oxide in distilled water to prepare a graphene oxide suspension;
2) preparing a graphite-type carbon nitride-reduced graphene oxide complex (gC3 N4 @RGO) by hydrothermal synthesis after adding a carbon nitride precursor to the suspension; And
3) dispersing the composite in a polyol solvent, adding a transition metal salt, mixing and stirring, and carrying the transition metal catalyst,
The suspension prepared in the step 1) comprises graphite oxide containing at least one functional group selected from a hydroxyl group, a carboxyl group and an epoxy group; The carbon nitride precursor in the step 2) is selected from the group consisting of cyanuric chloride (C3 Cl3 N3 ), melamine (C3 H6 N6 ), melem (C3 H6 N10 ), and melam (C6 H9 N11 ) ≪ / RTI >
The step (3)
a) modifying the surface of the gC3 N4 @RGO composite prepared in step 2), b) dispersing the surface modified complex in a polyol solvent, further adding a transition metal salt and mixing, and c) The method comprising: controlling the pH of the mixed solution of the step b) to 9 to 11, and then carrying the transition metal catalyst on the surface-modified composite by stirring and dispersing the catalyst. The catalyst-graphitic carbon nitride- / RTI > oxide.
상기 2)단계의 탄소질화물 전구체는 멜라민이고; 상기 멜라민과 그래파이트옥사이드의 중량비는 1: 5~20인 것을 특징으로 하는, 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법.
The method according to claim 1,
The carbon nitride precursor in step 2) is melamine; Wherein the weight ratio of the melamine to the graphite oxide is 1: 5 to 20. The method of claim 1, wherein the weight ratio of the graphite oxide to the graphite oxide is 1: 5 to 20.
상기 2)단계는, 수열합성으로 g-C3N4@RGO 복합체를 제조한 후, 열처리하여 상기 g-C3N4@RGO 복합체를 안정화하는 것을 특징으로 하는, 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법.
The method according to claim 1,
In the step 2), the gC3 N4 @RGO composite is prepared by hydrothermal synthesis, and then the gC3 N4 @RGO composite is heat treated to stabilize the gC3 N4 @RGO composite. Oxide complex.
상기 수열합성은 90~110℃의 온도로 48~120시간 동안 수행하고; 상기 열처리는 100~300℃의 온도로 5~30분간 수행하는 것을 특징으로 하는, 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법.
5. The method of claim 4,
The hydrothermal synthesis is carried out at a temperature of 90 to 110 캜 for 48 to 120 hours; Wherein the heat treatment is performed at a temperature of 100 to 300 DEG C for 5 to 30 minutes.
상기 표면개질은 H2SO4, HNO3 및 P2O5 중에서 선택되는 적어도 하나 이상의 산화제를 이용하여 수행되는 것을 특징으로 하는, 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법.
The method according to claim 1,
Wherein the surface modification is performed using at least one oxidizing agent selected from H2 SO4 , HNO3 and P2 O5 .
상기 3)단계의 폴리올 용매는 에틸렌글리콜(Ethylene Glycol), 디에틸렌글리콜(Diethylene Glycol), 트리에틸렌글리콜(Triethylene Glycol) 및 테트라에틸렌글리콜(Tetraethylene Glycol)로 이루어진 군에서 선택된 1종 이상인 것을 특징으로 하는, 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법.
The method according to claim 1,
The polyol solvent in the step 3) is at least one selected from the group consisting of ethylene glycol, diethylene glycol, triethylene glycol, and tetraethylene glycol. , A process for producing a catalyst-graphitic carbon nitride-reduced graphene oxide complex.
상기 전이금속염은, 백금(Pt), 팔라듐(Pd), 구리(Au), 은(Ag), 니켈(Ni), 코발트(Co), 철(Fe), 주석(Sn), 로듐(Rh), 오스뮴(Os), 이리듐(Ir), 텅스텐(W), 루테듐(Ru), 및 티타늄(Ti) 및 바나듐(V) 중에서 선택된 1종 이상의 금속을 포함하는 것을 특징으로 하는, 촉매-그래파이트형 탄소질화물-환원된 그래핀 옥사이드 복합체의 제조방법.
The method according to claim 1,
The transition metal salt may be at least one selected from the group consisting of Pt, Pd, Au, Ag, Ni, Co, Fe, Sn, Rh, Characterized in that it comprises at least one metal selected from the group consisting of osmium (Os), iridium (Ir), tungsten (W), ruthenium (Ru), titanium (Ti) and vanadium Lt; RTI ID = 0.0 > of a nitride-reduced graphene oxide complex.
A catalyst-graphitic carbon nitride-reduced graphene oxide composite prepared according to any one of claims 1, 3 to 5, 7 to 9.
An electrode produced using the catalyst-graphitic carbon nitride-reduced graphene oxide complex according to claim 10.
A fuel cell produced using the electrode according to claim 11.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020150043552AKR101640545B1 (en) | 2015-03-27 | 2015-03-27 | Production method of catalyst-graphitic carbon nitride-reduced graphene oxide composite, the composite produced thereby, and an electrode using the same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020150043552AKR101640545B1 (en) | 2015-03-27 | 2015-03-27 | Production method of catalyst-graphitic carbon nitride-reduced graphene oxide composite, the composite produced thereby, and an electrode using the same |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR101640545B1true KR101640545B1 (en) | 2016-07-18 |
Family
ID=56679834
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020150043552AExpired - Fee RelatedKR101640545B1 (en) | 2015-03-27 | 2015-03-27 | Production method of catalyst-graphitic carbon nitride-reduced graphene oxide composite, the composite produced thereby, and an electrode using the same |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR101640545B1 (en) |
Cited By (27)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101775468B1 (en) | 2016-09-30 | 2017-09-06 | 전북대학교산학협력단 | Electrode for the super capacitor and method of the same |
| CN107297217A (en)* | 2017-06-01 | 2017-10-27 | 西安交通大学 | A kind of thin porous layer graphite phase carbon nitride loaded platinum photo catalyst and its preparation method and application |
| CN108624195A (en)* | 2018-06-07 | 2018-10-09 | 西南石油大学 | A kind of g-C3N4The preparation method of-G/ water-base epoxy composite coatings |
| CN109078648A (en)* | 2018-08-01 | 2018-12-25 | 天津大学 | A kind of preparation method of three-dimensional grapheme/nickel/graphite phase carbon nitride composite photocatalyst material |
| WO2019070844A1 (en)* | 2017-10-05 | 2019-04-11 | The Regents Of The University Of California | Catalysis of hydrogen evolution reaction using ruthenium ion complexed carbon nitride materials |
| CN110143578A (en)* | 2019-04-19 | 2019-08-20 | 南通途纳新材料有限公司 | The preparation method of graphite phase carbon nitride |
| KR20200006164A (en)* | 2020-01-10 | 2020-01-17 | 한국원자력연구원 | Reduced graphene, reduced graphene oxide-funtional material complex and production methods thereof |
| CN111071999A (en)* | 2019-11-20 | 2020-04-28 | 嘉兴学院 | A kind of synthesis method of low metal content, mesoporous graphitic carbon nitride nanosheets |
| CN111564321A (en)* | 2020-05-27 | 2020-08-21 | 新昌县易纵新材料科技有限公司 | Tin oxide-modified g-C3N4Electrode material of super capacitor and preparation method thereof |
| US10804538B2 (en) | 2016-06-08 | 2020-10-13 | Lg Chem, Ltd. | Self-assembled composite of carbon nitride and graphene oxide, manufacturing method for same, positive electrode having same applied thereto, and lithium-sulfur battery comprising same |
| KR102166566B1 (en)* | 2019-04-08 | 2020-10-19 | 주식회사 씨에스이노베이션 | Carbon electrode for electro-polishing and the method for preparing the same |
| KR20200120281A (en)* | 2019-04-12 | 2020-10-21 | 서울대학교산학협력단 | Carbon nitride having surface modified with diazonium salt and organic light emitting display device comprising the same |
| CN112264100A (en)* | 2020-10-20 | 2021-01-26 | 广州维港环保科技有限公司 | Bifunctional graphene oxide catalyst, and preparation method and application thereof |
| CN112349921A (en)* | 2020-11-17 | 2021-02-09 | 浙江理工大学 | Nitrogen-doped graphene hollow sphere catalyst, preparation method and application |
| CN112397728A (en)* | 2020-11-24 | 2021-02-23 | 上海纳米技术及应用国家工程研究中心有限公司 | Preparation method of Co and Fe element modified graphite-phase carbon nitride and graphene oxide fuel cell cathode catalyst |
| CN113087970A (en)* | 2020-01-08 | 2021-07-09 | 中国石油化工股份有限公司 | Halogen-free flame retardant and application thereof in preparation of halogen-free flame retardant PA6 |
| CN113444558A (en)* | 2021-05-26 | 2021-09-28 | 无锡烯创科技有限公司 | Organic modification method for improving dispersibility of graphite-phase carbon nitride in lubricating oil |
| CN113764684A (en)* | 2021-08-17 | 2021-12-07 | 上海纳米技术及应用国家工程研究中心有限公司 | Preparation method of fuel cell cathode catalyst material |
| CN114709388A (en)* | 2022-02-17 | 2022-07-05 | 山东科技大学 | Preparation method and application of graphite and melamine co-modified micron SiOx negative electrode material |
| KR20220116982A (en)* | 2021-02-16 | 2022-08-23 | 부산대학교 산학협력단 | Manufacturing method of noble metal-free catalysts for water electrolysis |
| US11539054B2 (en) | 2020-03-13 | 2022-12-27 | Hyundai Motor Company | Method of manufacturing catalyst ink free of eluted transition metal for fuel cell |
| CN115945205A (en)* | 2022-09-30 | 2023-04-11 | 江汉大学 | Preparation method and application of a graphitic carbon nitride material with enhanced photocatalytic performance |
| WO2024036756A1 (en)* | 2022-08-19 | 2024-02-22 | 台州学院 | Multifunctional phosphorus and nickel doped graphite-like carbon nitride nanosheet, preparation method therefor, and abs material |
| KR102639923B1 (en)* | 2022-11-14 | 2024-02-22 | 한국세라믹기술원 | Manufacturing method of nitrogen doped electrode active material with reduced chemical amount by using surface modifier, and supercapacitor using the same and method of manufacturing thereof |
| KR20240060993A (en)* | 2022-10-31 | 2024-05-08 | 경상국립대학교산학협력단 | Composition for sintering ceramic and manufacturing method thereof, zirconia sintered body using thereof and manufacturing method thereof |
| CN118637720A (en)* | 2024-08-16 | 2024-09-13 | 成都瀚川环境科技有限公司 | A method for eliminating organic matter in water by electrochemically activating sulfite |
| CN119447221A (en)* | 2024-09-24 | 2025-02-14 | 合肥国轩高科动力能源有限公司 | A phosphorus-carbon-silver composite material and its preparation method and application |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20130079735A (en)* | 2012-01-03 | 2013-07-11 | 부산대학교 산학협력단 | Method of manufacturing graphene/metal oxide nanocomposites through microwaved-assisted synthesis |
| KR20140004372A (en)* | 2012-07-02 | 2014-01-13 | 이화여자대학교 산학협력단 | Metal-graphene-layered metal oxide porous nanocomposites, preparation method thereof, and electrode catalyst comprising the same |
- 2015
- 2015-03-27KRKR1020150043552Apatent/KR101640545B1/ennot_activeExpired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20130079735A (en)* | 2012-01-03 | 2013-07-11 | 부산대학교 산학협력단 | Method of manufacturing graphene/metal oxide nanocomposites through microwaved-assisted synthesis |
| KR20140004372A (en)* | 2012-07-02 | 2014-01-13 | 이화여자대학교 산학협력단 | Metal-graphene-layered metal oxide porous nanocomposites, preparation method thereof, and electrode catalyst comprising the same |
Cited By (40)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10804538B2 (en) | 2016-06-08 | 2020-10-13 | Lg Chem, Ltd. | Self-assembled composite of carbon nitride and graphene oxide, manufacturing method for same, positive electrode having same applied thereto, and lithium-sulfur battery comprising same |
| KR101775468B1 (en) | 2016-09-30 | 2017-09-06 | 전북대학교산학협력단 | Electrode for the super capacitor and method of the same |
| CN107297217B (en)* | 2017-06-01 | 2020-04-28 | 西安交通大学 | Porous thin-layer graphite-phase carbon nitride-supported platinum photocatalyst and preparation method and application thereof |
| CN107297217A (en)* | 2017-06-01 | 2017-10-27 | 西安交通大学 | A kind of thin porous layer graphite phase carbon nitride loaded platinum photo catalyst and its preparation method and application |
| US11674232B2 (en) | 2017-10-05 | 2023-06-13 | The Regents Of The University Of California | Catalysis of hydrogen evolution reaction using ruthenium ion complexed carbon nitride materials |
| WO2019070844A1 (en)* | 2017-10-05 | 2019-04-11 | The Regents Of The University Of California | Catalysis of hydrogen evolution reaction using ruthenium ion complexed carbon nitride materials |
| US11352704B2 (en) | 2017-10-05 | 2022-06-07 | The Regents Of The University Of California | Catalysis of hydrogen evolution reaction using ruthenium ion complexed carbon nitride materials |
| CN108624195A (en)* | 2018-06-07 | 2018-10-09 | 西南石油大学 | A kind of g-C3N4The preparation method of-G/ water-base epoxy composite coatings |
| CN109078648A (en)* | 2018-08-01 | 2018-12-25 | 天津大学 | A kind of preparation method of three-dimensional grapheme/nickel/graphite phase carbon nitride composite photocatalyst material |
| KR102166566B1 (en)* | 2019-04-08 | 2020-10-19 | 주식회사 씨에스이노베이션 | Carbon electrode for electro-polishing and the method for preparing the same |
| KR20200120281A (en)* | 2019-04-12 | 2020-10-21 | 서울대학교산학협력단 | Carbon nitride having surface modified with diazonium salt and organic light emitting display device comprising the same |
| KR102192611B1 (en)* | 2019-04-12 | 2020-12-17 | 서울대학교산학협력단 | Carbon nitride having surface modified with diazonium salt and organic light emitting display device comprising the same |
| CN110143578B (en)* | 2019-04-19 | 2022-09-23 | 南通途纳新材料有限公司 | Preparation method of graphite phase carbon nitride |
| CN110143578A (en)* | 2019-04-19 | 2019-08-20 | 南通途纳新材料有限公司 | The preparation method of graphite phase carbon nitride |
| CN111071999A (en)* | 2019-11-20 | 2020-04-28 | 嘉兴学院 | A kind of synthesis method of low metal content, mesoporous graphitic carbon nitride nanosheets |
| CN113087970A (en)* | 2020-01-08 | 2021-07-09 | 中国石油化工股份有限公司 | Halogen-free flame retardant and application thereof in preparation of halogen-free flame retardant PA6 |
| CN113087970B (en)* | 2020-01-08 | 2024-01-30 | 中国石油化工股份有限公司 | Halogen-free flame retardant and application thereof in preparation of halogen-free flame retardant PA6 |
| KR102131198B1 (en) | 2020-01-10 | 2020-07-07 | 한국원자력연구원 | Reduced graphene oxide-funtional material complex and production method thereof |
| KR20200006164A (en)* | 2020-01-10 | 2020-01-17 | 한국원자력연구원 | Reduced graphene, reduced graphene oxide-funtional material complex and production methods thereof |
| US11539054B2 (en) | 2020-03-13 | 2022-12-27 | Hyundai Motor Company | Method of manufacturing catalyst ink free of eluted transition metal for fuel cell |
| CN111564321A (en)* | 2020-05-27 | 2020-08-21 | 新昌县易纵新材料科技有限公司 | Tin oxide-modified g-C3N4Electrode material of super capacitor and preparation method thereof |
| CN111564321B (en)* | 2020-05-27 | 2023-01-13 | 新昌县易纵新材料科技有限公司 | Tin oxide-modified g-C 3 N 4 Electrode material of super capacitor and preparation method thereof |
| CN112264100A (en)* | 2020-10-20 | 2021-01-26 | 广州维港环保科技有限公司 | Bifunctional graphene oxide catalyst, and preparation method and application thereof |
| WO2022083142A1 (en)* | 2020-10-20 | 2022-04-28 | 广州维港环保科技有限公司 | Bifunctional graphene oxide catalyst, preparation method therefor and use thereof |
| CN112349921A (en)* | 2020-11-17 | 2021-02-09 | 浙江理工大学 | Nitrogen-doped graphene hollow sphere catalyst, preparation method and application |
| CN112349921B (en)* | 2020-11-17 | 2021-09-24 | 浙江理工大学 | Nitrogen-doped graphene hollow sphere catalyst, preparation method and application |
| CN112397728A (en)* | 2020-11-24 | 2021-02-23 | 上海纳米技术及应用国家工程研究中心有限公司 | Preparation method of Co and Fe element modified graphite-phase carbon nitride and graphene oxide fuel cell cathode catalyst |
| KR102535864B1 (en) | 2021-02-16 | 2023-05-23 | 부산대학교 산학협력단 | Manufacturing method of noble metal-free catalysts for water electrolysis |
| KR20220116982A (en)* | 2021-02-16 | 2022-08-23 | 부산대학교 산학협력단 | Manufacturing method of noble metal-free catalysts for water electrolysis |
| CN113444558B (en)* | 2021-05-26 | 2023-12-01 | 无锡烯创科技有限公司 | Organic modification method for improving dispersibility of graphite-phase carbon nitride in lubricating oil |
| CN113444558A (en)* | 2021-05-26 | 2021-09-28 | 无锡烯创科技有限公司 | Organic modification method for improving dispersibility of graphite-phase carbon nitride in lubricating oil |
| CN113764684A (en)* | 2021-08-17 | 2021-12-07 | 上海纳米技术及应用国家工程研究中心有限公司 | Preparation method of fuel cell cathode catalyst material |
| CN114709388A (en)* | 2022-02-17 | 2022-07-05 | 山东科技大学 | Preparation method and application of graphite and melamine co-modified micron SiOx negative electrode material |
| WO2024036756A1 (en)* | 2022-08-19 | 2024-02-22 | 台州学院 | Multifunctional phosphorus and nickel doped graphite-like carbon nitride nanosheet, preparation method therefor, and abs material |
| CN115945205A (en)* | 2022-09-30 | 2023-04-11 | 江汉大学 | Preparation method and application of a graphitic carbon nitride material with enhanced photocatalytic performance |
| KR20240060993A (en)* | 2022-10-31 | 2024-05-08 | 경상국립대학교산학협력단 | Composition for sintering ceramic and manufacturing method thereof, zirconia sintered body using thereof and manufacturing method thereof |
| KR102845450B1 (en) | 2022-10-31 | 2025-08-12 | 경상국립대학교 산학협력단 | Composition for sintering ceramic and manufacturing method thereof, zirconia sintered body using thereof and manufacturing method thereof |
| KR102639923B1 (en)* | 2022-11-14 | 2024-02-22 | 한국세라믹기술원 | Manufacturing method of nitrogen doped electrode active material with reduced chemical amount by using surface modifier, and supercapacitor using the same and method of manufacturing thereof |
| CN118637720A (en)* | 2024-08-16 | 2024-09-13 | 成都瀚川环境科技有限公司 | A method for eliminating organic matter in water by electrochemically activating sulfite |
| CN119447221A (en)* | 2024-09-24 | 2025-02-14 | 合肥国轩高科动力能源有限公司 | A phosphorus-carbon-silver composite material and its preparation method and application |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101640545B1 (en) | Production method of catalyst-graphitic carbon nitride-reduced graphene oxide composite, the composite produced thereby, and an electrode using the same | |
| Gavrilov et al. | Electrocatalysis of oxygen reduction reaction on polyaniline-derived nitrogen-doped carbon nanoparticle surfaces in alkaline media | |
| Liu et al. | A facile preparation of CoFe 2 O 4 nanoparticles on polyaniline-functionalised carbon nanotubes as enhanced catalysts for the oxygen evolution reaction | |
| Tian et al. | Nitrogen‐doped graphene/carbon nanotube hybrids: in situ formation on bifunctional catalysts and their superior electrocatalytic activity for oxygen evolution/reduction reaction | |
| Sun et al. | Graphene-based transition metal oxide nanocomposites for the oxygen reduction reaction | |
| Sun et al. | Boron, nitrogen co-doped graphene: a superior electrocatalyst support and enhancing mechanism for methanol electrooxidation | |
| JP6289630B2 (en) | Method for producing nitrogen-doped carbon nanohorn for oxygen reduction electrocatalyst | |
| Hassani et al. | Porous nitrogen-doped graphene prepared through pyrolysis of ammonium acetate as an efficient ORR nanocatalyst | |
| Liu et al. | Heating treated carbon nanotubes as highly active electrocatalysts for oxygen reduction reaction | |
| Zhang et al. | Fabrication of 3D interconnected porous MXene-based PtNPs as highly efficient electrocatalysts for methanol oxidation | |
| Phihusut et al. | Gently reduced graphene oxide incorporated into cobalt oxalate rods as bifunctional oxygen electrocatalyst | |
| US20180034055A1 (en) | Composite including porous graphene and carbon nanotube material | |
| Song et al. | Additional doping of phosphorus into polypyrrole functionalized nitrogenous carbon nanotubes as novel metal-free oxygen reduction electrocatalyst in alkaline solution | |
| Shamraiz et al. | CaO-promoted graphene-supported palladium nanocrystals as a universal electrocatalyst for direct liquid fuel cells | |
| Ensafi et al. | NiO nanoparticles decorated at Nile blue-modified reduced graphene oxide, new powerful electrocatalysts for water splitting | |
| Zhou et al. | Free-standing S, N co-doped graphene/Ni foam as highly efficient and stable electrocatalyst for oxygen evolution reaction | |
| KR101381316B1 (en) | Boron doped reduced graphene oxide and method for preparation thereof | |
| Roy et al. | Site specific nitrogen incorporation in reduced graphene oxide using imidazole as a novel reducing agent for efficient oxygen reduction reaction and improved supercapacitive performance | |
| Ma et al. | Uric acid-derived Fe3C-containing mesoporous Fe/N/C composite with high activity for oxygen reduction reaction in alkaline medium | |
| Guo et al. | Mo-chelate strategy for synthesizing ultrasmall Mo2C nanoparticles embedded in carbon nanosheets for efficient hydrogen evolution | |
| Yusoff et al. | Synthesis and characterization of reduced graphene oxide/iron oxide/silicon dioxide (rGO/Fe3O4/SiO2) nanocomposite as a potential cathode catalyst | |
| Wang et al. | Hierarchical molybdenum carbide/N-doped carbon as efficient electrocatalyst for hydrogen evolution reaction in alkaline solution | |
| Li et al. | Structural construction of Bi-anchored honeycomb N-doped porous carbon catalyst for efficient CO2 conversion | |
| Ye et al. | Oxidized indium with transformable dimensions for CO 2 electroreduction toward formate aided by oxygen vacancies | |
| Li et al. | Ionic liquids-noncovalently functionalized multi-walled carbon nanotubes decorated with palladium nanoparticles: A promising electrocatalyst for ethanol electrooxidation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application | St.27 status event code:A-0-1-A10-A12-nap-PA0109 | |
| PA0201 | Request for examination | St.27 status event code:A-1-2-D10-D11-exm-PA0201 | |
| D13-X000 | Search requested | St.27 status event code:A-1-2-D10-D13-srh-X000 | |
| D14-X000 | Search report completed | St.27 status event code:A-1-2-D10-D14-srh-X000 | |
| PE0902 | Notice of grounds for rejection | St.27 status event code:A-1-2-D10-D21-exm-PE0902 | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-3-3-R10-R18-oth-X000 | |
| E13-X000 | Pre-grant limitation requested | St.27 status event code:A-2-3-E10-E13-lim-X000 | |
| P11-X000 | Amendment of application requested | St.27 status event code:A-2-2-P10-P11-nap-X000 | |
| P13-X000 | Application amended | St.27 status event code:A-2-2-P10-P13-nap-X000 | |
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration | St.27 status event code:A-1-2-D10-D22-exm-PE0701 | |
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment | St.27 status event code:A-2-4-F10-F11-exm-PR0701 | |
| PR1002 | Payment of registration fee | St.27 status event code:A-2-2-U10-U11-oth-PR1002 Fee payment year number:1 | |
| PG1601 | Publication of registration | St.27 status event code:A-4-4-Q10-Q13-nap-PG1601 | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-5-5-R10-R18-oth-X000 | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-5-5-R10-R18-oth-X000 | |
| P22-X000 | Classification modified | St.27 status event code:A-4-4-P10-P22-nap-X000 | |
| P22-X000 | Classification modified | St.27 status event code:A-4-4-P10-P22-nap-X000 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:4 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:5 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:6 | |
| PC1903 | Unpaid annual fee | St.27 status event code:A-4-4-U10-U13-oth-PC1903 Not in force date:20220713 Payment event data comment text:Termination Category : DEFAULT_OF_REGISTRATION_FEE | |
| PC1903 | Unpaid annual fee | St.27 status event code:N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text:Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date:20220713 | |
| PN2301 | Change of applicant | St.27 status event code:A-5-5-R10-R13-asn-PN2301 St.27 status event code:A-5-5-R10-R11-asn-PN2301 | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-5-5-R10-R18-oth-X000 | |
| PN2301 | Change of applicant | St.27 status event code:A-5-5-R10-R13-asn-PN2301 St.27 status event code:A-5-5-R10-R11-asn-PN2301 | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-5-5-R10-R18-oth-X000 |