KR101218412B1 - Block Copolymer Synthesized By RAFT Reaction, And White Light-Emitting Polymer Device Using The Same - Google Patents
Block Copolymer Synthesized By RAFT Reaction, And White Light-Emitting Polymer Device Using The SameDownload PDFInfo
- Publication number
- KR101218412B1 KR101218412B1KR1020100042522AKR20100042522AKR101218412B1KR 101218412 B1KR101218412 B1KR 101218412B1KR 1020100042522 AKR1020100042522 AKR 1020100042522AKR 20100042522 AKR20100042522 AKR 20100042522AKR 101218412 B1KR101218412 B1KR 101218412B1
- Authority
- KR
- South Korea
- Prior art keywords
- light emitting
- poly
- layer
- block copolymer
- emitting diode
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2/00—Processes of polymerisation
- C08F2/38—Polymerisation using regulators, e.g. chain terminating agents, e.g. telomerisation
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/111—Organic polymers or oligomers comprising aromatic, heteroaromatic, or aryl chains, e.g. polyaniline, polyphenylene or polyphenylene vinylene
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/10—Organic polymers or oligomers
- H10K85/151—Copolymers
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/14—Macromolecular compounds
- C09K2211/1441—Heterocyclic
- C09K2211/1466—Heterocyclic containing nitrogen as the only heteroatom
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Physics & Mathematics (AREA)
- Optics & Photonics (AREA)
- Polyoxymethylene Polymers And Polymers With Carbon-To-Carbon Bonds (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Translated fromKoreanDescription
Translated fromKorean본 발명은 RAFT 반응을 통해 합성된 블락 공중합체 및 이를 이용한 백색 고분자 발광다이오드에 관한 것으로, 상세하게는 보다 안정적이고 손쉽게 발광다이오드에 사용되는 백색 발광물질을 개발하기 위해 큰 밴드갭(high bandgap)을 가지는 폴리 엔 비닐카바졸(PVK) 등의 유기화합물 및 작은 밴드갭(low bandgap)을 가지는 폴리 쓰리 헥실싸이오펜(P3HT) 등의 유기화합물을 RAFT 반응을 통해 중합시킨 블락 공중합체 및 이를 이용한 발광다이오드 제작에 관한 것이다.
The present invention relates to a block copolymer synthesized through a RAFT reaction and a white polymer light emitting diode using the same, and more particularly, to develop a white light emitting material used for a light emitting diode more stably and easily. Block copolymer obtained by polymerizing an organic compound such as polyene vinylcarbazole (PVK) and an organic compound such as poly three hexyl thiophene (P3HT) having a low bandgap through a RAFT reaction and a light emitting diode using the same It's about making.
고분자 발광다이오드는 매우 간단한 공정에 의한 제조가 가능하고 발색 특성이 우수하며, 유연한 소자의 제조가 가능하기 때문에 발광다이오드 분야에서 큰 주목을 받고 있다. 그 중에서도 백색 발광다이오드는 액정 디스플레이의 배경조명(backlight)과 풀 칼라 디스플레이(full color display)에 많이 사용되며, 발광 효율이 우수해 친환경적인 조명기구의 광원으로 이용가능하기 때문에 특히 주목의 대상이 되고 있다.Polymer light emitting diodes have been attracting great attention in the field of light emitting diodes because they can be manufactured by a very simple process, have excellent color development, and can be manufactured with flexible devices. Among them, white light emitting diodes are used for backlight and full color display of liquid crystal display, and they are particularly attention because they can be used as light source of eco-friendly lighting equipment because they have excellent luminous efficiency. have.
일반적으로 백색 발광을 구현하기 위해서는 적색, 녹색, 청색의 세가지 색깔이 포함되어 있거나 황색과 청색의 두 가지 색깔을 포함하고 있어야 한다. 이러한 색깔을 발광하는 고분자를 이용하여 백색 고분자 발광다이오드를 제작하는 여러 예가 보고되고 있다.In general, in order to realize white light emission, three colors of red, green, and blue should be included, or two colors of yellow and blue should be included. Several examples of producing a white polymer light emitting diode using a polymer emitting such a color have been reported.
이러한 고분자 발광 다이오드 구현 방법을 크게 나누어보면, 첫째, 각각의 색깔을 가지는 고분자를 다층으로 쌓아 백색을 구현하는 방법, 둘째, 각각의 색깔을 나타내는 고분자를 적절히 비율에 맞게 혼합(blend)하여 단층 소자를 제조하는 방법, 셋째, 세가지 색 또는 두 가지 색을 내는 고분자를 공중합체화 하여 백색 발광다이오드 소자를 제조하는 방법으로 분류할 수 있다.Dividing the method of implementing the polymer light emitting diode into a large size, first, a method of implementing white by stacking polymers having respective colors in multiple layers, and secondly, blending polymers of each color appropriately in proportion to a single layer device. Method of manufacturing, and third, it can be classified as a method of manufacturing a white light emitting diode device by copolymerizing a polymer that emits three colors or two colors.
위의 분류 중 첫 번째인 고분자 다층구조로 제작된 발광다이오드의 경우는 각각의 층을 연속적으로 여러 번 코팅해야 하기 때문에 복잡한 제작과정을 거칠 뿐만 아니라 고분자 발광다이오드의 최대 장점 중 하나인 습식제작 방법을 이용하지 못한다는 단점이 있다.In the case of a light emitting diode made of a polymer multilayer structure, which is the first of the above classifications, each layer must be coated several times in succession. It has the disadvantage of not using it.
두 번째인 고분자 혼합을 이용하여 제작하는 발광다이오드는 혼합비의 작은 차이에도 발광 색깔이 확연하게 달라지거나 각각의 고분자 사이에서 일어나는 상(phase) 분리로 인해 인가하는 전압이 커짐에 따라 발광 색깔이 달라지는 불안정성 문제점을 가진다.Secondly, the light emitting diode manufactured by using the polymer mixture has an instability in which the color of the light is changed as the voltage applied is increased due to the difference in the color of the light emission even by a small difference in the mixing ratio or phase separation between the polymers. I have a problem.
세 번째인 공중합체를 이용하여 고분자 발광다이오드를 제작하는 방법은 위의 두 가지 방법에 따르는 문제점을 효과적으로 방지할 수 있지만, 밴드갭이 서로 다른 분자의 성분비에 대한 정확한 몰당량을 공중합체에 도입하기 힘이 들며, 각각의 분자들의 궤도함수가 혼성화(hybridization) 될 가능성이 커 백색이 아닌 녹색 또는 적색의 빛만 발광할 가능성이 있다.The third method of manufacturing the polymer light emitting diode using the copolymer can effectively prevent the problems caused by the above two methods, but to introduce the exact molar equivalents of the component ratios of the molecules having different bandgaps into the copolymer. The force is high, and the orbital function of each molecule is likely to hybridize, so that only light of green or red light is emitted, not white.
따라서 본 발명자는 이러한 문제를 해결하기 위하여 보다 안정한 백색 발광다이오드를 제공할 수 있는 본 블락 공중합체 및 이를 이용한 소자제작을 개발하기에 이르렀다.
Accordingly, the present inventors have developed a block copolymer which can provide a more stable white light emitting diode and device fabrication using the same.
상기 문제점을 해결하기 위한, 본 발명의 목적은 백색 광을 구현할 수 있는 블락 공중합체를 합성하여, 기존의 공중합체와는 달리 비율에 따른 색 불안정성 없고, 기존의 백색 고분자 발광다이오드보다 더욱 안정하며 용이한 방법으로 제조할 수 있는 발광 소자를 제공하는 것이다.
In order to solve the above problems, an object of the present invention is to synthesize a block copolymer that can implement white light, unlike conventional copolymers, there is no color instability according to the ratio, more stable and easier than conventional white polymer light emitting diodes It is to provide a light emitting device that can be manufactured by one method.
상술한 바와 같은 목적 달성을 위하여, 본 발명은 물질 자체의 자기 조립 특성으로 백색광 구현에 적합한 모폴로지를 형성하며, 자외선 영역에서 흡수를 가지고 청색을 발광하는 큰 밴드갭의 물질과 가시광 영역의 흡수를 가지고 황색을 내는 작은 밴드갭의 물질을 이용한 블락 공중합체의 합성을 통해 색 안정성을 높이고 제작 공정을 쉽게 하면서 순수한 백색광을 내는 발광다이오드를 개발하였다.In order to achieve the above object, the present invention forms a morphology suitable for realizing white light by the self-assembly of the material itself, has a large bandgap of absorption in the ultraviolet region and the absorption of visible region of the blue light The synthesis of block copolymers using small bandgap materials that produce yellow color has led to the development of light emitting diodes that produce pure white light while enhancing color stability and facilitating the fabrication process.
구체적으로, 상술한 바와 같은 목적 달성을 위하여, 본 발명은 폴리 엔 비닐카바졸(poly(N-vinylcarbazole)), 폴리풀루오렌(polyfluorene), PCPP(poly(2,6-(4,4-bis(2-ethylhexyl)-4H-cyclopenta-[def]phenanthrene))), 폴리파라피닐렌(PPP)으로부터 선택되는 어느 하나의 청색 발광 물질과, 폴리 쓰리 헥실싸이오펜(poly(3-hexylthiophene)), MEH-PPV(poly[2-methoxy-5-(2-ethyl-hexyloxy)-1,4-phenylene-vinylene]), 벤조싸이아다이아졸(BT), 풀루오레논(Fluorenon)으로부터 선택되는 어느 하나의 황색 발광 물질을 RAFT(reversible addition fragmentation chain transfer) 중합 반응시켜 제조한 블락 공중합체를 제공한다. 상기 중합 물질은 유기 발광 다이오드의 백색 발광체로 사용되는 것을 특징으로 한다.Specifically, in order to achieve the object as described above, the present invention is poly (N-vinylcarbazole), poly fluorene (polyfluorene), PCPP (poly (2,6- (4,4-bis) (2-ethylhexyl) -4H-cyclopenta- [def ] phenanthrene))), one of the blue light-emitting materials selected from polyparaffinylene (PPP), poly hexylthiophene (poly (3-hexylthiophene)), Any one selected from MEH-PPV (poly [2-methoxy-5- (2-ethyl-hexyloxy) -1,4-phenylene-vinylene]), benzothiadiazole (BT), and pullorenon Provided is a block copolymer prepared by reversible addition fragmentation chain transfer (RAFT) polymerization of a yellow light emitting material. The polymer material is used as a white light emitting body of an organic light emitting diode.
또한, 상술한 바와 같은 목적 달성을 위하여, 본 발명은 i) ITO 양극층, ii) 버퍼층, iii) 폴리 엔 비닐카바졸(poly(N-vinylcarbazole)), 폴리풀루오렌(polyfluorene,PF), PCPP(poly(2,6-(4,4-bis(2-ethylhexyl)-4H-cyclopenta-[def]phenanthrene))), 폴리파라피닐렌(PPP)으로부터 선택되는 어느 하나의 청색 발광 물질과, 폴리 쓰리 헥실싸이오펜(poly(3-hexylthiophene)), MEH-PPV(poly[2-methoxy-5-(2-ethyl-hexyloxy)-1,4-phenylene-vinylene]), 벤조싸이아다이아졸(BT), 풀루오레논(Fluorenon)으로부터 선택되는 어느 하나의 황색 발광 물질을 RAFT(reversible addition fragmentation chain transfer) 중합 반응시켜 제조한 블락 공중합체로 구성된 백색 발광층, 및 iv) Ba/Al 음극층을 포함하는 고분자 발광 다이오드 소자를 제공한다.In addition, in order to achieve the above object, the present invention is i) ITO anode layer, ii) buffer layer, iii) poly (N-vinylcarbazole), polyfluorene (PF), PCPP (poly (2,6- (4,4-bis (2-ethylhexyl) -4H-cyclopenta- [def ] phenanthrene))), any one blue light emitting material selected from polyparaffinylene (PPP), and 3-hexylthiophene (poly (3-hexylthiophene)), MEH-PPV (poly [2-methoxy-5- (2-ethyl-hexyloxy) -1,4-phenylene-vinylene]), benzothiazole (BT ), A white light emitting layer comprising a block copolymer prepared by reversible addition fragmentation chain transfer (RAFT) polymerization of any one yellow light emitting material selected from Fluorenon, and iv) a Ba / Al cathode layer. Provided is a polymer light emitting diode device.
이때, 상기 버퍼층은 PEDOT, MoO3, LiO로부터 선택되는 어느 하나로 이루어질 수 있으며, 상기 Ba/Al 음극층의 Ba를 대신하여 Cs2CO3, TiOX(1.5≤x≤2.5), ZnO로부터 선택되는 어느 하나가 도입되거나, Al를 대신하여 Ag 또는 Cu가 도입될 수 있다.In this case, the buffer layer may be formed of any one selected from PEDOT, MoO3 , LiO, and is selected from Cs2 CO3 , TiOX (1.5 ≦x ≦ 2.5), ZnO in place of Ba of the Ba / Al cathode layer. Either may be introduced or Ag or Cu may be introduced in place of Al.
한편, 상술한 바와 같은 목적 달성을 위하여, 본 발명은 i) Au 또는 Pt로 이루어진 양극층, ii) 폴리 엔 비닐카바졸(poly(N-vinylcarbazole)), 폴리풀루오렌(polyfluorene,PF), PCPP(poly(2,6-(4,4-bis(2-ethylhexyl)-4H-cyclopenta-[def]phenanthrene))), 폴리파라피닐렌(PPP)으로부터 선택되는 어느 하나의 청색 발광 물질과, 폴리 쓰리 헥실싸이오펜(poly(3-hexylthiophene)), MEH-PPV(poly[2-methoxy-5-(2-ethyl-hexyloxy)-1,4-phenylene-vinylene]), 벤조싸이아다이아졸(BT), 풀루오레논(Fluorenon)으로부터 선택되는 어느 하나의 황색 발광 물질을 RAFT(reversible addition fragmentation chain transfer) 중합 반응시켜 제조한 블락 공중합체로 구성된 백색 발광층, 및 iii) FTO 음극층을 포함하는 고분자 발광 다이오드 소자를 제공한다.On the other hand, in order to achieve the object as described above, the present invention is i) an anode layer made of Au or Pt, ii) poly (N-vinylcarbazole), polyfluorene (polyfluorene, PF), PCPP (poly (2,6- (4,4-bis (2-ethylhexyl) -4H-cyclopenta- [def ] phenanthrene))), any one blue light emitting material selected from polyparaffinylene (PPP), and 3-hexylthiophene (poly (3-hexylthiophene)), MEH-PPV (poly [2-methoxy-5- (2-ethyl-hexyloxy) -1,4-phenylene-vinylene]), benzothiazole (BT ), A white light emitting layer composed of a block copolymer prepared by reversible addition fragmentation chain transfer (RAFT) polymerization of any one yellow light emitting material selected from Fluorenon, and iii) a polymer light emitting layer comprising an FTO cathode layer. Provided is a diode device.
여기서, 상기 백색 발광층과 음극층 사이에 Cs2CO3, TiOX(1.5≤x≤2.5), ZnO로부터 선택되는 어느 하나로 이루어진 전자전달층을 포함하고, 상기 백색 발광층과 양극층 사이에 MoO3 또는 LiO로 이루어진 정공전달층을 포함할 수 있다.Here, an electron transport layer consisting of any one selected from Cs2 CO3 , TiOX (1.5≤x≤2.5), ZnO between the white light emitting layer and the cathode layer, MoO3 or between the white light emitting layer and the anode layer It may include a hole transport layer made of LiO.
또한, 상기 전자전달층과 백색 발광층 사이에 전자전달을 위한 버퍼층으로서 고분자전해물질 또는 이온성 액체 층을 포함할 수 있다.
Further, a polymer electrolyte material or an ionic liquid layer may be included as a buffer layer for electron transfer between the electron transport layer and the white light emitting layer.
본 발명의 블락 공중합체는 큰 밴드갭의 폴리 엔 비닐카바졸(PVK) 등의 유기분자와 작은밴드갭의 폴리 쓰리 헥실싸이오펜(P3HT) 등의 유기분자를 RAFT 반응을 통해 합성하며, 이렇게 합성된 블락 공중합체를 이용한 발광 소자는 안정하고 순수한 백색 고분자 발광다이오드를 제작하는데 큰 기술적 향상을 이룰 것으로 기대된다.
The block copolymer of the present invention synthesizes organic molecules, such as poly band vinylene carbazole (PVK), having a large bandgap, and organic molecules, such as poly-hexylthiophene (P3HT), having a small bandgap, by RAFT reaction. The light emitting device using the block copolymer is expected to make a great technical improvement in producing a stable and pure white polymer light emitting diode.
도 1은 클로로포름(Chloroform, CHCl3)을 용매로 하여 측정한 폴리 엔 비닐카바졸-폴리 쓰리 헥실싸이오펜 블락 공중합체의 수소 핵자기 공명 분광 스펙트럼(1H NMR spectrum)이다.
도 2는 본 발명의 블락 공중합체의 2wt.% 클로로벤젠(Chlorobenzene) 필름 상에서의 자외선-가시광선 흡수 스펙트럼(UV-vis absorption spectrum)이다.
도 3은 본 발명의 블락 공중합체의 2wt.% 클로로벤젠(Chlorobenzene) 필름 상에서의 형광 스펙트럼(Photoluminescence spectrum)이다.
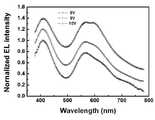
도 4는 본 발명의 블락 공중합체의 1wt.% 클로로벤젠(Chlorobenzene) 용액을 이용한 전계발광 스펙트럼(electroluminescence spectrum)이다.
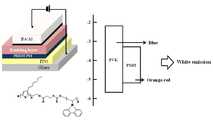
도 5는 본 발명의 폴리 엔 비닐카바졸-폴리 쓰리 헥실싸이오펜 블락 공중합체를 이용하여 제작된 백색 고분자 발광다이오드의 모식도이다.
도 6은 도 5에서와 같이 제작된 발광다이오드를 이용하여 측정한 전류밀도-전압-세기(Current density vs. voltage vs. luminance intensity(J-V-L)) 특성 그래프이다.1 is a hydrogen nuclear magnetic resonance spectral spectrum (1 H NMR spectrum) of a polyene vinylcarbazole-poly three hexylthiophene block copolymer measured using chloroform (CHCl3 ) as a solvent.
FIG. 2 is a UV-vis absorption spectrum on 2 wt.% Chlorobenzene film of the block copolymer of the present invention.
3 is a fluorescence spectrum (Photoluminescence spectrum) on a 2wt.% Chlorobenzene film of the block copolymer of the present invention.
4 is an electroluminescence spectrum using a 1 wt.% Chlorobenzene solution of the block copolymer of the present invention.
FIG. 5 is a schematic view of a white polymer light emitting diode manufactured using the polyene vinylcarbazole-poly three hexylthiophene block copolymer of the present invention. FIG.
FIG. 6 is a graph illustrating current density vs. voltage vs. luminance intensity(JVL ) characteristics measured using a light emitting diode manufactured as in FIG. 5.
본 발명에 따른 블락 공중합체 및 이를 이용한 백색 발광다이오드를 첨부된 도면을 참조하여 이하 상세하게 설명하기로 한다.The block copolymer and the white light emitting diode using the same according to the present invention will be described in detail below with reference to the accompanying drawings.
본 발명에 따른 블락 공중합체는, 하기 반응식 1에 도시된 바와 같이 청색을 발광하는 큰 밴드갭의 물질인 폴리 엔 비닐카바졸(poly(N-vinylcarbazole))과 황색 을 발광하는 작은 밴드갭의 물질인 폴리 쓰리 헥실싸이오펜(poly(3-hexylthiophene))을 RAFT(reversible addition fragmentation chain transfer) 중합 반응시켜 제조한다.The block copolymer according to the present invention, as shown in the following
[반응식 1][Reaction Scheme 1]
이때, 상기 폴리 엔 비닐카바졸(poly(N-vinylcarbazole)) 외에 , 폴리풀루오렌(polyfluorene), PCPP(poly(2,6-(4,4-bis(2-ethylhexyl)-4H-cyclopenta-[def]phenanthrene))), 폴리파라피닐렌(PPP) 등의 유기화합물이 청색 발광 물질로서 사용될 수 있으며, 상기 폴리 쓰리 헥실싸이오펜(poly(3-hexylthiophene)) 외에 MEH-PPV(poly[2-methoxy-5-(2-ethyl-hexyloxy)-1,4-phenylene-vinylene]), 벤조싸이아다이아졸(BT), 풀루오레논(Fluorenon) 등의 유기화합물이 황색 발광 물질로 사용될 수 있다.At this time, in addition to the poly (N-vinylcarbazole), polyfluorene (polyfluorene), PCPP (poly (2,6- (4,4-bis (2-ethylhexyl) -4H-cyclopenta- [def ] phenanthrene))), polyparaffinylene (PPP) and the like can be used as a blue light emitting material, and in addition to the poly three-hexylthiophene (poly (3-hexylthiophene)) MEH-PPV (poly [2- Organic compounds such as methoxy-5- (2-ethyl-hexyloxy) -1,4-phenylene-vinylene]), benzothiadiazole (BT), and fluororenon may be used as yellow light emitting materials.
상기 RAFT(reversible addition fragmentation chain transfer) 중합 반응은고분자를 합성할 때 원하는 분자량과 분자량 분포도를 정밀하게 콘트롤할 수 있는 리빙 라디칼 중합법(living radical polymerization) 중의 하나로서, 고분자 체인 끝에서 라디칼의 반응성을 조절해 원하는 분자량과 낮은 분자량 분포도의 고분자를 합성할 수 있는 방법이다.The reversible addition fragmentation chain transfer (RAFT) polymerization is one of living radical polymerizations that can precisely control the desired molecular weight and molecular weight distribution when synthesizing polymers. It is a method that can synthesize the polymer of desired molecular weight and low molecular weight distribution by adjusting.
상기 RAFT 중합 반응을 통해 합성된 본 발명의 블락 공중합체는 유기 발광 다이오드의 백색 발광체로 사용되는 것을 특징으로 한다.The block copolymer of the present invention synthesized through the RAFT polymerization reaction is used as a white light emitting body of an organic light emitting diode.
또한, 본 발명의 고분자 발광 다이오드 소자는 i) ITO 양극층, ii) 버퍼층, iii) 폴리 엔 비닐카바졸(poly(N-vinylcarbazole)), 폴리풀루오렌(polyfluorene), PCPP(poly(2,6-(4,4-bis(2-ethylhexyl)-4H-cyclopenta-[def]phenanthrene))), 폴리파라피닐렌(PPP)으로부터 선택되는 어느 하나의 청색 발광 물질과, 폴리 쓰리 헥실싸이오펜(poly(3-hexylthiophene)), MEH-PPV(poly[2-methoxy-5-(2-ethyl-hexyloxy)-1,4-phenylene-vinylene]), 벤조싸이아다이아졸(BT), 풀루오레논(Fluorenon)으로부터 선택되는 어느 하나의 황색 발광 물질을 RAFT(reversible addition fragmentation chain transfer) 중합 반응시켜 제조한 블락 공중합체로 구성된 백색 발광층, 및 iv) Ba/Al 음극층을 포함한다.In addition, the polymer light emitting diode device of the present invention is i) ITO anode layer, ii) buffer layer, iii) poly (N-vinylcarbazole), polyfluorene, PCPP (poly (2,6) -(4,4-bis (2-ethylhexyl) -4H-cyclopenta- [def ] phenanthrene))), any one blue light emitting material selected from polyparaffinylene (PPP), and poly 3-hexylthiophene (poly (3-hexylthiophene)), MEH-PPV (poly [2-methoxy-5- (2-ethyl-hexyloxy) -1,4-phenylene-vinylene]), benzothiadiazole (BT), pullulenone ( A white light emitting layer comprising a block copolymer prepared by reversible addition fragmentation chain transfer (RAFT) polymerization of any one yellow light emitting material selected from Fluorenon), and iv) a Ba / Al cathode layer.
이때, 상기 버퍼층은 PEDOT, MoO3, LiO로부터 선택되는 어느 하나로 이루어질 수 있으며, 상기 Ba/Al 음극층의 Ba를 대신하여 Cs2CO3, TiOX(1.5≤x≤2.5), ZnO로부터 선택되는 어느 하나가 도입되거나, Al를 대신하여 Ag 또는 Cu가 도입될 수 있다.In this case, the buffer layer may be formed of any one selected from PEDOT, MoO3 , LiO, and is selected from Cs2 CO3 , TiOX (1.5 ≦x ≦ 2.5), ZnO in place of Ba of the Ba / Al cathode layer. Either may be introduced or Ag or Cu may be introduced in place of Al.
또한, 본 발명의 고분자 발광 다이오드 소자는 i) Au 또는 Pt로 이루어진 양극층, ii) 폴리 엔 비닐카바졸(poly(N-vinylcarbazole)), 폴리풀루오렌(polyfluorene,PF), PCPP(poly(2,6-(4,4-bis(2-ethylhexyl)-4H-cyclopenta-[def]phenanthrene))), 폴리파라피닐렌(PPP)으로부터 선택되는 어느 하나의 청색 발광 물질과, 폴리 쓰리 헥실싸이오펜(poly(3-hexylthiophene)), MEH-PPV(poly[2-methoxy-5-(2-ethyl-hexyloxy)-1,4-phenylene-vinylene]), 벤조싸이아다이아졸(BT), 풀루오레논(Fluorenon)으로부터 선택되는 어느 하나의 황색 발광 물질을 RAFT(reversible addition fragmentation chain transfer) 중합 반응시켜 제조한 블락 공중합체로 구성된 백색 발광층, 및 iii) FTO 음극층을 포함할 수 있다.In addition, the polymer light emitting diode device of the present invention is i) an anode layer made of Au or Pt, ii) poly (N-vinylcarbazole), polyfluorene (PF), PCPP (poly (2) , 3- (4,4-bis (2-ethylhexyl) -4H-cyclopenta- [def ] phenanthrene))), polyparaffinylene (PPP), and any one of the blue light-emitting substances selected from the group, and poly-hexylthiophene (poly (3-hexylthiophene)), MEH-PPV (poly [2-methoxy-5- (2-ethyl-hexyloxy) -1,4-phenylene-vinylene]), benzothiadiazole (BT), pullo It may include a white light emitting layer consisting of a block copolymer prepared by reversible addition fragmentation chain transfer (RAFT) polymerization of any one yellow light emitting material selected from Fluorenon, and iii) FTO cathode layer.
여기서, 상기 백색 발광층과 음극층 사이에 Cs2CO3, TiOX(1.5≤x≤2.5), ZnO로부터 선택되는 어느 하나로 이루어진 전자전달층을 포함하고, 상기 백색 발광층과 양극층 사이에 MoO3 또는 LiO로 이루어진 정공전달층을 포함할 수 있다. 또한, 상기 전자전달층과 백색 발광층 사이에 전자전달을 위한 버퍼층으로서 고분자전해물질 또는 이온성 액체 층을 포함할 수 있다.Here, an electron transport layer consisting of any one selected from Cs2 CO3 , TiOX (1.5≤x≤2.5), ZnO between the white light emitting layer and the cathode layer, MoO3 or between the white light emitting layer and the anode layer It may include a hole transport layer made of LiO. Further, a polymer electrolyte material or an ionic liquid layer may be included as a buffer layer for electron transfer between the electron transport layer and the white light emitting layer.
이하에서는 상기에서 설명한 개량종국의 제조 및 활성 등을 확인하기 위한 단계별 실시방법을 살펴볼 것인바, 본 발명의 권리범위가 이들 실시 예에 한정되는 것이 아님은 당연하다.
Hereinafter, a step-by-step implementation method for confirming the production and activity of the improved species described above, bar, it is obvious that the scope of the present invention is not limited to these embodiments.
[실시 예][Example]
이하 실시예에서는 폴리 엔 비닐카바졸(poly(N-vinylcarbazole))과 폴리 쓰리 헥실싸이오펜(poly(3-hexylthiophene))을 RAFT 방법으로 블락 공중합체로 합성하고 NMR 분석하였다.In the following examples, poly (N-vinylcarbazole) and poly three-hexylthiophene (poly (3-hexylthiophene)) were synthesized by block copolymers by RAFT method and analyzed by NMR.
1.One.P3HTP3HT-b--b-PVKPVK의 합성Synthesis of
macro-RAFT 시약으로서 P3HT가 연결된 Trithiocarbonate (0.10 g, ~ 12 mmol estimated by GPC), 개시제 역할을 하는 AIBN (0.75 mg, 4.5 mmol), 및 무수 톨루엔(anhydrous toluene)(2.5 mL)가 아르곤 가스가 주입된 Schlenk 플라스크에서 15분 동안 혼합되었다.As a macro-RAFT reagent, trithiocarbonate (0.10 g, ˜12 mmol estimated by GPC) linked with P3HT, AIBN (0.75 mg, 4.5 mmol) serving as an initiator, and anhydrous toluene (2.5 mL) were injected with argon gas. Mixed for 15 minutes in a Schlenk flask.
상기 용액에,N-vinylcarbazole (1.2 g, 6.21 mmol)과 무수 톨루엔 (3 mL)의 혼합용액이 첨가되고, freeze-pump-thaw cycles(3ㅧ)에 의해 진공처리되고, 드라이 아르곤 가스로 플러쉬(flush)되었다. 상기 혼합물은 24 시간 동안 70℃에서 오일 배쓰에 담가졌다. 상기 고분자 용액은 원심분리 튜브로 옮겨지고, MeOH (200 mL)로 석출시킨 후, 원심분리 처리되었다. 얻어진 미정제 생성물은 같은 방식으로 두번 MeOH 처리되었다.To the solution, a mixed solution ofN- vinylcarbazole (1.2 g, 6.21 mmol) and anhydrous toluene (3 mL) is added, vacuumed by freeze-pump-thaw cycles (3x) and flushed with dry argon gas ( flushed). The mixture was immersed in an oil bath at 70 ° C. for 24 hours. The polymer solution was transferred to a centrifuge tube, precipitated with MeOH (200 mL) and then centrifuged. The crude product obtained was treated MeOH twice in the same manner.
이렇게 얻어진 고체 생성물은 여과된 후, P3HT와N-vinylcarbazole 모노머를 제거하기 위하여 MeOH(1 d)와 acetone(1 d)로 Soxhlet 추출하였다. 다시 상기 생성물을 THF에 녹인 후, 다시 MeOH로 석출시키고, 원심분리하여, MeOH로 세척한 후에 진공에서 건조시켜 붉은 색의 고체 고분자를 얻었다.The solid product thus obtained was filtered and then Soxhlet extracted with MeOH (1 d) and acetone (1 d) to remove P3HT andN -vinylcarbazole monomers. The product was again dissolved in THF, precipitated again with MeOH, centrifuged, washed with MeOH and dried in vacuo to give a red solid polymer.
1H NMR (CDCl3, 600 MHz): d ppm 7.97-7.77 (br, m), 7.21-6.77 (br, m), 6.67-6.1 (br, m), 5.1-4.7 (br, m), 2.87-2.65 (br, m), 1.81-1.63 (br, m), 1.55-1.17 (br, m), 0.97-0.81(br, m). GPC analysis Mn = 13,800 g/mol, Mw = 21,400 kg/mol, and PDI = 1.55 (against PS standard).
1 H NMR (CDCl3 , 600 MHz): d ppm 7.97-7.77 (br, m), 7.21-6.77 (br, m), 6.67-6.1 (br, m), 5.1-4.7 (br, m), 2.87 -2.65 (br, m), 1.81-1.63 (br, m), 1.55-1.17 (br, m), 0.97-0.81 (br, m). GPC analysis Mn = 13,800 g / mol, Mw = 21,400 kg / mol, and PDI = 1.55 (against PS standard).
2. 물질 및 분석2. Materials and Analysis
다양한 모노머들에 적용가능하고 전이금속촉매를 사용하지 않아도 되기 때문에, 폴리올레핀을 포함하는 로드-코일 블락 공중합체의 합성을 위해서 다양한 리빙 중합 방법들 중에서 RAFT (reversible addition fragmentation chain transfer)방법이 선택되었다.Since it is applicable to various monomers and does not need to use a transition metal catalyst, a reversible addition fragmentation chain transfer (RAFT) method has been selected from various living polymerization methods for the synthesis of a rod-coil block copolymer including polyolefin.
좁은 중합분포도를 가지는 트리씨오카보네이트(trithiocarbonate) macro-RAFT 시약(Mn =8.3 kg/mol, PDI = 1.11, against PS standard)을 최초 중합 (Grignard metathesis (GRIM) reaction) 및 연이은 폴리머-아날로그 반응들을 통해서 생성하였다.Initial polymerization (Grignard metathesis (GRIM) reaction) and subsequent polymer-analog reaction of trithiocarbonate macro-RAFT reagent (Mn = 8.3 kg / mol, PDI = 1.11, against PS standard) with narrow polymerization distribution Created through
N-비닐카바졸을 가진 로드-코일 폴리(싸이오펜-블락-N-비닐카바졸) 디블락 코폴리머(P3HT-b-PVK)을 RAFT 중합을 통해서 합성한 후, GPC(Gel permeation chromatography)로 관찰한 결과, 트레이스의 주된 이동이 더 높은 분자량에서 관찰되어 블락 공중합체 형성을 확인할 수 있었다. 최종 생성된 AP3HT-b-PVK의 GPC 분석은 Mn = 13.8 kg/mol (PDI = 1.55) (THF, PS standard)를 나타내었다.A rod-coil poly (thiophene-block-N-vinylcarbazole) diblock copolymer (P3HT-b-PVK) with N-vinylcarbazole was synthesized by RAFT polymerization and then subjected to gel permeation chromatography (GPC). Observations showed that the major shifts in traces were observed at higher molecular weights, confirming block copolymer formation. GPC analysis of the finally produced AP3HT-b-PVK showed Mn = 13.8 kg / mol (PDI = 1.55) (THF, PS standard).
도 1은 핵자기 공명분광기(Nuclear resonance spectrometer, NMR) 결과로서, 폴리 엔 비닐카바졸-폴리 쓰리 헥실싸이오펜 블락 공중합체의 합성을 확인할 수 있다. 도면에서 볼 수 있듯이, P3HT-b-PVK의1H NMR spectrum 의 결과는 8.2 ~ 4.3 ppm 에서 넓고 복작합 신호를 보여주는 PVK 블락 뿐만 아니라 P3HT 블락에서도 특징적인 화학 이동을 보여주었다 (H-a는 싸이오펜 CH, H-b는 싸이오펜 근처의 n-헥실 그룹의 메틸렌, H-c-g는 알킬 체인).Figure 1 shows the results of the nuclear magnetic resonance spectrometer (Nuclear resonance spectrometer, NMR), it can confirm the synthesis of polyene vinylcarbazole-poly three hexyl thiophene block copolymer. As can be seen from the figure, the results of the1 H NMR spectrum of P3HT-b-PVK showed characteristic chemical shifts in the P3HT block as well as the PVK block showing a wide and complex signal at 8.2 to 4.3 ppm (Ha is the thiophene CH , Hb is methylene of n-hexyl group near thiophene, Hcg is alkyl chain).
한편, 비대칭 PVK 공명(o-h)이 카바졸 moiety가 C2v 대칭 그룹에 속해 있음에도 불구하고,1H NMR 에서 보이는 것을 알 수 있다. PVK의 이러한 비등가성(non equivalence)은 이미 알려진 것으로, 이는 이웃 고리의 링 전류(ring current) 효과와 합쳐진 bulky 카바졸의 제한된 회전에 기인한다. 3HT-b-PVK의 구조적인 조성은 싸이오펜의 메틸렌 프로톤들(H-a)에 대한 방향성 카바졸 양성자들(H-k와 H-l)의 합산으로부터 추정될 수 있다.On the other hand, it can be seen that the asymmetric PVK resonance (oh) is seen in1 H NMR, although the carbazole moiety belongs to the C2v symmetric group. This non equivalence of PVK is already known due to the limited rotation of bulky carbazole combined with the ring current effect of neighboring rings. The structural composition of 3HT-b-PVK can be estimated from the sum of the aromatic carbazole protons (Hk and Hl) for the methylene protons (Ha) of thiophene.
한편, 도 2는 클로로벤젠을 용매로 한 용액상에서의 폴리 엔 비닐카바졸-폴리 쓰리 헥실싸이오펜 블락 공중합체의 흡수스펙트럼을 나타낸 것으로서, 331nm와 344nm에서의 흡수 피크는 PVK 부분으로부터 기인하며 최고점이 553nm에서 나타나는 흡수 피크는 P3HT 부분에 의한 것이다.On the other hand, Figure 2 shows the absorption spectrum of the polyene vinylcarbazole-poly three hexylthiophene block copolymer in the chlorobenzene solvent solution, the absorption peak at 331nm and 344nm is derived from the PVK portion, the highest point The absorption peak at 553 nm is due to the P3HT moiety.
도 3은 약 410nm에서 폴리 엔 비닐카바졸에 의한 발광과 약 580nm 근처에서의 폴리 쓰리 헥실싸이오펜에 의한 발광 피크를 측정한 형광(photoluminescence) 스펙트럼 그래프로서, 폴리 쓰리 헥실싸이오펜의 에너지 밴드가 폴리 엔 비닐카바졸의 에너지 밴드 안에 들어감에도 불구하고, 에너지 이동(energy transfer) 없이 폴리 엔 비닐카바졸로 부터 청색이, 그리고 폴리 쓰리 헥실싸이오펜으로부터 황색이 발현되어 백색이 구현됨을 알 수 있다.FIG. 3 is a fluorescence spectral graph measuring emission peaks by polyene vinylcarbazole at about 410 nm and emission peaks by poly three hexylthiophenes at around 580 nm, wherein the energy band of poly three hexylthiophene is poly In spite of being in the energy band of ene vinylcarbazole, it can be seen that blue is expressed from poly ene vinylcarbazole and yellow from poly three hexylthiophene without energy transfer to realize white color.
이러한 백색광은 소자를 통해서도 구현될 수 있으며, 도 4의 전계발광(electroluminescence) 그래프를 통해서도 확인할 수 있다. 폴리 엔 비닐카바졸-폴리 쓰리 헥실싸이오펜 블락 공중합체에 의한 발광은 청색을 발현하는 400nm대의 파장과 황색을 나타내는 580nm 파장 부근에서 나타나며 이러한 개별적인 각 색상의 합으로 인해 백색이 구현되었다. 또한, 도면에서 볼 수 있듯이, 전압의 변화에 크게 의존하지 않는 안정적인 백색광이 발광됨을 확인할 수 있다.
Such white light may be realized through the device, and may also be confirmed through the electroluminescence graph of FIG. 4. Light emission by the polyene vinylcarbazole-poly three hexylthiophene block copolymers appeared in the wavelength range of 400 nm representing blue and 580 nm representing yellow, and the sum of each of these individual colors resulted in white. In addition, as can be seen in the figure, it can be seen that stable white light is emitted which does not largely depend on a change in voltage.
3. 소자의 제조3. Fabrication of Devices
상기에서 살펴본 블락 공중합체를 이용한 소자의 효율을 측정하기 위하며 도 5와 같은 구조의 소자를 제작하였다.In order to measure the efficiency of the device using the block copolymer described above, a device having a structure as shown in FIG. 5 was manufactured.
먼저 기판으로 사용할 유리 기판 위에 양극으로 이용하기 위해 코팅된 산화인듐주석(Indium tin oxide,ITO)을 세정제와 증류수, 아세톤(acetone), 이소프로필 알코올(isopropyl alcohol)의 순서대로 초음파(ultrasonic)를 이용하여 세척한 후, 세척되어진 기판을 약 하루 동안 섭씨 100도의 오븐에서 건조시킨 후 폴리 (쓰리, 포-에틸렌디옥실렌싸이오펜):폴리스틸렌 설포닉 산 (poly(3,4-ethylenedioxylene thiophene): polystylene sulfonic acid, PEDOT:PSS)을 4000rpm으로 40초 동안 스핀 코팅하여 버퍼 층으로 이용한다.First, indium tin oxide (ITO) coated for use as an anode on a glass substrate to be used as a substrate is cleaned using ultrasonic waves in the order of a detergent, distilled water, acetone, and isopropyl alcohol. The washed substrates were then dried in an oven at 100 degrees Celsius for about a day and then poly (3,4-ethylenedioxylenethiophene): polystyrene sulfonic acid (poly (3,4-ethylenedioxylene thiophene): polystylene sulfonic acid, PEDOT: PSS) is spin-coated at 4000 rpm for 40 seconds and used as a buffer layer.
이를 공기 중에 150도로 약 10 분간 건조시킨 후, 질소로 채워진 글로브 박스 안에서 클로로벤젠 용매에 1wt.%로 녹여진 폴리 엔 비닐카바졸-폴리 쓰리 헥실싸이오펜 블락 공중합체를 700rpm으로 1분간 스핀 코팅하였다.After drying for about 10 minutes at 150 ° C. in air, a polyene vinylcarbazole-poly three hexylthiophene block copolymer dissolved in 1 wt.% Of chlorobenzene in a glove box filled with nitrogen was spun at 700 rpm for 1 minute. .
기판 위에 코팅된 폴리 엔 비닐카바졸-폴리 쓰리 헥실싸이오펜 블락 공중합체의 유기 발광층에 남아있는 클로로벤젠 용매를 제거하기 위해 온도 약 60도의 핫 플레이트(hot plate)에서 10분간 건조시킨 후, 진공 열 증착기(vacuum thermal evaporator)를 이용하여 바륨(Barium) 8nm와 알루미늄(aluminum) 95nm를 연속적으로 발광층 위에 증착시켜 음극으로 이용하였다.In order to remove the chlorobenzene solvent remaining in the organic light emitting layer of the polyene vinylcarbazole-poly three hexylthiophene block copolymer coated on the substrate for 10 minutes in a hot plate of about 60 degrees temperature, vacuum heat A vapor thermal evaporator was used to deposit 8 nm of barium and 95 nm of aluminum on the light emitting layer in succession to use as a cathode.
상기와 같이 제조된 소자를 이용하여 전기발광 세기를 측정한 결과, 도 6에서 볼 수 있듯이 10.5V의 전압까지 비례하는 전계발광 세기를 확인할 수 있었으며 이러한 특성은 안정한 백광 발색 소자 구동이 가능함을 알려준다. 소자의 구동 시작전압이 2V로 낮으며 최대 발광의 세기는 130cd/m2로 측정되었다.As a result of measuring the electroluminescent intensity using the device manufactured as described above, as shown in FIG. 6, the electroluminescent intensity proportional to the voltage of 10.5V was confirmed, and this characteristic indicates that a stable white light emitting device can be driven. The driving start voltage of the device was as low as 2V and the maximum light emission intensity was measured as 130cd / m2 .
상술한 바와 같이, 본 발명의 바람직한 실시 예에 대해 설명하였으나, 본 발명은 상술한 특정의 바람직한 실시예에 한정되지 아니하며, 청구범위에서 청구하는 본 발명의 요지를 벗어남이 없이 당해 발명이 속하는 기술분야에서 통상의 지식을 가진 자라면 누구든지 다양한 변형실시가 가능한 것은 물론이고, 그와 같은 변경은 청구범위 기재의 기술적 범위 내에 포함된다 할 수 있다.As described above, although preferred embodiments of the present invention have been described, the present invention is not limited to the specific preferred embodiments described above, and the technical field to which the present invention pertains without departing from the gist of the present invention claimed in the claims. Anyone of ordinary skill in the art can make various modifications, as well as such changes can be included within the technical scope of the claims.
Claims (8)
Translated fromKoreanPoly (N-vinylcarbazole), polyfluorene, PCPP (poly (2,6- (4,4-bis (2-ethylhexyl) -4H-cyclopenta- [def ] phenanthrene) )), Any one blue light emitting material selected from polyparaffinylene (PPP), poly (hexylthiophene), MEH-PPV (poly [2-methoxy-5- (2-) ethyl-hexyloxy) -1,4-phenylene-vinylene]), benzothiadiazole (BT), and any one yellow luminescent material selected from pullorenone (Fluorenon) is a polymerization reaction of RAFT (reversible addition fragmentation chain transfer) Block copolymer prepared by
2. The block copolymer of claim 1, wherein the polymeric material is used as a white light emitter of an organic light emitting diode.
i) ITO anode layer, ii) buffer layer, iii) poly (N-vinylcarbazole), polyfluorene (PF), PCPP (poly (2,6- (4,4-bis ( 2-ethylhexyl) -4H-cyclopenta- [def ] phenanthrene))), polyparaffinylene (PPP), any one of the blue light-emitting substance, poly hexylthiophene (poly (3-hexylthiophene), MEH Any one selected from -PPV (poly [2-methoxy-5- (2-ethyl-hexyloxy) -1,4-phenylene-vinylene]), benzothiadiazole (BT), and pullorenon A polymer light emitting diode comprising a white light emitting layer comprising a block copolymer prepared by reversible addition fragmentation chain transfer (RAFT) polymerization of a yellow light emitting material, and iv) a Ba / Al cathode layer.
4. The polymer light emitting diode device of claim 3, wherein the buffer layer is formed of any one selected from PEDOT, MoO3 , and LiO.
The method of claim 3, wherein any one selected from Cs2 CO3 , TiOX (1.5 ≦x ≦ 2.5), ZnO is introduced in place of Ba of the Ba / Al cathode layer, or Ag or Cu is substituted in place of Al. A polymer light emitting diode device, characterized in that introduced.
According to claim 6, Between the white light emitting layer and the cathode layer comprises a electron transport layer consisting of any one selected from Cs2 CO3 , TiOX (1.5≤x≤2.5), ZnO, Between the white light emitting layer and the anode layer A polymer light emitting diode device comprising a hole transport layer made of MoO3 or LiO.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020100042522AKR101218412B1 (en) | 2010-05-06 | 2010-05-06 | Block Copolymer Synthesized By RAFT Reaction, And White Light-Emitting Polymer Device Using The Same |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020100042522AKR101218412B1 (en) | 2010-05-06 | 2010-05-06 | Block Copolymer Synthesized By RAFT Reaction, And White Light-Emitting Polymer Device Using The Same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20110123080A KR20110123080A (en) | 2011-11-14 |
| KR101218412B1true KR101218412B1 (en) | 2013-01-18 |
Family
ID=45393364
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020100042522AExpired - Fee RelatedKR101218412B1 (en) | 2010-05-06 | 2010-05-06 | Block Copolymer Synthesized By RAFT Reaction, And White Light-Emitting Polymer Device Using The Same |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR101218412B1 (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20200020116A (en) | 2018-08-16 | 2020-02-26 | 동우 화인켐 주식회사 | A photo sensitive resin composition, a display partition wall structure prepared using the composition, and a display devide comprising the same |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102169515B1 (en)* | 2013-08-30 | 2020-10-26 | 엘지디스플레이 주식회사 | Quinone derivatives and organic light emitting diode device comprising the same |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5807974A (en) | 1996-05-16 | 1998-09-15 | Korea Institute Of Science And Technology | Fluorene-based alternating copolymers for electroluminescence element and electroluminescence element using such copolymers as light emitting materials |
| US20010053462A1 (en) | 2000-05-02 | 2001-12-20 | Masayuki Mishima | Light-emitting device |
| US6451458B1 (en) | 1998-11-27 | 2002-09-17 | Jsr Corporation | Electroluminescent material and electroluminescent cell |
- 2010
- 2010-05-06KRKR1020100042522Apatent/KR101218412B1/ennot_activeExpired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5807974A (en) | 1996-05-16 | 1998-09-15 | Korea Institute Of Science And Technology | Fluorene-based alternating copolymers for electroluminescence element and electroluminescence element using such copolymers as light emitting materials |
| US6451458B1 (en) | 1998-11-27 | 2002-09-17 | Jsr Corporation | Electroluminescent material and electroluminescent cell |
| US20010053462A1 (en) | 2000-05-02 | 2001-12-20 | Masayuki Mishima | Light-emitting device |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20200020116A (en) | 2018-08-16 | 2020-02-26 | 동우 화인켐 주식회사 | A photo sensitive resin composition, a display partition wall structure prepared using the composition, and a display devide comprising the same |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20110123080A (en) | 2011-11-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Wang et al. | High-efficiency red and green light-emitting polymers based on a novel wide bandgap poly (2, 7-silafluorene) | |
| CN101238756B (en) | Electroluminescent polymers and their use | |
| CN105778054B (en) | A kind of monolayer exciplex and monomolecular exciplex white light polymer and its preparation method and application | |
| Liu et al. | Three‐Color White Electroluminescence from a Single Polymer System with Blue, Green and Red Dopant Units as Individual Emissive Species and Polyfluorene as Individual Polymer Host | |
| EP2207834B1 (en) | Polymer, and organic photoelectric device comprising the same | |
| Tamilavan et al. | Synthesis and characterization of indenofluorene‐based copolymers containing 2, 5‐bis (2‐thienyl)‐N‐arylpyrrole for bulk heterojunction solar cells and polymer light‐emitting diodes | |
| WO2006052457A2 (en) | New class of bridged biphenylene polymers | |
| TW201336968A (en) | Polymer, polymer composition and organic light-emitting device | |
| Zhao et al. | White light-emitting devices based on star-shape like polymers with diarylmaleimde fluorophores on the side chain of polyfluorene arms | |
| He et al. | Bipolar blue-emitting poly (N-9′-heptadecanyl-carbazole-2, 7-diyl-co-dibenzothiophene-S, S-dioxide-3, 7-diyl) s | |
| EP2076581A1 (en) | Light emissive device | |
| Peng et al. | Highly efficient single-layer blue polymer light-emitting diodes based on hole-transporting group substituted poly (fluorene-co-dibenzothiophene-S, S-dioxide) | |
| Zhang et al. | Deep blue light-emitting polymers with fluorinated backbone for enhanced color purity and efficiency | |
| CN111269344A (en) | White light fluorescent high molecular compound based on space charge transfer effect and preparation method and application thereof | |
| Liu et al. | Highly efficient green PLED based on triphenlyaminesilole-carbazole-fluorene copolymers with TPBI as the hole blocking layer | |
| Li et al. | Highly luminescent network films from electrochemical deposition of peripheral carbazole functionalized fluorene oligomer and their applications for light-emitting diodes | |
| Zhan et al. | Synthesis and electroluminescence of poly (aryleneethynylene) s based on fluorene containing hole-transport units | |
| JP2012500886A (en) | Luminescent materials and devices | |
| GB2473816A (en) | Electroluminescent materials and devices | |
| Wang et al. | Tunable charge transfer effect in poly (spirobifluorene) s with different electron-rich side chains | |
| KR101218412B1 (en) | Block Copolymer Synthesized By RAFT Reaction, And White Light-Emitting Polymer Device Using The Same | |
| JP5183212B2 (en) | Phosphorescent OLED | |
| KR101237139B1 (en) | Electroactive polymer, device made therefrom and method | |
| KR20170048424A (en) | Organic light-emitting composition, device and method | |
| He et al. | A novel hyperbranched conjugated polymer for light emitting devices |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application | St.27 status event code:A-0-1-A10-A12-nap-PA0109 | |
| PA0201 | Request for examination | St.27 status event code:A-1-2-D10-D11-exm-PA0201 | |
| P11-X000 | Amendment of application requested | St.27 status event code:A-2-2-P10-P11-nap-X000 | |
| P13-X000 | Application amended | St.27 status event code:A-2-2-P10-P13-nap-X000 | |
| P11-X000 | Amendment of application requested | St.27 status event code:A-2-2-P10-P11-nap-X000 | |
| P13-X000 | Application amended | St.27 status event code:A-2-2-P10-P13-nap-X000 | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-3-3-R10-R18-oth-X000 | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-3-3-R10-R18-oth-X000 | |
| D13-X000 | Search requested | St.27 status event code:A-1-2-D10-D13-srh-X000 | |
| D14-X000 | Search report completed | St.27 status event code:A-1-2-D10-D14-srh-X000 | |
| PG1501 | Laying open of application | St.27 status event code:A-1-1-Q10-Q12-nap-PG1501 | |
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection | St.27 status event code:A-1-2-D10-D21-exm-PE0902 | |
| P11-X000 | Amendment of application requested | St.27 status event code:A-2-2-P10-P11-nap-X000 | |
| P13-X000 | Application amended | St.27 status event code:A-2-2-P10-P13-nap-X000 | |
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration | St.27 status event code:A-1-2-D10-D22-exm-PE0701 | |
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment | St.27 status event code:A-2-4-F10-F11-exm-PR0701 | |
| PR1002 | Payment of registration fee | St.27 status event code:A-2-2-U10-U11-oth-PR1002 Fee payment year number:1 | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-5-5-R10-R18-oth-X000 | |
| PG1601 | Publication of registration | St.27 status event code:A-4-4-Q10-Q13-nap-PG1601 | |
| FPAY | Annual fee payment | Payment date:20151229 Year of fee payment:4 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:4 | |
| PN2301 | Change of applicant | St.27 status event code:A-5-5-R10-R13-asn-PN2301 St.27 status event code:A-5-5-R10-R11-asn-PN2301 | |
| PN2301 | Change of applicant | St.27 status event code:A-5-5-R10-R11-asn-PN2301 | |
| PN2301 | Change of applicant | St.27 status event code:A-5-5-R10-R14-asn-PN2301 | |
| R17-X000 | Change to representative recorded | St.27 status event code:A-5-5-R10-R17-oth-X000 | |
| P22-X000 | Classification modified | St.27 status event code:A-4-4-P10-P22-nap-X000 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:5 | |
| FPAY | Annual fee payment | Payment date:20170927 Year of fee payment:6 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:6 | |
| LAPS | Lapse due to unpaid annual fee | ||
| PC1903 | Unpaid annual fee | St.27 status event code:A-4-4-U10-U13-oth-PC1903 Not in force date:20181228 Payment event data comment text:Termination Category : DEFAULT_OF_REGISTRATION_FEE | |
| PC1903 | Unpaid annual fee | St.27 status event code:N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text:Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date:20181228 | |
| P22-X000 | Classification modified | St.27 status event code:A-4-4-P10-P22-nap-X000 | |
| P22-X000 | Classification modified | St.27 status event code:A-4-4-P10-P22-nap-X000 | |
| P22-X000 | Classification modified | St.27 status event code:A-4-4-P10-P22-nap-X000 |