KR100855621B1 - Apparatus and method for producing autologous thrombin and fibrinogen - Google Patents
Apparatus and method for producing autologous thrombin and fibrinogenDownload PDFInfo
- Publication number
- KR100855621B1 KR100855621B1KR1020060057186AKR20060057186AKR100855621B1KR 100855621 B1KR100855621 B1KR 100855621B1KR 1020060057186 AKR1020060057186 AKR 1020060057186AKR 20060057186 AKR20060057186 AKR 20060057186AKR 100855621 B1KR100855621 B1KR 100855621B1
- Authority
- KR
- South Korea
- Prior art keywords
- blood
- fibrinogen
- thrombin
- solution
- plasma
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M3/00—Tissue, human, animal or plant cell, or virus culture apparatus
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/36—Blood coagulation or fibrinolysis factors
- A61K38/363—Fibrinogen
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/48—Hydrolases (3) acting on peptide bonds (3.4)
- A61K38/482—Serine endopeptidases (3.4.21)
- A61K38/4833—Thrombin (3.4.21.5)
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- Biotechnology (AREA)
- Virology (AREA)
- Organic Chemistry (AREA)
- Hematology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Cell Biology (AREA)
- Wood Science & Technology (AREA)
- Sustainable Development (AREA)
- Microbiology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Developmental Biology & Embryology (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Translated fromKoreanDescription
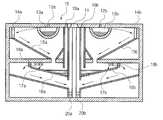
Translated fromKorean도 1은 본 발명에 따른 자가 트롬빈 및 피브리노겐의 제조장치를 나타내는 단면도,1 is a cross-sectional view showing an apparatus for producing autologous thrombin and fibrinogen according to the present invention;
도 2는 본 발명에 따른 자가 트롬빈 및 피브리노겐의 제조장치를 나타내는 평면도,2 is a plan view showing an apparatus for producing autologous thrombin and fibrinogen according to the present invention;
도 3은 본 발명에 따른 자가 트롬빈 및 피브리노겐으로 만든 젤을 나타내는 사진,Figure 3 is a photograph showing a gel made of autologous thrombin and fibrinogen according to the present invention,
도 4는 본 발명에 따른 자가 트롬빈 및 피브리노겐으로 만든 젤을 이용하여 찢어진 상악동점막을 붙여 재료의 부착성능을 보여주는 사진,Figure 4 is a photograph showing the adhesion performance of the material by attaching the torn maxillary sinus mucosa using a gel made of autologous thrombin and fibrinogen according to the present invention,
도 5는 본 발명에 따른 자가 트롬빈 및 피브리노겐으로 만든 젤을 타이타늄 인공치아 표면에 적용하여 재료의 부착성을 보여주는 사진,Figure 5 is a photograph showing the adhesion of the material by applying a gel made of autologous thrombin and fibrinogen according to the invention on the titanium artificial tooth surface,
도 6은 본 발명에 따른 자가 트롬빈 및 피브리노겐으로 만든 젤 및 혈소판풍부혈장의 골조직재생능력을 나타내는 사진이다.Figure 6 is a photograph showing the bone tissue regeneration ability of the gel and platelet rich plasma made of autologous thrombin and fibrinogen according to the present invention.
<도면의 주요 부분에 대한 부호의 설명><Explanation of symbols for main parts of the drawings>
10 : 회전구동체11 : 구동축10: rotary drive 11: drive shaft
12a,12b : 투입부13a,13b : 제1저장부12a, 12b:
14a,14b : 혈장액분리부15a,15b : 이송부14a, 14b: Plasma
16a,16b : 제2저장부17a,17b : 시약첨가부16a, 16b:
18a,18b : 용액분리부19a,19b : 용액흡입부18a, 18b:
20a,20b : 배출부20a, 20b: discharge part
본 발명은 자가 트롬빈 및 피브리노겐의 제조장치 및 방법에 관한 것으로서, 더욱 상세하게는 환자 자신의 혈액을 이용하여 자가 혈액젤을 간단하게 자동화 시스템을 이용하여 제조할 수 있도록 함으로써, 작업 공수 및 공정 시간을 절감하며, 이를 토대로 자가 혈액젤의 대량 생산이 가능한 새로운 자가 트롬빈 및 피브리노겐의 제조장치 및 방법에 관한 것이다.The present invention relates to an apparatus and method for producing autologous thrombin and fibrinogen, and more specifically, by using an automated system, autologous blood gel can be manufactured using a patient's own blood, thereby reducing workmanship and processing time. The present invention relates to a device and a method for producing a new autologous thrombin and fibrinogen capable of mass production of autologous blood gel.
일반적으로, 외과적인 시술에서 흔히 순간접착제로 사용되는 합성재료인 시아노아크릴레이트(cyanoacrylate)를 사용하여 조직을 재생시키는 방법이 있다.In general, there is a method for regenerating tissue using cyanoacrylate, which is a synthetic material commonly used as a temporary adhesive in surgical procedures.
그러나, 상기 재료는 신체 조직 내에 잘 흡수되지 않고, 영구적으로 조직 내에 남아 있기 때문에 신체의 외부 즉 피부에서는 많이 사용되어 왔으나, 인체 내부에서는 널리 사용되지 않고 있다.However, the material has not been absorbed well in body tissues and remains permanently in tissues, so it has been widely used on the outside of the body, that is, the skin, but is not widely used inside the human body.
최근 인간의 혈액에서 채취한 피브리노겐으로 만든 피브린 젤이 상기한 재료 에 비해 널리 사용되고 있다.Recently, fibrin gel made from fibrinogen collected from human blood has been widely used in comparison with the above materials.
이는 상기 피브린 젤이 상기 시아노아크릴레이트보다 조직적합성, 생분해성, 지혈능력 면에서 우수하기 때문이다.This is because the fibrin gel is superior in cyanoacrylate in terms of histocompatibility, biodegradability, and hemostatic ability.
현재 상품화되어 판매되고 있는 피브린 젤로는 TISSEEL(Baxter AG, Austria), TISSUCOL(Baxter AG, Austria), BERIPLAST(Behring, Germany), GREENPLAST(녹십자, 한국) 등이 있다.Commercially available fibrin gels include TISSEEL (Baxter AG, Austria), TISSUCOL (Baxter AG, Austria), BERIPLAST (Behring, Germany) and GREENPLAST (Green Cross, Korea).
그러나, 이러한 피브린 젤은 여러 사람에서 얻어진 혈액을 재료로 하여 만들어지기 때문에 감염이나 후천성면역결핍증(AIDS)과 같은 전염성 질환의 전이에 대한 우려가 있고, 또한 소의 트롬빈을 사용하므로 응고장애와 같은 과민반응 등이 발생될 수 있는 위험이 있으며, 광우병 발생시에 전면적으로 사용이 중단되는 어려움이 있다.However, since these fibrin gels are made from blood obtained from various people, there is a concern about the transmission of infectious diseases such as infections and AIDS, and also because of the use of bovine thrombin, hypersensitivity reactions such as clotting disorders. There is a risk that can occur, etc., there is a difficulty in stopping the use of the whole when mad cow disease occurs.
이러한 이유로 미국에서는 피브린 젤이 FDA 승인을 받지 못하고 있다.For this reason, fibrin gels are not FDA approved in the United States.
따라서, 자가혈액을 이용하여 젤을 개발하여야 할 필요성이 끊임없이 대두되고 있으며, 이에 자가혈액에서 고농도의 성장인자와 고농도의 피브리노겐을 함유하는 피브린과 트롬빈을 추출하여 자가 혈액젤을 제조하는 기술이 개발되었으며, 이들을 이용하여 조직 재생이 타생체 재료나 기존의 혈소판풍부혈장보다 더 효과적으로 이루어지는 것을 확인하였다.Therefore, the necessity of developing a gel using autologous blood is constantly emerging. Therefore, a technology for producing autologous blood gel by extracting fibrin and thrombin containing high growth factor and high concentration of fibrinogen from autologous blood has been developed. Using these results, tissue regeneration was confirmed to be more effective than other biomaterials or conventional platelet-rich plasma.
그런데, 이러한 자가 혈액젤을 제조시 임상 전문가가 일일이 자가 혈액에서 상기 트롬빈과 피브리노겐을 추출하게 되는 바, 그 공정이 복잡하고, 공정 시간이 오래 걸리는 문제점이 있으며, 제조된 혈액젤의 양이 소량으로 한정되어 경제적으 로 불리한 문제점이 있다.However, when manufacturing such autologous blood gel, a clinical expert extracts the thrombin and fibrinogen from autologous blood one by one, and the process is complicated and takes a long time to process, and the amount of manufactured blood gel is small. There is a limited economic disadvantage.
따라서, 본 발명은 상기와 같은 문제점을 해결하기 위해 발명한 것으로서, 환자 자신의 혈액을 이용하여 자가 혈액젤을 제조할 수 있는 트롬빈 및 피브리노겐을 동시에 자동화 시스템을 이용하여 간단하게 제조할 수 있도록 함으로써, 작업 공수 및 공정 시간을 절감하며, 이를 토대로 자가 혈액젤의 대량 생산을 구현할 수 있는 새로운 자가 트롬빈 및 피브리노겐의 제조장치 및 방법을 제공하는데 그 목적이 있다.Therefore, the present invention has been invented to solve the above problems, by allowing a simple production of thrombin and fibrinogen, which can produce autologous blood gel using the patient's own blood, using an automated system at the same time, It is an object of the present invention to provide a new device and method for producing autologous thrombin and fibrinogen, which can reduce labor and processing time, and can realize mass production of autologous blood gel.
이하, 상기와 같은 목적을 달성하기 위한 본 발명의 특징에 대해 설명하면 다음과 같다.Hereinafter, the features of the present invention for achieving the above object are as follows.
본 발명에 따른 자가 트롬빈 및 피브리노겐의 제조장치는, 원심분리기에 탈,장착되며 회전 중심축을 중심으로 좌우 대칭인 2개로 분리된 챔버를 갖는 회전구동체로 이루어지며,The apparatus for producing autologous thrombin and fibrinogen according to the present invention comprises a rotary drive having two separate chambers which are detached and mounted in a centrifuge and are symmetrical about a rotational central axis.
자가 혈액의 일정량이 투입되어 여액을 분리하거나 첨가제를 혼합할 수 있도록 임시 저장하는 저장수단과;Storage means for temporarily storing a certain amount of autologous blood to separate the filtrate or mix the additives;
상기 저장수단의 외측에 장착되어 상기 원심 분리 후 혈액에서 필요없는 여액(혈구세포층, 상층액)을 여과할 수 있도록 하는 여과수단과:Filtering means mounted on an outer side of the storage means to filter the filtrate (blood cell layer, supernatant) that is not necessary in the blood after the centrifugation;
상기 여과수단에 의해 분리된 혈액에서 각각의 트롬빈과 피브리노겐을 추출할 수 있도록 첨가제를 자동으로 제어하여 첨가시키는 첨가수단을 포함하여 구성된 것을 특징으로 한다.Characterized in that it comprises an additional means for automatically controlling the additives to extract the respective thrombin and fibrinogen in the blood separated by the filtering means.
특히, 상기 혈액을 회전구동체 내에 투입할 수 있도록 형성된 투입부와;In particular, an input unit formed to inject the blood into the rotary drive;
상기 혈액에서 추출된 트롬빈과 피브리노겐을 외부로 뽑아낼 수 있도록 형성된 용액흡입부가 더 포함되고, 상기 여과수단인 혈장액분리부에서 분리된 혈장액이 중력을 통해 하방으로 흘러 제2저장부로 이송되도록 깔때기 형태의 이송부가 더 포함된 것을 특징으로 한다.The solution intake portion formed to extract the thrombin and fibrinogen extracted from the blood is further included, and the funnel so that the plasma liquid separated from the plasma solution separation unit, the filtering means flows downward through gravity to be transferred to the second storage unit. Characterized in that the transfer portion further comprises.
또한, 회전구동체의 일측 투입부를 통하여 혈액 5ml를 주사하여 일측의 제1저장부에 넣는 동시에, 타측 투입부를 통하여 혈액 15ml를 주사하여 타측의 제1저장부에 넣은 후 외부로부터의 오염을 방지하기 위하여 양쪽 투입부를 밀봉하는 제1단계와;In addition, by injecting 5ml of blood through one input part of the rotary drive into the first storage part on one side, and 15ml of blood injected through the other input part into the first storage part on the other side to prevent contamination from the outside A first step of sealing both inputs in order to
상기 회전구동체를 온도, 속도, 회전시간 및 회전방향의 조절이 가능한 원심분리기 내에 위치시키고, 상기 원심분리기를 작동하여 필요없는 여액이 분리된 혈장액을 얻고 이 혈장액을 제2저장부에 저장하는 제2단계와;The rotary drive is placed in a centrifuge capable of adjusting temperature, speed, rotation time and direction of rotation, and the centrifuge is operated to obtain a plasma solution from which unnecessary filtrates have been separated and store this plasma solution in a second reservoir. A second step of doing;
상기 제2저장부에 저장되는 혈장액에 안정화제 및 응고제를 첨가하는 제3단계와;Adding a stabilizer and a coagulant to the plasma solution stored in the second storage unit;
상기 원심분리기가 회전하지 않도록 정지상태를 유지한 다음, 동일한 온도에서 작동하여 침전물 위의 상층액을 분리하는 제4단계와;A fourth step of maintaining the stationary state so that the centrifuge does not rotate and then operating at the same temperature to separate the supernatant on the precipitate;
상기 원심분리기가 정지하게 되면 제2저장부 일측의 침전물에 용해제를 첨가 하는 제5단계와;A fifth step of adding a solvent to a precipitate of one side of the second storage part when the centrifuge is stopped;
일측의 트롬빈 용액에 pH조절 용액을 첨가하는 제6단계와;A sixth step of adding a pH adjusting solution to one side of the thrombin solution;
제조된 트롬빈 용액과 피브리노겐 용액을 주사기를 사용하여 용액흡입부를 통해 뽑아내는 제7단계를 포함하여 이루어진 것을 특징으로 한다.The thrombin solution and the fibrinogen solution is characterized in that it comprises a seventh step to extract through the solution intake using a syringe.
이하, 첨부도면을 참조하여 본 발명의 구성에 대해 상세하게 설명하면 다음과 같다.Hereinafter, the configuration of the present invention with reference to the accompanying drawings in detail.
첨부한 도 1 및 도 2는 본 발명에 따른 자가 트롬빈 및 피브리노겐의 제조장치를 나타내는 각각의 단면도 및 평면도이다.1 and 2 are cross-sectional and plan views, respectively, illustrating an apparatus for producing autologous thrombin and fibrinogen according to the present invention.
본 발명은 자가 트롬빈 및 자가 피브리노겐을 동시에 제조할 수 있는 장치로서, 도 1에 도시된 바와 같이, 상기 장치는 원심분리기(미도시)에 탈,장착 가능한 형태로서, 그 중심에 회전하는 구동축(11)이 설치되어 좌우 양쪽이 동일하게 회전 가능하도록 되어 있는 회전구동체(10)이다.The present invention is a device capable of simultaneously producing autologous thrombin and autologous fibrinogen, as shown in Figure 1, the device is detachable, mounted in a centrifuge (not shown), the drive shaft rotating in the center (11) ) Is a
이와 같은 원심분리기에 탈,장착되는 회전구동체(10)는 통상의 원심분리기의 작동 환경인 온도, 속도, 회전시간 및 회전 방향의 제어를 통해 동일하게 작용할 수 있도록 이루어져 있다.The
상기 회전구동체(10)의 내부 구성에 대해 살펴보면, 그 내부는 상기 자가 혈액에서 각각 트롬빈과 피브리노겐을 추출할 수 있도록 2개로 분리된 좌우 대칭인 챔버로 구성되어 있으며, 그 중심에는 구동축(11)이 형성되어 있다.Looking at the internal configuration of the
이때, 상기 챔버의 좌우 구성은 동일하므로 일측의 구성만을 상세하게 설명하기로 한다.At this time, since the left and right configurations of the chamber are the same, only one configuration will be described in detail.
먼저, 상기 회전구동체(10) 상부의 임의의 위치에는 환자 자신의 혈액을 일정량 투입할 수 있는 일정한 직경을 갖는 홀형태의 투입부(12a,12b)가 형성되어 있으며, 그 바로 아래에는 투입된 혈액이 임시 저장되는 제1저장부(13a,13b)가 형성되어 있다.First, at any position on the upper part of the
상기 제1저장부(13a,13b)에서 일정 거리의 외측에는 상기 제1저장부(13a,13b)에 저장되어 있는 혈액에서 원심분리를 통해 혈구세포층과, 혈소판층 및 혈장층을 분리할 수 있도록 여과기(filter)로 이루어진 혈장액분리부(14a,14b)가 구비되어 있다.In order to separate the blood cell layer, the platelet layer and the plasma layer by centrifugation from the blood stored in the first storage unit (13a, 13b) outside the predetermined distance from the first storage unit (13a, 13b) Plasma
상기 혈장액분리부(14a,14b)는 상기 혈구세포층인 적혈구와 백혈구만이 흡수되도록 하고, 혈소판층 및 혈장층으로 이루어진 혈소판농축혈장은 그 하단부의 제2저장부(16a,16b)로 흐르도록 되어 있다.The plasma
이때 상기 혈장액분리부(14a,14b)에서 분리된 혈소판농축혈장은 중력을 통해 깔때기 형태의 이송부(15a,15b)를 따라 하방으로 흘러 제2저장부(16a,16b)로 이송된다.At this time, the platelet-concentrated plasma separated from the plasma
이렇게 제2저장부(16a,16b)로 이송된 혈장액에는 안정화제, 응고제, 그리고 용해제 등으로 이루어진 첨가제가 자동으로 분사되도록 상기 제2저장부(16a,16b)의 상측에 분사노즐 형태의 시약첨가부(17a,17b)가 구비되어 있다.The reagent in the form of a spray nozzle on the upper side of the second reservoir (16a, 16b) to be automatically injected into the plasma solution transferred to the second reservoir (16a, 16b) such as a stabilizer, a coagulant, and a dissolving agent.
이때, 그 시약첨가부(17a,17b)에서 제2저장부(16a,16b)로 첨가제가 일정하게 첨가되도록 하는 제어로직은 장치의 제어부에 설정되어 상기 제2저장부(16a,16b)에 혈장액이 투입될 경우 바로 구현 가능하도록 되어 있다.At this time, the control logic for constantly adding the additives from the
이때, 상기 시약첨가부(17a,17b)는 외부 인터페이스와 접촉하여 제어신호를 부여하도록 형성되어 있는 바, 상기 시약첨가부(17a,17b)의 제어로직은 트롬빈이 제조되는 제2저장부(16a)에는 일정량의 응고제인 시트르산(citric acid)이, 피브리노겐이 제조되는 제2저장부(16b)에는 일정량의 안정화제인 트랜자믹산(tranexamic acid)과 응고제인 에탄올이 혼합되도록 설정되어 있으며, 이어서 상기 트롬빈이 제조되는 제2저장부(16a)에 다시 용해제인 염화칼슘(CaCl2)과, pH를 중성(pH7)으로 조절하는 탄산수소나트륨(NaHCO3)이 혼합되도록 설정되어 있다.At this time, the
한편, 상기 시약첨가부(17a,17b)에서 1차로 응고제와 안정화제를 상기 혈장액에 첨가한 다음 원심분리하여 최종 침전물과 상층액을 분리하고, 분리된 상층액만을 배출부(20a,20b)로 흘려 보낼 수 있도록 상기 제2저장부(16a,16b)의 외측에는 여과기(filter)로 이루어진 용액분리부(18a,18b)가 구비되어 있다.Meanwhile, the coagulant and the stabilizer are first added to the plasma solution in the
이와 같이 상층액이 분리된 최종 침전물은 트롬빈 용액과 피브리노겐 용액으로 구분되는 바, 상기 일측의 트롬빈 용액에 탄산수소나트륨을 일정량 첨가할 경우, pH가 중성으로 조절되어 최종 트롬빈 용액이 제조되는 것이다.Thus, the final precipitate separated from the supernatant is divided into a thrombin solution and a fibrinogen solution. When a certain amount of sodium bicarbonate is added to the thrombin solution on one side, the pH is adjusted to neutral to prepare a final thrombin solution.
상기 제2저장부(16a,16b)에 최종적으로 남아 있는 트롬빈 용액과 피브리노겐 용액을 흡입구인 용액흡입부(19a,19b)를 통해 주사기를 이용하여 각각 뽑아내어 저장하게 되고, 이를 혼합하게 될 경우, 젤 형태의 자가 혈액젤이 완성되는 것이다.When the thrombin solution and fibrinogen solution remaining in the second storage unit (16a, 16b) is finally drawn out and stored by using a syringe through the solution intake unit (19a, 19b) as the inlet, and mixed, The gel form of autologous blood gel is completed.
이와 같이 구성되는 본 발명에 따른 자가 트롬빈 및 피브리노겐의 제조장치를 이용하여 자가 트롬빈과 피브리노겐의 제조방법을 단계별로 상세하게 설명하면 다음과 같다.The method for producing autologous thrombin and fibrinogen using the apparatus for producing autologous thrombin and fibrinogen according to the present invention configured as described above will be described in detail as follows.
1. 환자에서 혈액응고제(10% sodium citrate)를 함유한 주사기를 사용하여 혈액 20ml를 채취한다.
2. 회전구동체(10)의 왼쪽(도 1에서 구동축을 기준으로 왼쪽) 투입부(12a)를 통해 혈액 15ml를 주사하여 왼쪽의 제1저장부(13a)에 넣고, 회전구동체(10)의 오른쪽(도 1에서 구동축을 기준으로 오른쪽) 투입부(12b)를 통해 혈액 5ml를 주사하여 오른쪽의 제1저장부(13b)에 넣은 후, 외부로부터의 오염을 방지하기 위하여 양쪽 투입부(12a,12b)를 밀봉한다.
3. 상기 회전구동체(10)를 온도, 속도, 회전시간 및 회전방향의 조절이 가능한 원심분리기 내에 위치시키고, 작동 버튼을 눌러 원심분리기를 작동시킨다.
이후, 트롬빈과 피브리노겐이 얻어질 때까지 모든 과정이 자동으로 작동되도록 조절하는 것이 바람직하다.
4. 상기 원심분리기를 37℃, 1200rpm 속도로 15분간 작동시켜 혈장액인 혈소판농축혈장을 얻는다.
이때, 상기 회전구동체(10) 내의 혈액은 제1저장부(13a,13b)의 출구를 통해 빠져나가 혈장액분리부(14a,14b)를 통과하고, 혈구세포층인 적혈구와 백혈구들만이 상기 혈장액분리부(14a,14b)에 흡수된다.
5. 상기 원심분리기가 정지하면 혈액의 혈소판층과 혈장층으로 이루어진 혈소판농축혈장이 이송부(15a,15b)를 따라 왼쪽과 오른쪽의 제2저장부(16a,16b)에 저장된다.
다음, 시약첨가부(17a,17b)로부터 오른쪽의 제2저장부(16b)에는 2.85 mM 시트르산(citric acid) 22.5ml가 혈소판농축혈장에 첨가되고, 왼쪽의 제2저장부(16a)에는 100 mg/ml 트랜자믹산(tranexamic acid) 240 ml와, 99% 에탄올(ethanol) 0.75 ml가 첨가된다.
6. 상기 원심분리기는 상기 혈소판농축혈장과 첨가제가 작용할 수 있도록 온도 0 ~ 4℃에서 30분 ~ 2시간 동안 정지상태를 유지한다.
7. 상기 원심분리기를 생성된 침전물이 그 형상을 유지할 수 있는 온도인 0 ~ 4℃에서 2000 ~ 3000rpm 속도로 5 ~ 15분간 작동시켜 침전물 위의 상층액을 배출부(20a,20b)로 흘려 보낸다.
8. 상기 원심분리기가 정지하게 되면 오른쪽의 제2저장부(16b)에 있는 침전물에 0.1M 염화칼슘(CaCl2)150 ml를 첨가한다.
9. 상기 침전물이 염화칼슘과 작용하여 용해될 수 있도록 상기 원심분리기는 온도 37℃, 100rpm 속도로 좌우 방향을 바꾸어 가면서 10분간 작동한다.
이와 같이 회전 작동된 양쪽의 침전물은 용해되어 오른쪽에는 트롬빈 용액, 왼쪽에는 피브리노겐 용액이 얻어진다.
10. 상기 오른쪽의 트롬빈 용액에는 75 mM 탄산수소나트륨(NaHCO3) 100ml가 첨가되어 pH7로 조절된다.1. Collect 20 ml of blood from the patient using a syringe containing 10% sodium citrate.
2. Inject 15ml of blood through the
3. Place the
Thereafter, it is desirable to adjust the whole process to work automatically until thrombin and fibrinogen are obtained.
4. The centrifuge was operated at 37 ° C. and 1200 rpm for 15 minutes to obtain platelet-rich plasma.
At this time, the blood in the
5. When the centrifuge is stopped, platelet concentrate plasma consisting of a platelet layer and a plasma layer of blood is stored in the
Next, 22.5 ml of 2.85 mM citric acid was added to the platelet concentrate plasma in the
6. The centrifuge maintains a stationary state for 30 minutes to 2 hours at a temperature of 0 ~ 4 ℃ so that the platelet concentrate plasma and the additive can act.
7. The centrifuge is operated for 5 to 15 minutes at a speed of 2000 to 3000 rpm at a temperature at which the resulting precipitate maintains its shape at 0 to 4 ° C., and the supernatant on the precipitate is sent to the
8. When the centrifuge is stopped, 0.1M calcium chloride (CaCl2 ) in the precipitate in the second reservoir (16b) on the right 150 ml are added.
9. The centrifuge is operated for 10 minutes while changing the left and right directions at a temperature of 37 ° C. and 100 rpm so that the precipitate can be dissolved by working with calcium chloride.
The precipitates on both sides of this rotary operation are dissolved to obtain a thrombin solution on the right and a fibrinogen solution on the left.
10. 100 ml of 75 mM sodium hydrogencarbonate (NaHCO3 ) is added to the thrombin solution on the right side to adjust pH 7.
삭제delete
삭제delete
삭제delete
삭제delete
삭제delete
삭제delete
삭제delete
삭제delete
삭제delete
삭제delete
삭제delete
삭제delete
삭제delete
11. 이와 같이 제조된 트롬빈 용액과 피브리노겐 용액을 주사기를 사용하여 용액흡입부(19a,19b)를 통해 뽑아낸다.11. The thrombin solution and fibrinogen solution thus prepared are extracted through the
상기한 제조방법을 통해 제조된 자가 트롬빈 용액 및 피브리노겐 용액을 혼합하여 혈액젤로 제조하는 바, 도 3에 환자의 혈액 30ml을 이용하여 자가 트롬빈 용액 및 자가 피브리노겐 용액을 각각 제조하고, 이를 혼합하여 젤 형상을 보이는 것을 확인할 수 있다.The autogenous thrombin solution and the fibrinogen solution prepared by the above-described manufacturing method were prepared as blood gels. In FIG. 3, autologous thrombin solution and autologous fibrinogen solution were prepared using 30ml of blood of the patient, respectively, and the gels were mixed. It can be seen that the shape is shown.
한편, 첨부한 도 4는 본 발명에 따른 자가 트롬빈 및 피브리노겐으로 만든 젤을 이용하여 찢어진 상악동점막을 붙여 재료의 부착성능을 보여주는 사진으로서, 제조된 자가 혈액젤을 이용하여 찢어진 상악동점막을 다시 붙여서 점막의 치유에 미치는 효과를 확인할 수 있다.On the other hand, Figure 4 is a picture showing the adhesion performance of the material by attaching the torn maxillary sinus mucosa using a gel made of autologous thrombin and fibrinogen according to the present invention, the mucosa is reattached to the maxillary sinus mucosa using a manufactured autologous blood gel You can see the effect on healing.
또한, 첨부한 도 5는 본 발명에 따른 자가 트롬빈 및 피브리노겐으로 만든 젤을 타이타늄 인공치아 표면에 적용한 것으로서, 자가 혈액젤의 부착성을 확인할 수 있다.In addition, Figure 5 attached as applied to the surface of the titanium artificial teeth of the gel made of autologous thrombin and fibrinogen according to the present invention, it can confirm the adhesion of the autologous blood gel.
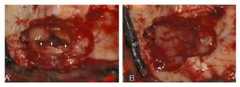
첨부한 도 6은 본 발명에 따른 자가 트롬빈 및 피브리노겐으로 만든 혈액젤(A) 및 혈소판풍부혈장(B)의 골조직재생능력을 나타내는 사진으로서, 자가 혈액젤의 골조직재생능력이 혈소판풍부혈장보다 형성된 골의 크기와 골주의 양에 있어 더 효과적으로 이루어지는 것을 확인할 수 있다.6 is a photograph showing the bone tissue regeneration ability of the blood gel (A) and platelet-rich plasma (B) made of autologous thrombin and fibrinogen according to the present invention, the bone tissue regeneration ability of the autologous blood gel than the platelet-rich plasma It can be seen that it is more effective in the size and the amount of the column.
따라서, 본 발명은 임상 전문가가 일일이 자가 혈액에서 상기 트롬빈과 피브리노겐을 추출하여 자가 혈액젤을 제조하는 기존의 공정과 비교하여 쉽고 간단하면서 신속하게 자동화 시스템을 이용하여 자가 트롬빈 용액과 피브리노겐 용액을 제조할 수 있게 된다.Therefore, the present invention provides a clinical expert to prepare autologous thrombin solution and fibrinogen solution using an automated system easily, simply and quickly compared to the conventional process of extracting the thrombin and fibrinogen from autologous blood to prepare autologous blood gel. It becomes possible.
상술한 바와 같이, 본 발명에 따른 자가 트롬빈 및 피브리노겐의 제조장치 및 방법에 의하면, 환자 자신의 혈액을 이용하여 자가 트롬빈과 자가 피브리노겐을 동시에 자동화 시스템을 이용하여 간단하게 제조하게 되므로 면역반응 문제를 방지할 수 있으며, 조직재생을 돕는 성장인자가 다량 포함되어 있어 창상부위에 적용할 경우, 조직재생의 치유기간을 단축시킬 수 있다.As described above, according to the apparatus and method for producing autologous thrombin and fibrinogen according to the present invention, the autologous thrombin and autologous fibrinogen are simply manufactured using an automated system simultaneously using the patient's own blood, thereby preventing the immune response problem. It is possible to reduce the healing period of tissue regeneration when applied to the wound site because it contains a large amount of growth factors to help tissue regeneration.
또한, 우수한 친수성, 점착성, 부착성 등과 같은 물리적 특성을 갖고 있어 다양한 형태의 골파괴된 부위에 효과적으로 충전 가능하며, 인체 적용시 주사기를 이용하여 용이하게 주입 가능하여 조직절개 및 박리를 최소한으로 하거나 하지 않고도 골결손 부위에 충전하여 골재생을 유도할 수 있는 효과가 있다.In addition, it has excellent physical properties such as hydrophilicity, adhesiveness, and adhesion, so that it can be effectively filled in various forms of bone fracture, and it can be easily injected using a syringe when applying to human body to minimize tissue incision and detachment. There is an effect that can induce bone regeneration by filling the bone defects without.
Claims (10)
Translated fromKoreanPriority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020060057186AKR100855621B1 (en) | 2006-06-26 | 2006-06-26 | Apparatus and method for producing autologous thrombin and fibrinogen |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020060057186AKR100855621B1 (en) | 2006-06-26 | 2006-06-26 | Apparatus and method for producing autologous thrombin and fibrinogen |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20080000004A KR20080000004A (en) | 2008-01-02 |
| KR100855621B1true KR100855621B1 (en) | 2008-09-01 |
Family
ID=39212375
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020060057186AExpired - Fee RelatedKR100855621B1 (en) | 2006-06-26 | 2006-06-26 | Apparatus and method for producing autologous thrombin and fibrinogen |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR100855621B1 (en) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5741428A (en) | 1993-11-19 | 1998-04-21 | E.R. Squibb & Sons, Inc. | Rapid centrifugal process for preparing fibrin monomer solution |
| US6719901B2 (en) | 1996-04-30 | 2004-04-13 | Medtronic, Inc. | System for the production of an autologous thrombin |
- 2006
- 2006-06-26KRKR1020060057186Apatent/KR100855621B1/ennot_activeExpired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5741428A (en) | 1993-11-19 | 1998-04-21 | E.R. Squibb & Sons, Inc. | Rapid centrifugal process for preparing fibrin monomer solution |
| US6719901B2 (en) | 1996-04-30 | 2004-04-13 | Medtronic, Inc. | System for the production of an autologous thrombin |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20080000004A (en) | 2008-01-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE69615163T2 (en) | TILE ADHESIVE WOUND SEALANT | |
| ES2306655T3 (en) | COMPOSITION FOR THE REGENERATION OF OSEO FABRIC. | |
| ES2340705T3 (en) | METHODS TO PREPARE AUTOMATIC FIBRINE TAIL. | |
| US6649072B2 (en) | Method for producing autologous platelet-rich plasma | |
| CN1238083C (en) | Method and apparatus for producing platelet-rich plasma and/or platelet concentrate | |
| US6444228B1 (en) | Autologous fibrin sealant and method for making the same | |
| WO2008022651A1 (en) | Process and device for the preparation of platelet rich plasma for extemporaneous use and combination thereof with skin and bone cells | |
| JP2017536892A (en) | New standardization and medical devices for preparing platelet rich plasma (prp) or bone marrow centrate (bmc), alone or in combination with hyaluronic acid | |
| US20050170006A1 (en) | Methods of applying a biological composition to an individual | |
| EP2520316B1 (en) | Thrombin isolated from blood and blood fractions | |
| JP2003517272A (en) | Apparatus and method for preparing stable, long-term thrombin from plasma, and thrombin formed thereby | |
| KR20180127538A (en) | Process, tube and device for the preparation of wound healant composition | |
| JPH09509432A (en) | Plasma concentrate and tissue sealant composition | |
| CN101677836A (en) | Methods for preparing concentrated fibrinogen-containing compositions and related systems for preparing fibrin glue | |
| CN103690999B (en) | The liquid-solid embedded material turning to gel film of a kind of PRF precursor | |
| KR100855621B1 (en) | Apparatus and method for producing autologous thrombin and fibrinogen | |
| EP2337793A1 (en) | Methods of making concentrated fibrinogen- and platelet containing compositions | |
| TWI736824B (en) | Blood separation method | |
| CA2529905A1 (en) | Autologous activated platelets | |
| CN113817712A (en) | Process for preparing thrombin | |
| Mansour et al. | Use of concentrated growth factor (CGF) in implantology | |
| CN1247271C (en) | Device for producing blood products such as fibrin glue and its medical application | |
| JP2004201799A (en) | Bone defect composite bone graft material for oral cavity and periodontal treatment | |
| CN1454667A (en) | Convenient fibrin blocking agent | |
| Al-Noori | Platelet Rich Fibrin (PRF) for treatment of oroantral fistula: a case report |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application | St.27 status event code:A-0-1-A10-A12-nap-PA0109 | |
| PA0201 | Request for examination | St.27 status event code:A-1-2-D10-D11-exm-PA0201 | |
| D13-X000 | Search requested | St.27 status event code:A-1-2-D10-D13-srh-X000 | |
| D14-X000 | Search report completed | St.27 status event code:A-1-2-D10-D14-srh-X000 | |
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection | St.27 status event code:A-1-2-D10-D21-exm-PE0902 | |
| T11-X000 | Administrative time limit extension requested | St.27 status event code:U-3-3-T10-T11-oth-X000 | |
| E13-X000 | Pre-grant limitation requested | St.27 status event code:A-2-3-E10-E13-lim-X000 | |
| P11-X000 | Amendment of application requested | St.27 status event code:A-2-2-P10-P11-nap-X000 | |
| P13-X000 | Application amended | St.27 status event code:A-2-2-P10-P13-nap-X000 | |
| E90F | Notification of reason for final refusal | ||
| PE0902 | Notice of grounds for rejection | St.27 status event code:A-1-2-D10-D21-exm-PE0902 | |
| PG1501 | Laying open of application | St.27 status event code:A-1-1-Q10-Q12-nap-PG1501 | |
| P11-X000 | Amendment of application requested | St.27 status event code:A-2-2-P10-P11-nap-X000 | |
| P13-X000 | Application amended | St.27 status event code:A-2-2-P10-P13-nap-X000 | |
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration | St.27 status event code:A-1-2-D10-D22-exm-PE0701 | |
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment | St.27 status event code:A-2-4-F10-F11-exm-PR0701 | |
| PR1002 | Payment of registration fee | St.27 status event code:A-2-2-U10-U11-oth-PR1002 Fee payment year number:1 | |
| PG1601 | Publication of registration | St.27 status event code:A-4-4-Q10-Q13-nap-PG1601 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:4 | |
| PN2301 | Change of applicant | St.27 status event code:A-5-5-R10-R13-asn-PN2301 St.27 status event code:A-5-5-R10-R11-asn-PN2301 | |
| FPAY | Annual fee payment | Payment date:20120828 Year of fee payment:5 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:5 | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-5-5-R10-R18-oth-X000 | |
| PN2301 | Change of applicant | St.27 status event code:A-5-5-R10-R13-asn-PN2301 St.27 status event code:A-5-5-R10-R11-asn-PN2301 | |
| FPAY | Annual fee payment | Payment date:20131017 Year of fee payment:6 | |
| PR1001 | Payment of annual fee | St.27 status event code:A-4-4-U10-U11-oth-PR1001 Fee payment year number:6 | |
| PN2301 | Change of applicant | St.27 status event code:A-5-5-R10-R11-asn-PN2301 | |
| PN2301 | Change of applicant | St.27 status event code:A-5-5-R10-R14-asn-PN2301 | |
| LAPS | Lapse due to unpaid annual fee | ||
| PC1903 | Unpaid annual fee | St.27 status event code:A-4-4-U10-U13-oth-PC1903 Not in force date:20140827 Payment event data comment text:Termination Category : DEFAULT_OF_REGISTRATION_FEE | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-5-5-R10-R18-oth-X000 | |
| PC1903 | Unpaid annual fee | St.27 status event code:N-4-6-H10-H13-oth-PC1903 Ip right cessation event data comment text:Termination Category : DEFAULT_OF_REGISTRATION_FEE Not in force date:20140827 | |
| P22-X000 | Classification modified | St.27 status event code:A-4-4-P10-P22-nap-X000 | |
| R18-X000 | Changes to party contact information recorded | St.27 status event code:A-5-5-R10-R18-oth-X000 | |
| PN2301 | Change of applicant | St.27 status event code:A-5-5-R10-R13-asn-PN2301 St.27 status event code:A-5-5-R10-R11-asn-PN2301 |